
|
学习小专题 |

|
学习小专题 |
 [元素化合物] 中学化学中反常规情况的归纳与分析 作者:鲁志超 来源: 日期:2015-12-23 17:29:22 点击:23308 所属专题:反常 一般与特殊
[元素化合物] 中学化学中反常规情况的归纳与分析 作者:鲁志超 来源: 日期:2015-12-23 17:29:22 点击:23308 所属专题:反常 一般与特殊
掌握规律是人们认识事物的重要手段,但对于化学学习过程中出现的特殊情况往往容易被疏忽。因此,在学习中不但要运用知识去认识问题,而且要分析一般规律受影响的因素和存在的条件。掌握物质的个性,并处理好共性和个性的关系。下面就中学化学中常见的反常规情况进行讨...
 [元素化合物] 强酸制取弱酸的原理及其应用 作者:程新 来源: 日期:2007-05-14 14:21:18 点击:26513 所属专题:强酸制弱酸
[元素化合物] 强酸制取弱酸的原理及其应用 作者:程新 来源: 日期:2007-05-14 14:21:18 点击:26513 所属专题:强酸制弱酸
强酸制取弱酸,指的是较强酸(可以是强酸或弱酸)可生成较弱酸。即: 强酸+弱酸盐弱酸+强酸盐 中学化学通常以 H 2 CO 3 、 的酸性作为比较标准,要求掌握常见弱酸酸性强弱顺序: 强酸制弱酸原理的应用主要体现在以下几个方面: 1. 实验室制取某些弱酸 2. 解释现象 漂...
 [元素化合物] 化学鉴源与略考 作者:潘祥泰 来源: 日期:2012-05-08 10:09:12 点击:30092 所属专题:俗名 汉字读音
[元素化合物] 化学鉴源与略考 作者:潘祥泰 来源: 日期:2012-05-08 10:09:12 点击:30092 所属专题:俗名 汉字读音
化学上的概念、名词、术语不少,有声、有色,声色俱备,给人以清澈见底的明晰感觉。就有那么一些无声、元色,或声色模糊的名称、名词、术语,使人无从理解,甚至给人以莫名其妙的感觉。笔者趣意对中学化学教学中常见而又难于回避的名称、名词和术语溯本求源略加考证,...
 [元素化合物] 中学化学中的水解反应分析 作者:玉素甫 来源: 日期:2016-02-27 16:47:37 点击:14786 所属专题:水解反应
[元素化合物] 中学化学中的水解反应分析 作者:玉素甫 来源: 日期:2016-02-27 16:47:37 点击:14786 所属专题:水解反应
对于水解反应,大家一定不会陌生的,在中学化学的很多处都出现了水解反应的概念,比如说盐类的水解以及双水解,共价化合物的水解,卤代烃的水解,酯的水解,糖类的水解和蛋白质的水解等等.在反应类型上很多的同学都是分开看这些问题,在无机反应中一般把水解反应划分到复分解反...
 [元素化合物] 非金属单质的通性和制法 作者:陈爱玉 来源: 日期:2016-01-07 17:37:02 点击:12282 所属专题:非金属及其化合物
[元素化合物] 非金属单质的通性和制法 作者:陈爱玉 来源: 日期:2016-01-07 17:37:02 点击:12282 所属专题:非金属及其化合物
1 .概述 (1) 位置及其原子结构 位置:位于元素周期表的右上角。把 6 种稀有气体除外,一般所指的非金属元素就只有 16 种。 原子结构:最外层电子数较多,原子半径较小,化学反应中容易结合电子,显示负化合价。 (2) 单质的晶体类型 分子晶体: H 2 、 X 2 、 O 2 、 O...
 [元素化合物] 金属单质的通性和制法 作者:吴乾环 来源: 日期:2016-01-07 16:43:36 点击:16937 所属专题:金属及其化合物
[元素化合物] 金属单质的通性和制法 作者:吴乾环 来源: 日期:2016-01-07 16:43:36 点击:16937 所属专题:金属及其化合物
1 .金属在元素周期表中的位置 到目前发现的 110 种元素来看,金属元素有 88 种,它们位于元素周期表的左下面, 2 .金属的结构 金属元素的原子最外层电子数一般少于 4 个。最外层电子数越少,电子层数越多,金属元素的金属性越强,还原性也越强。 金属单质是金属晶体...
 [元素化合物] 元素及其化合物的一些小规律 作者:程波 来源: 日期:2007-03-25 13:07:29 点击:22020 所属专题:元素化合物
[元素化合物] 元素及其化合物的一些小规律 作者:程波 来源: 日期:2007-03-25 13:07:29 点击:22020 所属专题:元素化合物
三构一律四平衡,单质两性化三性;化学性质是重点,性、制、存、用、构相连; 三类反应连实验,活动顺序是条绳;比较异同找规律,突出重点记方程。 复习中的注意事项: 化学性质是重点,是物质间反应,是讲物质间的相互关系;同时某些物质的一种性质,还可能是另一种物...
 [元素化合物] 高三元素及其化合物复习的思考和建议 作者:耿艳 来源:富顺二中 日期:2007-03-08 14:13:36 点击:18268 所属专题:元素化合物 复习方法
[元素化合物] 高三元素及其化合物复习的思考和建议 作者:耿艳 来源:富顺二中 日期:2007-03-08 14:13:36 点击:18268 所属专题:元素化合物 复习方法
近年高考试题中,元素及其化合物部分的试题一直是紧靠中学教学内容,涉及较多的基本知识点,特别是各部分知识的进一步融合。在选择题和无机方框图推断题中,都在重点考查元素及其化合物知识,同时配合考查考生的实验能力、计算能力,这已经是多年高考试题的一种稳定的...
 [元素化合物] 学法指导:元素及其化合物网络图及学习方法 作者:武群 来源: 日期:2020-03-05 12:59:44 点击:10023 所属专题:元素化合物 网络图
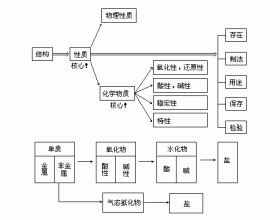
[元素化合物] 学法指导:元素及其化合物网络图及学习方法 作者:武群 来源: 日期:2020-03-05 12:59:44 点击:10023 所属专题:元素化合物 网络图
元素化合物是中学化学的核心内容,在高考中约占20%,但它同时也是考核其他化学内容的载体,如概念、理论、实验、计算等无不以元素化合物的知识为载体。元素化合物的内容庞杂、琐碎、条理性较差、逻辑性也不够强,复习时要注意: 1.充分利用已有的理论知识(物质结构理论...
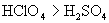 [元素化合物] 常见酸的酸性强弱的判断 作者:郝凯军 来源: 日期:2021-12-14 15:14:02 点击:25463 所属专题:常见酸 酸性
[元素化合物] 常见酸的酸性强弱的判断 作者:郝凯军 来源: 日期:2021-12-14 15:14:02 点击:25463 所属专题:常见酸 酸性
(1)含氧酸的酸性强弱的判断: ①不同元素的最高价含氧酸,元素的非金属性越强,酸性越强, 如 ②同种元素的不同价态的含氧酸,元素的化合价越高,酸性越强 氧化性: 酸性: (2)无氧酸(气态氢化物水溶液)酸性强弱的判断: ①同一主族元素,半径越大,氢化物酸性越...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。元素种类 对应物质的常考易错点 N 性质:(1)浓HNO 3 和Cu(足量)在反应时,随反应进行...
例题1:浓硫酸与金属反应的条件 题目:常温下,浓硫酸能否与金属铁发生反应? 错误答...
鲍林在研究含氧酸时,将其化学式一般写作 HRO,其中 R 代表中心原子,羟基(–OH)与...
...
一、银47Ag 银亲硫,极化能力强。在自然界中常以自然银、硫化物等形式存在,因其离子...
一、镓Ga 从铝土矿Al 2 O 3 或闪锌矿Zns的冶炼过程中提取,最后经电解制得纯净镓。 门...
一、铁 Fe 古代社会铁器时代大约起始于 前 2000 年 ,最早发现和使用的铁是来自外空的...
一、钪Sc 1、单质是柔软、银白色。熔点1500℃以上。钪常用来制特种玻璃、轻质耐高温合...