
|
学习小专题 |

|
学习小专题 |
 [注解与辨疑f] 为什么氯化钠、氯化镁、氯化铝的熔沸点依次降低? 作者:化学自习室 来源:未知 日期:2025-06-23 18:21:59 点击:67 所属专题:离子晶体
[注解与辨疑f] 为什么氯化钠、氯化镁、氯化铝的熔沸点依次降低? 作者:化学自习室 来源:未知 日期:2025-06-23 18:21:59 点击:67 所属专题:离子晶体
Na + 、Mg 2+ 、Al 3+ 的离子半径依次减小,电荷数依次增多,可是NaCl、MgCl 2 、AlCl 3 的熔点却依次降低,分别为801℃、714℃、192.4℃;沸点也依次降低,依次为1443℃、1000℃、177.8℃。 从离子极化理论解释:离子极化作用的影响因素,即离子的半径越...
 [注解与辨疑f] 为什么氧化镁的熔点比氧化铝的熔点高? 作者:化学自习室 来源:未知 日期:2025-06-17 06:31:39 点击:129 所属专题:氧化铝
[注解与辨疑f] 为什么氧化镁的熔点比氧化铝的熔点高? 作者:化学自习室 来源:未知 日期:2025-06-17 06:31:39 点击:129 所属专题:氧化铝
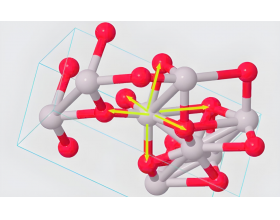
【导读】MgO熔点为2852℃;AlO熔点为2050–2054℃。 在对比中发现MgO中Mg半径比Al半径大,离子晶体中,离子半径越小,离子间的距离越近,离子键越强;Al所带电荷数比Mg多,从电荷数看,AlO中离子键应更强,熔点应该更高,而事实恰恰相反。 首先主导因素是离子键百分数,...
 [注解与辨疑f] 如何区分超分子与配合物? 作者:化学自习室 来源:未知 日期:2025-04-21 10:13:18 点击:469 所属专题:超分子
[注解与辨疑f] 如何区分超分子与配合物? 作者:化学自习室 来源:未知 日期:2025-04-21 10:13:18 点击:469 所属专题:超分子
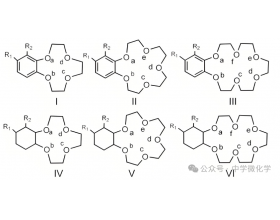
一、超分子的定义 超分子是由两种或多种分子通过非共价键相互作用(如氢键、静电作用、疏水作用、范德华力等)形成的分子聚集体。例如冠醚、DNA双螺旋结构、杯酚等都属于超分子。 冠醚,是分子中含有多个-氧-亚甲基-结构单元的大环多醚。常见的冠醚有15-冠-5、18-冠-6,...
 [注解与辨疑f] 正四面体空隙和八面体空隙 作者:化学自习室 来源:未知 日期:2025-03-18 10:00:32 点击:865 所属专题:晶体空隙
[注解与辨疑f] 正四面体空隙和八面体空隙 作者:化学自习室 来源:未知 日期:2025-03-18 10:00:32 点击:865 所属专题:晶体空隙
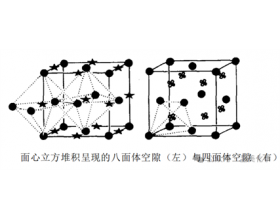
一、面心立方最密堆积 面心立方最密堆之中,八面体间隙位于 棱 心和体心,如上图可知,八面体间隙位于体心的计1个,位于12条 棱 心各计1/4,12×1/4=3,合计4个。 四面体间隙位于 晶胞 内部,在每条体对角线的1/4和3/4两处,共4×2=8个。 体对角线垂直于密置层。 正四面...
 [注解与辨疑f] 晶格能一定是离子键的键能吗? 作者:化学自习室 来源:未知 日期:2024-12-31 09:24:13 点击:821 所属专题:晶格能
[注解与辨疑f] 晶格能一定是离子键的键能吗? 作者:化学自习室 来源:未知 日期:2024-12-31 09:24:13 点击:821 所属专题:晶格能
晶格能的概念是针对离子晶体而言的,因为它描述的是离子键的强度,从某种意义上来说, 晶格能 可以看作是离子键键能的一种体现 ,但不等价于离子键键能。 晶格能是指在标准状况下,将 1mol 离子晶体 中的阴、阳离子完全气化而远离所需要吸收的能量,或者说 1mol 的 离子...
 [注解与辨疑f] 铜铁交错的黄铜矿晶体 作者:化学自习室 来源:未知 日期:2024-09-05 11:07:04 点击:522 所属专题:黄铜矿
[注解与辨疑f] 铜铁交错的黄铜矿晶体 作者:化学自习室 来源:未知 日期:2024-09-05 11:07:04 点击:522 所属专题:黄铜矿
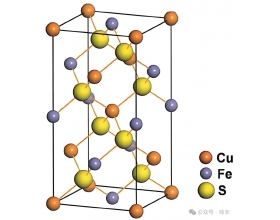
1. Cu 、Fe交错 一种CuFeS 2 (黄铜矿)的 四方晶系 晶胞结构如图。 如果将该晶体中的所有 Cu 改成 Fe (或所有 Fe 改成 Cu ),则该晶胞的上下一半就是一个立方 FeS (或 CuS )晶胞。该“立方 FeS 晶胞”涉及 14 个 Fe 原子,形成面心立方,然后在由 Fe 构成的 8 个 ...
 [注解与辨疑f] 石墨晶体中有金属键吗? 作者:化学自习室 来源:未知 日期:2024-03-24 17:35:41 点击:988 所属专题:石墨 金属键
[注解与辨疑f] 石墨晶体中有金属键吗? 作者:化学自习室 来源:未知 日期:2024-03-24 17:35:41 点击:988 所属专题:石墨 金属键
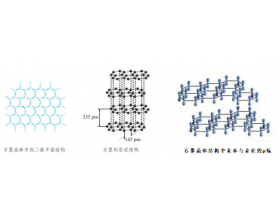
在目前有些资料中,提及石墨中含有金属键。下面我们通过4种版本(人教版、鲁科版、苏教版、沪科版)的高中化学教材对石墨的介绍一起来了解一下石墨晶体中是否含有金属键? 人教版2020版高中化学选择性必修 2 物质结构与性质第 90 页相关介绍为:由于所有的 p 轨道相互平...
 [注解与辨疑f] 晶体结构与性质基础知识常见问题集 作者:化学自习室 来源:未知 日期:2024-03-19 16:03:19 点击:1281 所属专题:晶体结构与性质
[注解与辨疑f] 晶体结构与性质基础知识常见问题集 作者:化学自习室 来源:未知 日期:2024-03-19 16:03:19 点击:1281 所属专题:晶体结构与性质
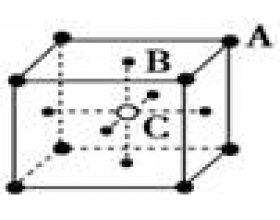
1. 晶体与非晶体有什么区别? 晶体是指具有规则几何外形的固体。其结构特征是其内的原子或分子在主维空间的排布具有特定的周期性,即隔一定距离重复出现,重复的单位可以是单个原子或分子,也可以是多个分子或原子团,重复的单位必须具备3个条件,化学组成相同,空间结构(包...
 [注解与辨疑f] 有关金刚石与石墨问题集 作者:王笃年 来源:未知 日期:2024-03-17 17:48:22 点击:296 所属专题:金刚石 石墨
[注解与辨疑f] 有关金刚石与石墨问题集 作者:王笃年 来源:未知 日期:2024-03-17 17:48:22 点击:296 所属专题:金刚石 石墨
铅笔芯的成分是碳,钻石的成分也是碳。用铅笔芯造钻石,早就已经不再是梦想。 作为碳元素的同素异形体,铅笔芯(石墨)与钻石(金刚石)为什么从颜色、到硬度,差异巨大?如何用铅笔芯制造金刚石呢? 1.根据金刚石和石墨的结构差异,如何由石墨制得金刚石? 自从人类揭开石...
 [注解与辨疑f] 金刚石硬度非常大,为什么熔点却不如石墨高? 作者:化学自习室 来源:未知 日期:2024-03-22 11:12:42 点击:511 所属专题:金刚石 石墨 熔沸点
[注解与辨疑f] 金刚石硬度非常大,为什么熔点却不如石墨高? 作者:化学自习室 来源:未知 日期:2024-03-22 11:12:42 点击:511 所属专题:金刚石 石墨 熔沸点
金刚石硬度比石墨大得多,缘于金刚石的“均匀一体化”的空间网状结构,无论从哪个方向施加外力,都需要同时破坏大量的共价键才能改变这种空间网状结构; 而石墨由于其具有层状结构,层与层之间距离过大、作用力太弱,容易被“各个击破”——先被轻易地“搓开”成极薄的...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。Na + 、Mg 2+ 、Al 3+ 的离子半径依次减小,电荷数依次增多,可是NaCl、MgCl 2 、A...
【导读】MgO熔点为2852℃;AlO熔点为2050–2054℃。 在对比中发现MgO中Mg半径比Al半径...
一、面心立方最密堆积 面心立方最密堆之中,八面体间隙位于 棱 心和体心,如上图可知...
1. Cu 、Fe交错 一种CuFeS 2 (黄铜矿)的 四方晶系 晶胞结构如图。 如果将该晶体中的...
在目前有些资料中,提及石墨中含有金属键。下面我们通过4种版本(人教版、鲁科版、苏...
金刚石硬度比石墨大得多,缘于金刚石的“均匀一体化”的空间网状结构,无论从哪个方向...
键能,常见有共价键的键能:使1mol 某共价键断裂所需的能量(键焓,kJ/mol)。 不说离子...
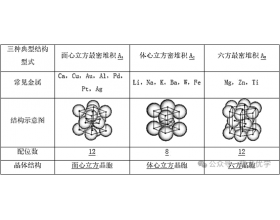
01原子结构 HCP,即密排六方晶格(Hexagonal Close Packed),是晶体结构的一种,其原...