
|
学习小专题 |

|
学习小专题 |
 [注解与辨疑f] 为什么水在4度时密度最大? 作者:王利平 来源: 日期:2007-09-10 05:45:46 点击:7863 所属专题:纯水 密度 氢键02
[注解与辨疑f] 为什么水在4度时密度最大? 作者:王利平 来源: 日期:2007-09-10 05:45:46 点击:7863 所属专题:纯水 密度 氢键02
温度改变时,水的体积变化也不寻常,它在 0-4 ℃ 范围内,一反 热胀冷缩 的普通规律,而是在 4 ℃时密度最大,高于或低于此温度时,密度都较小,因此当水结冰时,体积反而大而变轻,所以冰浮在水面上。水的这一特性,对自然界水下生命的保护有着十分重要的意义,当冬季...
 [注解与辨疑f] 几种典型晶体结构的特点分析 作者:张超鹏 来源: 日期:2016-01-30 15:48:08 点击:12503 所属专题:晶体结构
[注解与辨疑f] 几种典型晶体结构的特点分析 作者:张超鹏 来源: 日期:2016-01-30 15:48:08 点击:12503 所属专题:晶体结构
有关晶体结构的知识是高中化学中的一个难点,它能很好地考查同学们的观察能力和三维想像能力,而且又很容易与数学、物理特别是立体几何知识相结合,是近年高考的热点之一。熟练掌握NaCl、CsCl、CO 2 、SiO 2 、金刚石、石墨、C 60 等晶体结构特点,理解和掌握一些重要...
 [注解与辨疑f] 晶体类型判定法 作者:杨董 来源: 日期:2016-01-30 15:50:35 点击:10217 所属专题:晶体类型
[注解与辨疑f] 晶体类型判定法 作者:杨董 来源: 日期:2016-01-30 15:50:35 点击:10217 所属专题:晶体类型
晶体类型的判断,不论在选择题还是在综合推断填空题,都是常考常新的知识点。下面归纳晶体判断的一些依据,储备这些知识,做到有备无患。 一、根据各类晶体的定义判断: 根据构成晶体的粒子和粒子间的作用力类别进行判断。如由阴、阳离子间通过离子键结合而形成的晶体...
 [注解与辨疑f] 离子晶体、分子晶体和原子晶体 作者:爱莉 来源: 日期:2016-01-30 16:01:12 点击:15548 所属专题:离子晶体 分子晶体 原子晶体
[注解与辨疑f] 离子晶体、分子晶体和原子晶体 作者:爱莉 来源: 日期:2016-01-30 16:01:12 点击:15548 所属专题:离子晶体 分子晶体 原子晶体
在学习中要加强对化学键中的非极性键、极性键、离子键、晶体类型及结构的认识与理解;在掌握微粒半径递变规律的基础上,分析离子晶体、原子晶体、分子晶体的熔点、沸点等物理性质的变化规律;并在认识晶体的空间结构的过程中,培养空间想象能力及思维的严密性和抽象性...
 [注解与辨疑f] 判断晶体类型的方法 作者:陈丽娟 来源: 日期:2016-01-30 16:03:03 点击:9692 所属专题:晶体类型
[注解与辨疑f] 判断晶体类型的方法 作者:陈丽娟 来源: 日期:2016-01-30 16:03:03 点击:9692 所属专题:晶体类型
晶体结构的确定及晶体物理性质的比较在高考中的比重有增大的趋势.难度也有所增加.对知识的要求比较细致深刻.应用能力要求较高. 1.判断晶体类型的方法? (1)依据组成晶体的晶格质点和质点间的作用判断? 离子晶体的晶格质点是阴、阳离子.质点间的作用是离子键;原...
 [注解与辨疑f] 晶体的通性和分类 作者:赵宝 来源: 日期:2016-01-30 16:13:40 点击:5971 所属专题:晶体性质
[注解与辨疑f] 晶体的通性和分类 作者:赵宝 来源: 日期:2016-01-30 16:13:40 点击:5971 所属专题:晶体性质
应用X射线研究晶体内部结构的大量实验证明,一切晶体在结构上不同于非晶体(以及液体、气体)的最本质的特征,是组成晶体的微粒(离子、原子、分子等)在三维空间中有规则的排列,具有结构的周期性。所谓结构的周期性,是指同一种微粒在空间排列上每隔一定距离重复出...
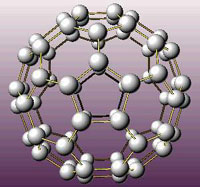 [注解与辨疑f] 石墨是混合晶体 作者:胡长胜 来源: 日期:2006-09-11 07:25:42 点击:5089 所属专题:石墨 混合型晶体
[注解与辨疑f] 石墨是混合晶体 作者:胡长胜 来源: 日期:2006-09-11 07:25:42 点击:5089 所属专题:石墨 混合型晶体
石墨到底是什么晶体呢?有人认为石墨是原子晶体;其实石墨不只是一种单一的晶体类型,而是几种晶体混合而成的。 在石墨晶体中,同层的碳原子以 sp 2 杂化形成共价键,海一个碳原子以三个共价键与另外三个原子相连。六个碳原子在同一个平面上形成了正六连连形的环,伸展...
 [注解与辨疑f] 晶体的基本性质 作者:周书峰 来源:摘抄于因特网 日期:2016-01-30 16:15:47 点击:6438 所属专题:晶体性质
[注解与辨疑f] 晶体的基本性质 作者:周书峰 来源:摘抄于因特网 日期:2016-01-30 16:15:47 点击:6438 所属专题:晶体性质
晶体的基本性质由晶体的周期性结构决定的。晶体具有均匀性和各向异性。均匀性如晶体的化学组成、密度等性质在晶体中各部分都是相同的,这是由于晶体周期性结构中的周期很小,宏观上分辨不出的缘故。然而晶体中沿不同方向,原子或分子排列的情况不同,因此在不同方向上...
 [注解与辨疑f] 金属键和金属晶体结构理论 作者:李萱 来源:摘抄于因特网 日期:2016-01-30 16:19:49 点击:21455 所属专题:金属键 金属晶体
[注解与辨疑f] 金属键和金属晶体结构理论 作者:李萱 来源:摘抄于因特网 日期:2016-01-30 16:19:49 点击:21455 所属专题:金属键 金属晶体
在高中化学课本“金属键”一节中,简略地讲了金属键的自由电子理论和金属晶体的圆球密堆积结构。在本节中将介绍这两种理论的有关史实,并对理论本身进一步加以阐述。 一、金属键理论及其对金属通性的解释 一切金属元素的单质,或多或少具有下述通性:有金属光泽、不透明...
 [注解与辨疑f] 二氧化硅晶体中最小环由十二个原子构成 作者:黄勇 来源:摘抄于因特网 日期:2022-08-12 07:52:28 点击:26134 所属专题:二氧化硅晶胞
[注解与辨疑f] 二氧化硅晶体中最小环由十二个原子构成 作者:黄勇 来源:摘抄于因特网 日期:2022-08-12 07:52:28 点击:26134 所属专题:二氧化硅晶胞
现行高中教材给出二氧化硅晶体的平面结构如下图1。该示意图准确地表示了二氧化硅晶体结构中,每个硅原子结合4个氧原子,同时每个氧原子结合2个硅原子。这样很好地解释了为什么二氧化硅的化学式是SiO 2 。...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。Na + 、Mg 2+ 、Al 3+ 的离子半径依次减小,电荷数依次增多,可是NaCl、MgCl 2 、A...
【导读】MgO熔点为2852℃;AlO熔点为2050–2054℃。 在对比中发现MgO中Mg半径比Al半径...
一、面心立方最密堆积 面心立方最密堆之中,八面体间隙位于 棱 心和体心,如上图可知...
1. Cu 、Fe交错 一种CuFeS 2 (黄铜矿)的 四方晶系 晶胞结构如图。 如果将该晶体中的...
在目前有些资料中,提及石墨中含有金属键。下面我们通过4种版本(人教版、鲁科版、苏...
金刚石硬度比石墨大得多,缘于金刚石的“均匀一体化”的空间网状结构,无论从哪个方向...
键能,常见有共价键的键能:使1mol 某共价键断裂所需的能量(键焓,kJ/mol)。 不说离子...
01原子结构 HCP,即密排六方晶格(Hexagonal Close Packed),是晶体结构的一种,其原...