
|
学习小专题 |

|
学习小专题 |
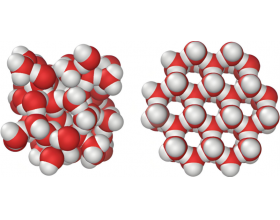 [注解与辨疑e] 氢键的强弱比较 作者:化学自习室 来源:未知 日期:2025-08-06 09:29:45 点击:1662 所属专题:氢键强弱
[注解与辨疑e] 氢键的强弱比较 作者:化学自习室 来源:未知 日期:2025-08-06 09:29:45 点击:1662 所属专题:氢键强弱
一、知识梳理 (一)影响氢键强弱的因素 1. 供体原子的电负性:电负性越高,对H的极化作用越强,氢键越强。 电负性顺序:F(4.0)O(3.5)N(3.0) 氢键强度顺序:F-H…FO-H…ON-H…N 2.受体原子的电负性:受体原子电负性越高,越容易吸引H的δ+电荷,氢键越强。 例如:O-H…O...
 [注解与辨疑e] 氨和水中有多少氢键?氨水中氢键主要存在形式是什么? 作者:化学自习室 来源:未知 日期:2025-04-18 10:10:34 点击:899 所属专题:氨水 氢键
[注解与辨疑e] 氨和水中有多少氢键?氨水中氢键主要存在形式是什么? 作者:化学自习室 来源:未知 日期:2025-04-18 10:10:34 点击:899 所属专题:氨水 氢键
1mol 氨中氢键数量分析 一、氢键形成机制 NH分子结构 H原子作为氢键供体(需与高电负性原子如N、O、F结合);孤对电子作为氢键受体(存在于另一分子中)。 每个NH分子含3个N-H键和一个孤对电子位于N原子上。 二、不同状态下氢键数量 1、固态氨(晶体) 理想情况:每个NH分子...
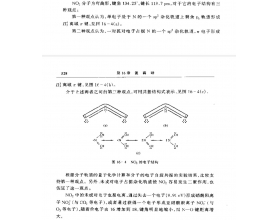 [注解与辨疑e] 二氧化氮的氮原子是什么杂化? 作者:化学自习室 来源:未知 日期:2025-04-14 10:51:20 点击:2238 所属专题:二氧化氮
[注解与辨疑e] 二氧化氮的氮原子是什么杂化? 作者:化学自习室 来源:未知 日期:2025-04-14 10:51:20 点击:2238 所属专题:二氧化氮
二氧化氮(NO)中氮原子的杂化类型为 sp杂化,具体分析如下: 1.计算 n (的价层电子对数) =2+1/2(5-2×2)=2.5 注意:这里的0.5对即单电子,根据VSePr理论,单电子视为一个“等效电子对”,因此氮原子的价层电子对总数为 3对(2个σ键电子对 + 1个单电子等效对)。 2. 杂...
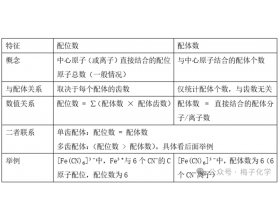 [注解与辨疑e] 配位数和配体数概念辨析 作者:化学自习室 来源:未知 日期:2025-03-25 09:32:01 点击:154550 所属专题:配位数
[注解与辨疑e] 配位数和配体数概念辨析 作者:化学自习室 来源:未知 日期:2025-03-25 09:32:01 点击:154550 所属专题:配位数
一、概念辨析 1. 区别与联系 注:配位数和配位键之间没有直接的、必然的关系。 2. 典型实例分析 ( 1 )单齿配体(配位数 = 配体数) 例如: [Co(NH ) ] 中,配体数 =6 ,有 6 个 NH 分子(每个 NH 是单齿配体)。 配位数 =6 ,每个 NH 提供 1 个 N 原子与 Co 结合。 所...
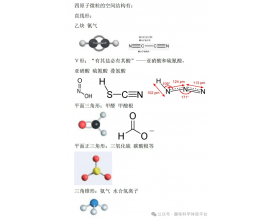 [注解与辨疑e] 四原子微粒的空间结构 作者:化学自习室 来源:未知 日期:2025-03-24 15:47:22 点击:242 所属专题:分子空间结构
[注解与辨疑e] 四原子微粒的空间结构 作者:化学自习室 来源:未知 日期:2025-03-24 15:47:22 点击:242 所属专题:分子空间结构
...
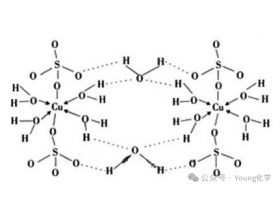 [注解与辨疑e] 五水硫酸铜晶体中的化学键 作者:化学自习室 来源:未知 日期:2025-03-11 08:08:12 点击:874 所属专题:硫酸铜
[注解与辨疑e] 五水硫酸铜晶体中的化学键 作者:化学自习室 来源:未知 日期:2025-03-11 08:08:12 点击:874 所属专题:硫酸铜
五水硫酸铜晶体( CuSO45H2O )中存在多种化学键,主要包括: 离子键 存在位置: 铜离子 (Cu2+)和硫酸根离子(SO42)之间。 形成原因: Cu2+带正电荷, SO42带负电荷,它们之间由于静电引力形成离子键。 配位键 存在位置:铜离子( Cu2+)与四个水分子之间。 形成原因...
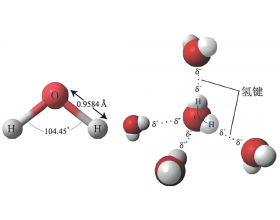 [注解与辨疑e] 如何比较氢键的强弱? 作者:化学自习室 来源:未知 日期:2025-08-06 09:30:08 点击:2184 所属专题:氢键强弱
[注解与辨疑e] 如何比较氢键的强弱? 作者:化学自习室 来源:未知 日期:2025-08-06 09:30:08 点击:2184 所属专题:氢键强弱
【导读】 以下是快速判定氢键强弱的基本原则,实际案例中经常会进一步考虑综合因素的影响,而非简单单一因素。 ①看供体原子 : FONCl (电负性优先,原子半径次之) ②看受体原子 : 受体电负性越高,氢键越强(如 ONCl ) ③看键长和角度 : 键长越短、越接近线性,氢...
 [注解与辨疑e] 二氧化氯按照价电子互斥理论是3.5,而实际上Cl是sp2杂化? 作者:化学自习室 来源:未知 日期:2025-03-03 16:12:08 点击:2095 所属专题:二氧化氯
[注解与辨疑e] 二氧化氯按照价电子互斥理论是3.5,而实际上Cl是sp2杂化? 作者:化学自习室 来源:未知 日期:2025-03-03 16:12:08 点击:2095 所属专题:二氧化氯
根据价电子互斥理论, ClO 2 中氯原子周围的价电子对数计算为 3.5,理论上应倾向于 sp 3 杂化。然而,实际情况是氯原子采用 sp 2 杂化,这可以通过以下几点来理解: 大π键的形成:在 ClO 2 分子中,氯原子与两个氧原子之间可以形成三中心五电子的大π键。这种大π键的形成...
 [注解与辨疑e] 哪些轨道可以形成π键? 作者:化学自习室 来源:未知 日期:2025-02-20 10:09:18 点击:2156 所属专题:π键
[注解与辨疑e] 哪些轨道可以形成π键? 作者:化学自习室 来源:未知 日期:2025-02-20 10:09:18 点击:2156 所属专题:π键
常见形成π键的轨道如下: p-p π键:最常见,如乙烯、氧气 d-p π键:常见于过渡金属配合物,如四羰基合镍 d-d π键:常见于某些金属化合物,如八氯化二铼 f-d π键:较少见,某些锕系元素的配合物中理论上存在 离域π键(大π键):常见于多原子分子,如苯、吡啶、二氧化硫 1. p-...
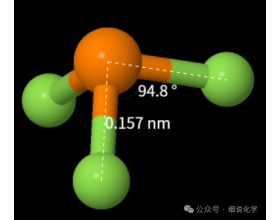 [注解与辨疑e] PH3与PF3键角大小比较 作者:化学自习室 来源:未知 日期:2025-02-18 17:16:45 点击:1196 所属专题:键角
[注解与辨疑e] PH3与PF3键角大小比较 作者:化学自习室 来源:未知 日期:2025-02-18 17:16:45 点击:1196 所属专题:键角
PH3与PF3两者中心原子杂化方式及孤对电子数都相同,F原子的电负性比H的电负性更大,P-F成键电对靠近氟原子P,理论上应是PH3键角大于PF3,但事实上确完全相反, 查阅资料,发现PH3键角小于PF3,PF3分子中由于F原子上的孤对电子对占有P原子的3d空轨道, 形成p-dπ配键,增...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。一、超分子的定义 超分子是由两种或多种分子通过非共价键相互作用(如氢键、静电作用...
要理解形成配位键不会改变化合价的核心,需从化合价的定义和配位键的成键本质两个层面...
一、基础概念 1. 超分子的定义 超分子是两种或两种以上分子(广义含离子)通过分子间...
...
硼是IIA族元素中唯一的非金属元素,性质与本族兄长们的相似度乏善可陈。远亲不如近邻...
...
弱作用力的“强作用”---- 《物质结构与性质》苏教版134学科提炼 微粒间的作用力类型...
2023年湖南卷16题的第(5)问(见图一), 第(5)问 “ 引发剂 C 6 H 5 CH 2 Cl 、 C ...