
|
学习小专题 |

|
学习小专题 |
 [注解与辨疑a] 元素汉字名称的读音 作者:陈艳丽 来源:未知 日期:2021-12-29 14:13:21 点击:7024 所属专题:元素读音
[注解与辨疑a] 元素汉字名称的读音 作者:陈艳丽 来源:未知 日期:2021-12-29 14:13:21 点击:7024 所属专题:元素读音
一些化学元素平时接触太少,其汉字读音比较陌生,有的甚至从来没去读过。秀才读半边,多数是对的,有些却是错。就如涞读来,法却不读去。锝( 43 Tc)读得,铁却不读失。汉字这块骨头可不是那么好啃的。 氮不读炎,读淡。钠读纳,不读内。氯不读录,读绿,含淡绿色之意。...
 [注解与辨疑a] 物质结构必修学习误区解析 作者:李萱 来源:未知 日期:2011-06-23 13:05:08 点击:17715 所属专题:物质结构必修
[注解与辨疑a] 物质结构必修学习误区解析 作者:李萱 来源:未知 日期:2011-06-23 13:05:08 点击:17715 所属专题:物质结构必修
疑点1:所有的原子都是由质子、中子、电子构成。 解析:一般的原子都是由质子、电子和中子构成,但普通氢原子没有中子。 疑点2:若两种原子核外电子排布相同,则一定属于同种元素。 解析:核外电子相同的原子的质子数一定相同,质子数决定元素种类,质子数相同的原子...
 [注解与辨疑a] 核外电子运动规律与电子云概念 作者:徐俊龙 来源:未知 日期:2021-12-17 09:18:19 点击:13646 所属专题:电子云
[注解与辨疑a] 核外电子运动规律与电子云概念 作者:徐俊龙 来源:未知 日期:2021-12-17 09:18:19 点击:13646 所属专题:电子云
原子核外的电子,作为我们认识的一种物质,它们的运动形式有什么特点?要回答这个问题,应先从微观世界的特点谈起。人们的感觉器官不能直接感受到的较小的物体及其运动现象,称为微观物体和微观现象,二者总称为微观世界。分子、原子、电子等均为微观物体。微观世界与宏...
 [注解与辨疑a] 概念辨析:H2、D2、T2三者之间的关系 作者:安勃 来源:未知 日期:2018-08-13 09:53:55 点击:31735 所属专题:同位素 纯净物
[注解与辨疑a] 概念辨析:H2、D2、T2三者之间的关系 作者:安勃 来源:未知 日期:2018-08-13 09:53:55 点击:31735 所属专题:同位素 纯净物
H 氕 piē D 氘 dāo T 氚 chuān 一、H 2 、 D 2 、 T 2 是同种单质 纯净物是由同种物质(只限制元素的种类及组成相同,默认同位素是自然界中都一样的比例)组成的,它具有一定的组成,可以用一种化学式来表示。由于H 在自然界中以...
 [注解与辨疑a] 元素特殊性质归纳 作者:易友生 来源:未知 日期:2021-12-29 09:35:19 点击:12638 所属专题:短周期元素
[注解与辨疑a] 元素特殊性质归纳 作者:易友生 来源:未知 日期:2021-12-29 09:35:19 点击:12638 所属专题:短周期元素
(1)单质密度最小的元素 ( H ) (2)单质密度最小的金属元素 ( Li ) (3)单质硬度最大的元素 ( C ) (4)地壳中含量最丰富的元素 ( O ) (5)地壳中含量最丰富的金属元素 ( Al ) (6)空气中含量最多的元素 ( N ) (7)自然界形成化合物种类最多的元素 ( C ) (8)单质氧化性最强的元...
 [注解与辨疑a] 关于氧有正价但没有最高正价的分析 作者:方丽妹 来源:未知 日期:2010-07-28 16:16:42 点击:12236 所属专题:化合价
[注解与辨疑a] 关于氧有正价但没有最高正价的分析 作者:方丽妹 来源:未知 日期:2010-07-28 16:16:42 点击:12236 所属专题:化合价
元素周期表中,主族元素的最高正价等于它的族序数,但氧和氟除外。这是因为两者氧化性太强,其中氟因为是氧化性最强的非金属元素,没有其他元素能夺取氟的电子,所以氟只有单质的零价和负价,没有正价;而氧的氧化性也很强,一般也显负价,但由于氟的氧化性更强,所以在氧与...
 [注解与辨疑a] 元素化合价与物质结构的关系 作者:张世敏 来源:未知 日期:2010-03-17 20:31:02 点击:12690 所属专题:化合价
[注解与辨疑a] 元素化合价与物质结构的关系 作者:张世敏 来源:未知 日期:2010-03-17 20:31:02 点击:12690 所属专题:化合价
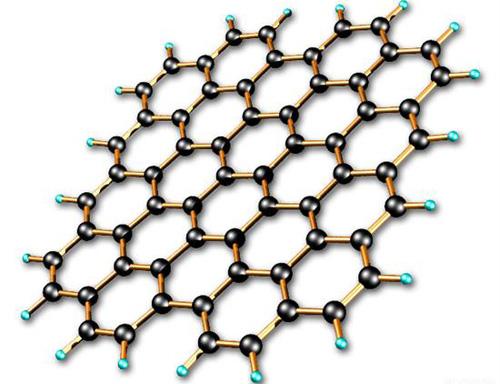
在对乙炔进行讲解时,出现的金属碳化物与水反应所得产物的判断问题,使学生提出了一些疑问。这些金属碳化物原来的结构是什么?为什么CaC 2 和水生成乙炔,Al 4 C 3 和水反应生成甲烷? 针对这些问题,首先应该让学生了解,得到怎样的生成物和原来的金属碳化物的结构有关...
 [注解与辨疑a] 化学键难点解析 作者:张世敏 来源:未知 日期:2012-12-03 11:28:08 点击:22000 所属专题:化学键
[注解与辨疑a] 化学键难点解析 作者:张世敏 来源:未知 日期:2012-12-03 11:28:08 点击:22000 所属专题:化学键
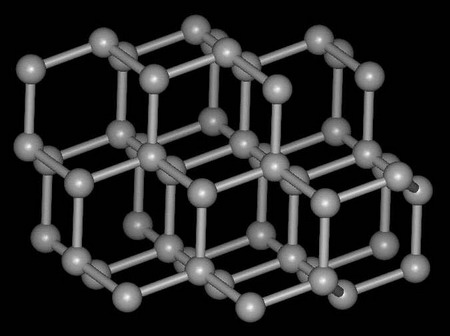
一、化学键概念中的相互作用 正确理解相互作用含义需要注意以下几个关键词。一是相互作用的微粒,除了原子外,还包括原子团以及它们得失电子而形成离子,如 Na + 、 Cl - 、 NH 4 + 、 NO 3 - 等;二是相邻与强烈,二者是一致的,只有相邻的原子间,相互作用才会强烈...
 [注解与辨疑a] 怎样证明金属、非金属性的强弱 作者:陈螯 来源: 日期:2016-01-08 15:18:53 点击:20639 所属专题:金属性 非金属性
[注解与辨疑a] 怎样证明金属、非金属性的强弱 作者:陈螯 来源: 日期:2016-01-08 15:18:53 点击:20639 所属专题:金属性 非金属性
一、 证明金属性强弱的方法 (一)理论法 1、 同一主族,从上至下,金属性逐渐增强 在同一主族的元素中,由于从上到下电子层数增多,原子半径增大,核对核外电子的引力减少,失电子能力逐渐增强,得电子能力逐渐减弱,所以元素的金属性逐渐增强,非金属性逐渐减弱。 2...
 [注解与辨疑a] “化学键”中的定与不定 作者:周广 来源: 日期:2016-05-19 17:05:19 点击:9613 所属专题:化学键 不一定
[注解与辨疑a] “化学键”中的定与不定 作者:周广 来源: 日期:2016-05-19 17:05:19 点击:9613 所属专题:化学键 不一定
1.离子化合物中一定含有离子键,但不一定不含共价键。例如,离子化合物 NaOH和NH 4 Cl分别含有O-H共价键和N-H共价键。 2.共价化合物一定只含共价键,一定不含离子键。 3.含有离子键的化合物,不一定含有金属元素。例如, NH 4 Cl,NH 4 NO 3 。 4.金属元素和非金属元素...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。人教版高中化学必修第一册2019年6月第1版2024年7月第8次印刷P 10 3 讲解卤素单质与氢...
冰在0℃开始融化。这是本家都熟悉的事儿。 然而,世界上竟有热冰它在3.8℃方才融化! ...
1. 为什么 HF 分子间氢键比 H 2 O 分子间氢键强,而 HF 的沸点却比 H 2 O 的低? 由于...
1、为什么氧、氟没有最高正价?(朱朝宇) 氟是非金属性最强的元素,理论上没有哪种物...
1.如何理解分子间作用力的本质也是静电作用? 首先,在极性分子与极性分子之间,存在...
【关于化学键(Chemical bond)】: 化学键(Chemical bond)实质上是电性的微观作用...
...
准金属(metalloid),又称为半金属(semimetal),介于金属和非金属之间的物质。准金...