
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
1、离域π键的概念 :
把分子轨道理论的一些结果,引入价键理论,来解释分子的结构和一些性质,产生了离域π键的概念。离域π键不同于两原子间的π键,是由三个或三个以上原子形成的π键。不像普通π键,它的成键电子不再局限在两个原子之间的区域,而是在多个原子之间运动,从而把这多个原子键合起来。所以也叫大π键,或多原子π键。一般生成离域π键的体系,其能量降低。
2、离域π键的形成条件
①所有参与离域π键的原子都必须在同一平面内,即连接这些原子的中心原子只能采取sp或sp2杂化。
②所有参与离域π键的原子都必须提供一个或两个相互平行的p轨道。
③参与离域π键的p轨道上的电子数必须小于2倍的p轨道数。即
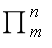
中n<2m
3、计算法分析离域π键依据:
价电子=σ键电子+孤电子+π键电子,杂化轨道数目=σ键电子对数目+孤电子对数目,则π键电子数目=价电子数-σ键电子-孤电子数
将所有原子按照中心原子一样的杂化方式分析。
(1)中心原子采用sp2杂化的分析,例CO32-
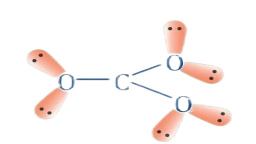
中心原子C原子的价电子数为4+2=6,形成3个σ键,sp2杂化,杂化轨道数目=σ键数目+孤电子对数目,孤电子对数为0,每个氧原子都按sp2杂化,形成1个σ键,孤电子对数为2,则π键电子数目=价电子数-σ键电子数-孤电子数
π键的总电子数=(4+2+6×3)-6-3×4=6.离域π键为
![]() 。
。
SO3、NO3-和CO32-是等电子体,成键情况相同均是![]() 。
。
(2)中心原子采取sp杂化有两套π键。例:N₂O
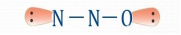
π键的总电子数=(6+5×2)-4-4=8.
故有两个
![]()
CO2、 SCN-和N₂O是等电子体也有两个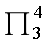
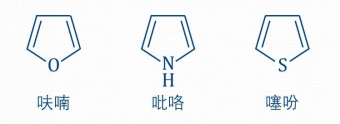
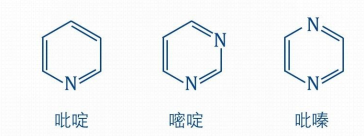
(3)芳香环等共轭体系也可用此方法分析。
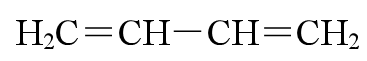
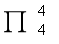
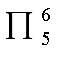
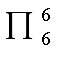

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
一、先定框架:4步快速判定有没有大π键 1. 看结构 :必须是平...
目前高考试题对对映异构的考查主要集中在有机分子中手性碳原...
...
...
配合物的配位数是指直接同中心离子(或原子)配位的原子数目。...
分析: 依据价层电子对数计算公式分析, 可得价层电子对数=...