
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
化学与物理结合的计算,主要涉及两个公式:
(1)Q=I×t=n(e-)×F,F计算时一般取值96500 C·mol-1。
(2)W=U×I×t。
1.[(2015·全国卷Ⅱ,26(1)(2))]酸性锌锰干电池是一种一次性电池,外壳为金属锌,中间是碳棒,其周围是由碳粉、MnO2、ZnCl2和NH4Cl等组成的糊状填充物。该电池放电过程产生MnOOH。
①该电池的正极反应式为____________________。
电池反应的离子方程式为_____________________________。
②维持电流强度为0.5A,电池工作5分钟,理论上消耗锌___________g。(已知F=96500 C·mol-1)
[答案]:①MnO2+H++e-===MnOOH;2MnO2+Zn+2H+===2MnOOH+Zn2+②0.05
[解析]:维持电流强度为0.5A,电池工作五分钟,则通过的电量是)Q=I×t=0.5×300=150 C,因此通过电子的物质的量是
![]()
,锌在反应中失去2个电子,则理论消耗Zn的质量是
![]()
2.新型固体燃料电池的电解质是固体氧化锆和氧化钇,高温下允许氧离子(O2-)在其间通过。如图所示,其中多孔电极不参与电极反应。
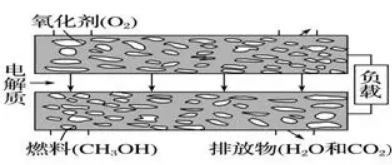
(1)①该电池的负极反应式为_______________。
②如果用该电池作为电解装置,当有16g 甲醇发生反应时,则理论上提供的电量表达式为________C(1个电子的电量为1.6×10-19C)。
(2)以CH4(g)为燃料可以设计甲烷燃料电池,该电池以稀H2SO4作电解质溶液,其负极电极反应式为_______,已知该电池的能量转换效率为86.4%,甲烷的燃烧热为-890.3kJ·mol-1,则该电池的比能量为_____kW·h·kg-1,(结果保留1位小数,比能量=![]() ,1kW·h=3. 6×106J)。
,1kW·h=3. 6×106J)。
[答案]:(1)①CH3OH-6e-+3O2-===CO2+2H2O
②0.5 mol×6×1.6×10-19C×6.02×1023mol-1(或2.890×105)
(2)CH4-8e-+2H2O===CO2+8H+ 13.4
[解析]:甲烷燃料电池中,甲烷在负极被氧化,电解质为硫酸,负极反应式:CH4-8e-+2H2O===CO2+8H+,该电池的能量转换效率为86.4%,甲烷的燃烧热为-890.3 KJ·mol-1,
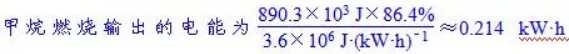

![]()
3.二甲醚(CH3OCH3)是无色气体,可作为一种新型能源。若电解质为酸性,二甲醚直接燃料电池的负极反应为__________________,
一个二甲醚分子经过电化学氧化,可以产生________个电子的电量;该电池的理论输出电压为1.20V,能量密度E=_______________
(列式计算。能量密度=![]() ,1kW·H=3.6×106J)。
,1kW·H=3.6×106J)。
[答案]:CH3OCH3-12e-+3H2O===2CO2+12H+ 12
![]()
[解析]:二甲醚直接燃料电池的负极发生氧化反应,反应的电极方程式为:CH3OCH3-12e-+3H2O===2CO2+12H+,显然1个二甲醚分子经过电化学氧化,可以产生12个e-的电量;1 kg 二甲醚的物质的量n=1000/46 mol,可以产生的1000/46×12×6.02×1023个e-的电量,1个e-的电量为1.602×10-19C。
1 kg 二甲醚输出的电能:
W=UIt=UQ=1.20×1000/46×12×6.02×1023×1.602×10-19J
=3.02×107 J=3.02×107/3.6×106(kW·h)=8.39 kW·h
二甲醚直接燃料电池能量密度或比能量E=8.39 KW·h·kg-1
用同样的方法,通过列式计算求出甲醇直接燃料电池的理论输出电压是多少?
若电解质为酸性,甲醇直接燃料电池的负极电极反应式为:
CH3OH+H2O-6e-=CO2+6H+,1个甲醇分子经过电化学氧化,可以转移6个e-;1 kg 甲醇的物质的量n=1000/32 mol,可以转移的1000/32×6×6.02×1023个e-的电量;
1个e-的电量是1.602×10-19C,
1 kg 二甲醚输出的电能:
W=UIt=UQ=U×1000/32×6×6.02×1023×1.602×10-19
=1.808×107U=1.808×107/3.6×106U(kW·h·V-1)
=5.02 U(kW·h·V-1)
已知,甲醇直接燃料电池的能量密度(5.93 KW·H·kg-1)
E=5.93kW·h·kg-1=5.02 UkW·H·kg-1·V-1U=1.18 V
若电解质为NaOH碱性溶液,同理也可算出理论输出电压是1.18 V;根据P=W/T,功率可以由电池输出的电能换算得到,求出比功率。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
锌溴液流电池是一种大规模储能电池,相比传统铅酸电池锂离子...
电化学是高中化学的重要组成部分,是高考的必考内容,然而,...
电化学原理是普通高中化学选择性必修1化学反应原理中的重要...
一、判断有机物得失电子 例1: 微生物电池是指在微生物的作用...
近几年全国卷高考电化学装置一般都带有离子交换膜,此类题目...
【 知识归纳 】 1. 浓差电池的定义 物质由 高浓度 向 低浓度 扩...