
|
学习小专题 |

|
学习小专题 |
 [课题与实验k] 铁氰化钾能将铁氧化吗? 作者:化学自习室 来源:未知 日期:2026-03-10 09:12:42 点击:715 所属专题:铁氰化钾
[课题与实验k] 铁氰化钾能将铁氧化吗? 作者:化学自习室 来源:未知 日期:2026-03-10 09:12:42 点击:715 所属专题:铁氰化钾
为什么取Fe电极区溶液少量于试管内,再加入铁氰化钾? 铁氰化钾中的[Fe(CN)]结构稳定,Fe被氰基配体紧密包裹,难以直接接触铁单质,因此传统认为两者无法发生氧化还原反应。 对比①②,...
 [课题与实验k] 实验考点系列:钢铁的电化学腐蚀与防护 作者:化学自习室 来源:未知 日期:2025-05-19 19:05:03 点击:654 所属专题:电化学腐蚀
[课题与实验k] 实验考点系列:钢铁的电化学腐蚀与防护 作者:化学自习室 来源:未知 日期:2025-05-19 19:05:03 点击:654 所属专题:电化学腐蚀
一、电化学腐蚀: 实验原理: 审题点1:看腐蚀类型是否正确 示例:下述装置能否探究铁的析氢腐蚀? 答:× 解析:析氢腐蚀的介质为酸性较强的电解质,食盐水为中性,Fe发生吸氧腐蚀。 审题点2:氢后金属不论环境的酸碱性,只发生吸氧腐蚀 示例:下述装置能否探究铜的析...
 [课题与实验k] 如何手工制作原电池中的盐桥? 作者:化学自习室 来源:未知 日期:2025-03-10 11:21:31 点击:1011 所属专题:盐桥
[课题与实验k] 如何手工制作原电池中的盐桥? 作者:化学自习室 来源:未知 日期:2025-03-10 11:21:31 点击:1011 所属专题:盐桥
常见的氯化钾琼脂块盐桥制作方法有三种: 一、用于全固态硝酸根离子选择电极的氯化钾琼脂块制作方法 1:称取 2-4g 琼脂溶于 96-98g 去离子水中,采用水浴加热法将混合物加热至 90-97°C,待琼脂全部溶解。 2:加入 25-35g 氯化钾,保持温度不变待用。 3:将橡胶圈一端放...
 [课题与实验k] 铜锌原电池锌为什么有气泡 作者:岳文虹 来源:未知 日期:2023-05-17 15:15:04 点击:4540 所属专题:铜锌原电池
[课题与实验k] 铜锌原电池锌为什么有气泡 作者:岳文虹 来源:未知 日期:2023-05-17 15:15:04 点击:4540 所属专题:铜锌原电池
理论上,在 Cu-Zn 单液原电池中,溶液中的 H + 在 Cu 电极表面得到电子生 成 H 2 ,产生气泡;Zn 片发生溶解,没有气体生成。 但实际实验中,由于 Zn 电 极不纯会不可避免地发生自腐蚀现象,在 Zn 电极表面也产生了大量气泡。 同时最新研究表明,即使用纯度极高的Zn 片来...
 [课题与实验k] 电解CuCl2溶液过程中,电解液为何变黑? 作者:化学自习室 来源:未知 日期:2021-12-23 14:15:14 点击:1674 所属专题:电解氯化铜
[课题与实验k] 电解CuCl2溶液过程中,电解液为何变黑? 作者:化学自习室 来源:未知 日期:2021-12-23 14:15:14 点击:1674 所属专题:电解氯化铜
从电解CuCl 2 溶液的过程来分析,无论是CuCl 2 的浓溶液,还是稀溶液,电解反应开始时,均发生了 如下反应: 2Cl--2e - =Cl 2 ;2e-+Cu 2+ =Cu。 如果CuCl 2 溶液是饱和溶液,反应一开始就会有铜生成,这是因为生成的铜处于浓度很高的铜离子的氧化性环境。这 样就发...
 [课题与实验k] 电解精炼铜的CuSO4溶液为什么常用硫酸酸化? 作者:化学自习室 来源:未知 日期:2020-11-16 08:40:52 点击:1734 所属专题:铜的精炼
[课题与实验k] 电解精炼铜的CuSO4溶液为什么常用硫酸酸化? 作者:化学自习室 来源:未知 日期:2020-11-16 08:40:52 点击:1734 所属专题:铜的精炼
电解过程中伴随着电能转化为化学能,同时也会产生热能,温度升高,促进Cu 2+ 水解,为了抑制Cu 2+ 的水解,防止阳极附近Cu 2+ 水解产生Cu(OH) 2 沉淀,为了增强Cu 2+ 的浓度,便于阴极析出Cu,所以常加入稀硫酸,同时也能增强电解液的导电性。...
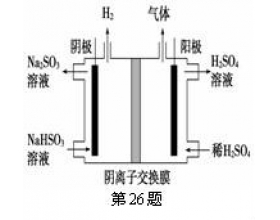 [课题与实验k] 电解亚硫酸钠、氯化亚铁、氯化铁、锰酸钾溶液 作者:吴文中 来源:未知 日期:2018-01-18 10:31:32 点击:4104 所属专题:电解原理 放电顺序
[课题与实验k] 电解亚硫酸钠、氯化亚铁、氯化铁、锰酸钾溶液 作者:吴文中 来源:未知 日期:2018-01-18 10:31:32 点击:4104 所属专题:电解原理 放电顺序
一.电解Na 2 SO 3 溶液 【分析】溶液中存在的离子有H + 、OH - 、Na + 、S O 3 2 - .简单分析就是要比较H + 和Na + 得到电子的能力以及OH - 和S O 3 2 - 失去电子的能力,显然产物应该分别为氢气和硫酸根离子。方程式为: Na 2 SO 3 + H 2 O = Na 2 SO 4 + H 2...
 [课题与实验k] 铁钉在水面与空气接触处腐蚀最严重吗? 作者:黄晓东 来源:未知 日期:2021-03-10 15:13:34 点击:1333 所属专题:铁钉锈蚀
[课题与实验k] 铁钉在水面与空气接触处腐蚀最严重吗? 作者:黄晓东 来源:未知 日期:2021-03-10 15:13:34 点击:1333 所属专题:铁钉锈蚀
...
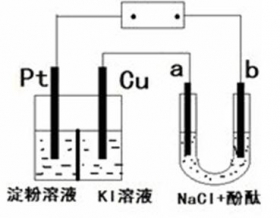 [课题与实验k] 变化多端的铜阳极 作者:吴文中 来源: 日期:2021-12-21 14:06:57 点击:1445 所属专题:电解氯化铜
[课题与实验k] 变化多端的铜阳极 作者:吴文中 来源: 日期:2021-12-21 14:06:57 点击:1445 所属专题:电解氯化铜
【基本资料】 半反应 电极电位 Cu + + e - = Cu φ=0.52 Cu 2+ + 2 e - = Cu φ=0.337 CuI + e - = Cu+I- φ=-0.1852 I 3 - + 2 e - = 3I - φ=0.545 Cu 2+ +Cl - +e - = CuCl 0.559 Cu 2+ +2CN - +e - =Cu(CN) 2 1.12 Cu(NH 3 ) 4 2+ +e - =Cu(NH...
 [课题与实验k] 电解水颜色变化的“秘密” 作者:袁建标 来源:未知 日期:2017-04-15 11:33:39 点击:5706 所属专题:电解原理应用 水的电解
[课题与实验k] 电解水颜色变化的“秘密” 作者:袁建标 来源:未知 日期:2017-04-15 11:33:39 点击:5706 所属专题:电解原理应用 水的电解
最近,市场上出现了一种净水装置。为了能够说明水中确实含 有一些杂质,销售人员还在现场以 矿泉水、纯净水以及自来水为实验 对象用水电解器来做电解水的实 验。只见销售人员打开开关几秒钟,水中便出现了红色的絮状物 质,还有的出现绿色絮状物质。这时他们解释说,水...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
为什么取Fe电极区溶液少量于试管内,再加入铁氰化钾? 铁氰化...
常见的氯化钾琼脂块盐桥制作方法有三种: 一、用于全固态硝酸...
理论上,在 Cu-Zn 单液原电池中,溶液中的 H + 在 Cu 电极表面...
从电解CuCl 2 溶液的过程来分析,无论是CuCl 2 的浓溶液,还是稀...
...
电解过程中伴随着电能转化为化学能,同时也会产生热能,温度...
一.电解Na 2 SO 3 溶液 【分析】溶液中存在的离子有H + 、OH -...
在原电池中,理论上,是在负极上发生氧化反应,在正极上发生...