
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
类型1 实验基本操作类
1.浓硫酸稀释操作
【规范操作】 将浓硫酸沿烧杯壁缓慢地倒入盛有水的烧杯里,用玻璃棒不断搅拌。
【答题关键】①浓硫酸倒入水中;②缓慢;③不断搅拌。
2.分液操作
【规范操作】 将分液漏斗上口的玻璃塞打开或使塞上的凹槽(或小孔)对准漏斗上的小孔,再将分液漏斗下面的活塞打开,使下层液体慢慢沿烧杯壁流下,当下层液体恰好流尽时,迅速关闭活塞。上层液体从分液漏斗上口倒出。
【答题关键】①液面上方与大气相通;②沿烧杯壁;③上上下下(上层液体从上口倒出;下层液体从下口放出)。
3.焰色反应操作
【规范操作】

【答题关键】①烧、蘸、烧、洗、烧;②观察钾元素焰色反应时,应透过蓝色钴玻璃观察。
4.容量瓶查漏操作
【规范操作】 向容量瓶中加适量水,塞紧瓶塞,用手指顶住瓶塞,倒立,用吸水纸检查是否有水珠渗出;如果不漏,再把塞子旋转180°,塞紧,倒置,用同样方法检查。
【答题关键】①装水;②倒立;③检查是否漏水;④旋转180°;⑤重复操作。
5.沉淀剂是否过量操作
【规范操作】(1)加沉淀剂:静置,向上层清液中继续滴加少量沉淀剂,若无沉淀产生,则证明沉淀剂已过量,否则沉淀剂不过量。
(2)加入与沉淀剂反应的试剂:静置,取适量上层清液于另一洁净试管中,向其中加入少量与沉淀剂作用产生沉淀的试剂,若产生沉淀,证明沉淀剂已过量,否则沉淀剂不过量。
【答题关键】①上层清液;②沉淀剂或与沉淀剂;③是否沉淀;④若需称量沉淀的质量而进行有关定量计算时则只能选用方法(1)。
6.沉淀洗涤操作
【规范操作】 向漏斗内加蒸馏水至浸没沉淀,待水自然流出后,重复操作2~3次。
【答题关键】①浸没;②重复2~3次。
7.判断沉淀是否洗净操作
【答题模板】 取少量最后一次洗涤液置于试管中,滴加……(试剂),若没有……现象,证明沉淀已经洗净。
8.常见试纸的使用
【答题模板】
(1)定量试纸(如pH试纸)
取一小片×××试纸放在表面皿(或玻璃片)上,用玻璃棒蘸取少量待测液,点在×××试纸上,待试纸变色后再与标准比色卡对照,得出测量数据。
(2)定性试纸(如红色石蕊试纸、蓝色石蕊试纸、淀粉KI试纸等)
①检验溶液:
将×××试纸放在表面皿(或玻璃片)上,用洁净的玻璃棒蘸取少量待测液点在试纸的中部,试纸由×××色变为×××色,即证明×××溶液具有×××性质。
②检验气体:
取一小片×××试纸用蒸馏水润湿,粘在玻璃棒的一端,靠近盛有待测气体的容器口(如试管的管口)附近,试纸由×××色变为×××色,即证明该气体是×××。
9.气密性检验
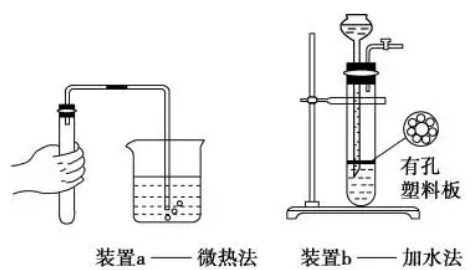
【规范操作】(1)装置a:连接导管,将导管插入水中,捂热(或加热)试管,导管口有气泡产生;停止加热,导管内有水上升并形成一段稳定的水柱。
(2)装置b:关闭活塞,从长颈漏斗注入蒸馏水,至浸没漏斗口,继续加水使漏斗中液面高于试管中的液面,静置观察液面是否变化。
【答题关键】(1)①密闭;②加热;③气泡;④水柱。
(2)①关闭活塞;②注水;③液柱。
【答题模板】 形成密闭体系―→操作―→描述现象―→得出结论。
10.滴定管检查是否漏水操作
【规范操作】(1)酸式滴定管:关闭活塞,向滴定管中加入适量水,用滴定管夹将滴定管固定在铁架台上,观察是否漏水,若2分钟内不漏水,将活塞旋转180°,重复上述操作。
(2)碱式滴定管:向滴定管中加入适量水,用滴定管夹将滴定管固定在铁架台上,观察是否漏水,若2分钟内不漏水,轻轻挤压玻璃球,放出少量液体,再次观察滴定管是否漏水。
【答题关键】①固定;②观察;③旋转活塞或挤压玻璃球。
11.滴定管排气泡操作
【规范操作】(1)酸式滴定管:右手将滴定管倾斜30°左右,左手迅速打开活塞使溶液冲出,从而使溶液充满尖嘴。
(2)碱式滴定管:将胶管弯曲使玻璃尖嘴向上倾斜,用两指捏住胶管,轻轻挤压玻璃球,使溶液从尖嘴流出,即可排出碱式滴定管中的气泡。
【答题关键】(1)①倾斜30°;②使溶液迅速流出。
(2)①胶管弯曲向上;②挤压玻璃球。
12.气体验满和验纯操作
【规范操作】
(1)氧气验满:用带火星的木条平放在集气瓶口,木条复燃,说明收集的氧气已满。
(2)可燃性气体(如氢气)的验纯方法:用排水法收集一小试管的气体,用大拇指摁住管口移近火焰,放开手指,若听到尖锐的爆鸣声,则气体不纯;若听到轻微的“噗”的一声,则气体纯净。
(3)二氧化碳验满:将燃着的木条平放在集气瓶口,若火焰熄灭,则气体已满。
(4)氨气验满:用湿润的红色石蕊试纸放在集气瓶口,若试纸变蓝说明气体已满。
(5)氯气验满:用湿润的淀粉碘化钾试纸放在集气瓶口,若试纸变蓝说明气体已满。
【答题模板】用……放在集气瓶口,若……(现象),说明……(“气体已满”或“是……气体”)。
类型2 检验、鉴别类
(1)结晶析出Na2S2O3·5H2O,其中可能含有Na2SO3、Na2SO4等杂质。利用所给试剂设计实验,检测产品中是否存在Na2SO4,简要说明实验操作、现象和结论:____________。
已知Na2S2O3·5H2O遇酸易分解:S2O32-+2H+===S↓+SO2↑+H2O
供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液
(2)榴石矿石可以看作CaO、FeO、Fe2O3、Al2O3、SiO2组成。试设计实验证明榴石矿中含有FeO(试剂任选,说明实验操作与现象)____________。
(3)鉴别SO2和CO2:___________________________。
【规范答案】(1)取少量产品溶于足量稀盐酸,静置,取上层溶液(或过滤,取滤液)于一试管中,滴加BaCl2溶液,若产生白色沉淀,说明含有Na2SO4杂质
(2)取矿石少许,加稀硫酸充分反应后,向其中滴加酸性高锰酸钾溶液,若紫色褪去,证明矿石中含有FeO(不能加盐酸溶解)
(3)法1:取适量品红溶液于两洁净的试管中,分别通入两气体,能使品红溶液褪色的是SO2气体,不能使品红溶液褪色的是CO2
法2:取适量酸性高锰酸钾溶液分别于两洁净的试管中,分别通入两气体,能使酸性高锰酸钾溶液的紫红色褪去的是SO2气体,不能使酸性高锰酸钾溶液褪色的是CO2
【答题模板】
1.离子检验的一般模式为

2.鉴别的一般模式为
(1)固体鉴别一般模式为:
①分别取固体分置于两支试管中加热或加入……试剂,现象是……的是……物质。
②分别取固体分置于两支试管中溶于水形成溶液,加……试剂,现象是……的是……物质。
(2)溶液鉴别一般模式为:
①分别取两溶液分置于两支试管中,分别加入……试剂,现象是……的是……物质。
②分别取两溶液分置于两支试管中,分别加入……试剂,现象是……继续加入……试剂,现象是……的是……物质。
(3)气体鉴别一般模式为:
取适量……溶液于两支洁净试管中,分别通入两种气体,能使……(试剂)……(现象)的是……气体,不能使……(试剂)……(现象)的是……气体。
类型3 原因描述类
【答题模板】“有理”——化学原理,“有据”——事实依据。
可采取以下两种方式:
(1)“正说”——“直接原因+根本目的”
(2)“反说”——“如果……,就……”
类型4 平衡理论描述类
【答题策略】
理论型简答题一般是演绎法的三段式答题模式(前提、推理、结论):(1)问题所涉及大前提(相关的理论或规律)的表述,一般很熟悉的理论或规律可以只写名称,也可以用化学方程式等化学用语表示,并不需要把其详细内容写出;(2)问题的推理过程(具体条件下的变化等)的表述;(3)问题所涉及的变化的结果。
(1)利用浓氨水和氢氧化钠作用可以制备NH3,用化学平衡原理分析NaOH的作用_______________________。
(2)常温下,如果向AlCl3饱和溶液中不断通入HCl气体,可析出ALCl3·6H2O晶体,结合化学平衡移动原理解释析出晶体的原因___________。
(3)惰性电极电解饱和NaCl溶液时,阴极附近的pH增大,结合平衡移动原理解释原因___________。
【规范答案】
(1) 浓氨水中存在平衡:NH3+H2O NH3 • H2O
NH3 • H2O  NH4++OH-, NaOH 溶于氨水放c(OH-)增大,使上述平衡向左移动,可生成NH3
NH4++OH-, NaOH 溶于氨水放c(OH-)增大,使上述平衡向左移动,可生成NH3
(2)AlCl3饱和溶液中存在溶解平衡:AlCl3 • 6H2O(s)  Al3+(aq) + 3Cl- (aq) + 6H2O(1),通入 HCl 气体,溶液c(Cl-)增大,平衡向左移动,析出AlCl3• 6H2O晶体
Al3+(aq) + 3Cl- (aq) + 6H2O(1),通入 HCl 气体,溶液c(Cl-)增大,平衡向左移动,析出AlCl3• 6H2O晶体
(3)溶液中存在平衡H2O H++OH-,电解时,阴极附近的H+放c(H+) 减小,平衡右c(OH-)増大,故pH增大
H++OH-,电解时,阴极附近的H+放c(H+) 减小,平衡右c(OH-)増大,故pH增大
【答题模板】
(1)……存在……平衡……(条件)使平衡向……(方向)移动,……(结论)
(2)对于……(反应特点),……(条件)使平衡向……(方向)移动
五. 实验现象描述类
1.实验现象答题模板三角度
(1)有关溶液的现象描述(五大类)
①颜色由……变成……;
②液面上升或下降(形成液面差);
③溶液变浑浊或生成(产生)……(颜色)沉淀;
④溶液发生倒吸;
⑤产生大量气泡(或有气体从溶液中逸出)等。
(2)有关固体物质的现象描述(四大类)
①……(固体)表面产生大量气泡;
②……(固体)逐渐溶解;
③……(固体)体积逐渐变小(变细);
④……(固体)颜色由……变成……。
(3)有关气体的现象描述(三大类)
①生成……色(味)气体;
②气体由……色变成……色;
③气体先变……后……(加深、变浅、褪色等)。
2.现象描述时的注意事项
(1)现象描述要全面:看到的、听到的、摸到的、闻到的。
(2)要注重对本质现象的观察:本质现象就是揭示事物本质特征的现象。如镁带在空气中燃烧时“生成白色固体”是本质现象,因为由此现象可正确理解化学变化这个概念,而发出“耀眼的白光”则是非本质现象。因此,观察实验现象要有明确的观察目的和主要的观察对象。
(3)现象描述要准确:
①不能以结论代替现象。如铁丝在氧气中燃烧的实验现象是“火星四射,放出大量的热,生成黑色固体”,而不能用结论“生成四氧化三铁”代替“生成黑色固体”。
②要明确“光”和“火焰”、“烟”和“雾”等概念的区别,不能相互代替。
类型6 实验装置中仪器或试剂的作用类
【答题模板】 装置中仪器和试剂的用途回答时一般包括直接作用和根本目的两部分内容,根据各部分装置的用途不同,可采用下列格式回答:

类型7 滴定终点现象类
【答题模板】
当滴入最后一滴×××标准溶液后,溶液由×××色变成×××色,或溶液×××色褪去,且半分钟内不变色。
【答题关键】


 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
1、对浸润液态石蜡油的碎瓷片加强热,将产生的气体通入酸性...
装置 装置的易错点或注意事项 (1)容量瓶中是否有固体,不能在...
知识要点 1.表格实验分析的“三个角度” (1)可行性。实验原理是...
一:水蒸气蒸馏 系指将含有挥发性成分的植物材料与水共蒸馏,...
...
1. 【实验 1-1 】胶体制备 实验原理: 实验步骤: 将饱和 FeCl 3...