
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
1.从铝土矿中提炼铝
流程Ⅰ
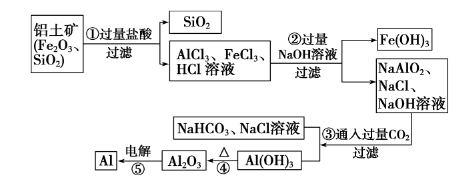
(1)涉及反应(写出并配平化学方程式)
①Al2O3+HCl=2AlCl3+3H2O
Fe2O3+HCl=2FeCl3+3H2O
②AlCl3+NaOH=NaAlO2+3NaCl+2H2O
FeCl3+NaOH=Fe(OH)3↓+3NaCl
HCl+NaOH=NaCl+H2O
③NaAlO2+H2O+CO2=Al(OH)3↓+NaHCO3
NaOH+CO2=NaHCO3
④Al(OH)3 Al2O3+3H2O
Al2O3+3H2O
⑤Al2O3(熔融) 4Al+3O2↑
4Al+3O2↑
(2)问题探讨(思考并回答问题)
①步骤①加入过量盐酸后的实验操作是什么?
提示:过滤。
②步骤②能否用氨水代替NaOH溶液?
提示:不能;原因是Al3+与过量氨水反应生成Al(OH)3沉淀,达不到分离Al3+、Fe3+的目的。
③步骤③中若将CO2的量改为“少量”,得到的产物还是NaHCO3吗?
提示:不是NaHCO3而是Na2CO3。
流程Ⅱ
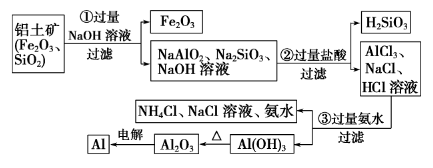
(1)涉及反应
①Al2O3+NaOH=2NaAlO2+H2O
SiO2+NaOH=Na2SiO3+H2O
②Na2SiO3+HCl=H2SiO3↓+2NaCl
NaAlO2+HCl=NaCl+AlCl3+2H2O
NaOH+HCl=NaCl+H2O
③AlCl3+NH3·H2O=Al(OH)3↓+NH4Cl
HCl+NH3·H2O=NH4Cl+H2O
(2)问题探讨
①步骤②中将盐酸改为“CO2”合适吗?为什么?
提示:不合适;因为过量CO2与NaAlO2、Na2SiO3反应生成Al(OH)3和H2SiO3沉淀,达不到分离SiO2和AlO2-的目的。
②步骤③中将氨水改为“NaOH溶液”合适吗?
提示:不合适;因为Al(OH)3能溶于NaOH。
③冶炼金属铝能否用氯化铝代替氧化铝?
提示:不能;因为AlCl3属于共价化合物。
2.硅的制备
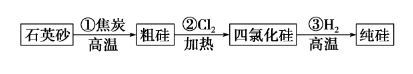
(1)涉及反应
①SiO2+C Si+CO↑
Si+CO↑
②Si+Cl2 SiCl4
SiCl4
③SiCl4+H2 Si+4HCl
Si+4HCl
(2)问题探讨
①步骤①中石英砂与焦炭高温下反应时为什么要隔绝空气?
提示:高温下,焦炭和空气中的O2发生反应。
②用石英砂和焦炭制备粗硅的反应中,焦炭的作用是什么?
提示:提供能量,作还原剂。
③粗硅与HCl完全反应后,经冷凝得到的SiCl4(沸点57.6 ℃)中混有少量的SiHCl3(沸点33 ℃),提纯SiCl4采用的方法是什么?
提示:蒸馏。
④由SiO2与C高温下反应得到的粗硅中可能含有什么杂质?
提示:SiO2、C、SiC等。
3.氯碱工业
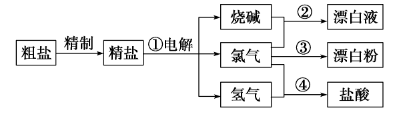
(1)涉及反应
①2NaCl+H2O 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
②Cl2+NaOH=NaCl+NaClO+H2O
③Cl2+Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
④H2+Cl2 2HCl
2HCl
(2)问题探讨
①食盐中含有Ca2+、Mg2+、SO42-等杂质离子,如何设计实验方案除去这些杂质离子?
②工业上电解食盐水制烧碱时,食盐水为什么必须要精制?
提示:精制食盐水的目的是除去食盐水中的Ca2+、Mg2+、SO42-等杂质离子,以防Mg2+与OH-结合生成Mg(OH)2堵塞隔膜电解槽中的隔膜,造成电解失败。
③用惰性电极电解饱和食盐水时,为什么要用隔膜把电解槽分成阳极室、阴极室?
提示:电解时,阳极产生Cl2,阴极产生H2,若无隔膜,二者混合光照时会发生爆炸,隔膜的作用是将H2和Cl2隔开,以防发生危险。
④步骤③制取漂白粉时是将Cl2通入澄清石灰水中吗?
提示:不是;原因是澄清石灰水中Ca(OH)2的含量低,不适合工业大量生产,应改为石灰乳。
4.工业上利用黄铁矿(FeS2)制取硫酸
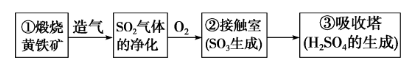
(1)涉及反应
①FeS2+O2 Fe2O3+SO2
Fe2O3+SO2
②SO2+O2 SO3
SO3
③SO3+H2O=H2SO4
(2)问题探讨
①煅烧黄铁矿要在沸腾炉中进行,其中矿石要粉碎,从炉底鼓入空气,炉中的粉末状固体就像沸腾的液体一样,煅烧时为什么要将矿石粉碎成粉末状?
提示:增大矿石和氧气的接触面积,提高燃烧效率。
②在接触室中通入过量的氧气,能否将SO2全部转化成SO3?
提示:不能;原因是SO2催化氧化成SO3的反应是可逆反应。
③依据化学反应速率和化学平衡原理,增大压强对SO2催化氧化成SO3的反应是十分有利的,而工业生产上为什么不采用高压而采用常压下进行反应?
提示:常压下,SO2催化氧化成SO3的转化率已经很高,增大压强,即增加了设备的投资,得不偿失。
④吸收塔中发生的是SO3与水的反应,为什么吸收SO3气体时用98%的浓硫酸而不用水吸收?
提示:用水吸收SO3易形成硫酸的酸雾,影响吸收效率。
⑤硫酸工厂的尾气中含有大量的SO2,写出用氨水吸收SO2的化学方程式。
提示:SO2+NH3·H2O=NH4HSO3,2NH3·H2O+SO2=(NH4)2SO3+H2O。
5.工业制硝酸
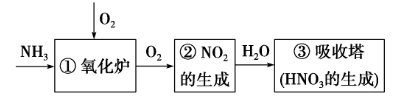
(1)涉及反应
①NH3+O2 NO+H2O
NO+H2O
②NO+O2=NO2
③NO2+H2O=HNO3+NO
(2)问题探讨
①步骤③吸收塔中为什么NO2被水吸收过程中要补充一定量的空气?
提示:因NO2与水反应生成HNO3时只有的NO2转化成HNO3,通入空气的目的是使NO2与O2作用完全转化成HNO3,方程式为4NO2+O2+2H2O=4HNO3。
②工业制硝酸时,能否将工业尾气直接排入大气中?
工业尾气中有害气体的主要成分是什么?
提示:不能;NO和NO2。
③已知:①NO+NO2+2NaOH=2NaNO2+H2O
②2NO2+2NaOH=NaNO2+NaNO3+H2O
硝酸工厂的尾气可用NOx(NO与NO2的混合气体)表示,用NaOH溶液可吸收尾气,为使NOx完全被NaOH溶液吸收x的取值范围是什么?如何操作才能保证NOx完全被NaOH溶液吸收?
提示:1.5≤x<2;通入一定量的空气(或O2)后,再被NaOH溶液吸收。
6.工业上制纯碱
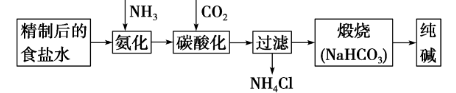
(1)涉及反应
NH3+H2O+CO2+NaCl=NaHCO3↓+NH4Cl
2NaHCO3 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
(2)问题探讨
①工业制纯碱时为什么先通入NH3后通入CO2?
提示:NH3在水中的溶解度大,形成的NH3·H2O呈碱性,更容易吸收CO2,得到更多的NaHCO3;若先通入CO2,得到的HCO浓度小,不利于NaHCO3的生成。
②工业上制备的纯碱中可能混有哪些杂质?
提示:依据制备反应:NH3+H2O+CO2+NaCl=NaHCO3↓+NH4Cl可知混有的杂质为NACl和NH4Cl。
③“碳酸化”后过滤获得的物质是什么?
提示:NaHCO3。
④过滤得到的母液为NH4Cl,加入熟石灰获得循环使用的物质是什么?
提示:NH3。
⑤设计实验证明纯碱产品中混有NaCl?
提示:取少量样品于一试管中,加水配成溶液,加入足量硝酸酸化的AgNO3溶液,若有白色沉淀生成说明纯碱样品中混有NaCl。
7.从工业废水中回收硫酸亚铁和铜的工艺流程
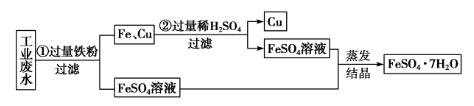
工业废水中含有大量的FeSO4,较多的Cu2+和少量的Na+。为了减少污染并变废为宝,回收硫酸亚铁和金属铜的工艺流程如下。
(1)涉及反应
①CuSO4+Fe=FeSO4+Cu
②Fe+H2SO4=FeSO4+H2↑
(2)问题探讨
①步骤②中加入过量稀H2SO4的目的是什么?
提示:除去Cu中残留的铁。
②步骤①中如何将Fe、Cu与FeSO4溶液分离?
提示:过滤。
③步骤③中如何从FeSO4溶液中获得硫酸亚铁晶体?
提示:将FeSO4溶液加热浓缩、冷却结晶,过滤得FeSO4·7H2O。
8.从海水中提取镁
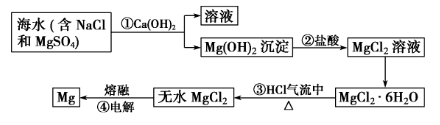
(1)涉及反应
①MgSO4+Ca(OH)2=Mg(OH)2↓+CaSO4
②Mg(OH)2+2HCl=MgCl2+2H2O
③MgCl2·6H2OHCl 气流中Δ MgCl2+6H2O
④MgCl2(熔融) Mg+Cl2↑
Mg+Cl2↑
(2)问题探讨
①步骤③中加热MgCl2·6H2O制取无水MgCl2时,为什么要在HCl的气流中进行?
提示:防止MgCl2水解。
②从海水中提取镁的工艺流程中,涉及哪些反应类型?
提示:分解反应、复分解反应、氧化还原反应。
③步骤④用电解法冶炼镁时,能否用MgO代替MgCl2?
提示:不能;原因是MgO的熔点高,浪费能源。
9.从海水中提取溴
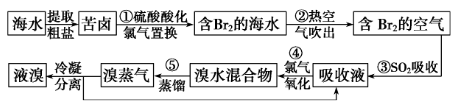
(1)涉及反应
①2Br-+Cl2=Br2+2Cl-
③Br2+SO2+2H2O=H2SO4+2HBr
(2)问题探讨
①从海水中提取溴的工艺流程中为什么要设计两步(步骤①、④)将Br-氧化,Br2的过程?
提示:将溴富集。
②步骤⑤蒸馏的过程中,温度应控制在80~90℃,温度过高或过低都不利于生产,请解释原因。
提示:温度过高,大量水蒸气随溴排出,溴蒸气中水量增加,温度过低,溴不能完全蒸出,回收率低。
③步骤②中用热空气吹出的溴也可以用饱和Na2CO3溶液吸收溴,写出反应过程的化学方程式。
提示:Br2+H2O=HBr+HBrO,Na2CO3+2HBr=2NaBr+H2O+CO2↑。
10.海带中碘的提取
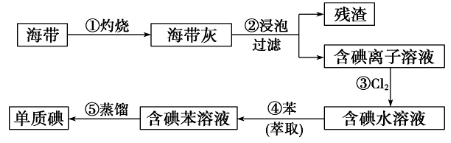
(1)涉及反应:2I-+Cl2=I2+2Cl-
(2)问题探讨
①步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是________(从下列仪器中选出所需的仪器,将标号字母填写在空白处)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
提示:B、D、E
②步骤⑤的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是什么?
提示:蒸馏。
③步骤④中,某同学选择苯来提取碘的理由是什么?
提示:苯与水互不相溶,碘在苯中的溶解度比在水中的大,苯与水溶液易分层。
④设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法。
提示:取少量提取碘后的水溶液于试管中,加入几滴淀粉溶液,若溶液变蓝,说明还有单质碘;若溶液不变蓝,说明溶液不含碘。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
钴、镍都是中等活泼的金属元素,化合物性质比较接近,但也存...
每次做化学大题,最让人又爱又恨的,绝对是化工流程题。 爱它...
一、硼及其常考化合物的性质简介 1.硼单质 硼(B)的化学性质与...
在高中化学大题中,工艺流程题堪称“分值大户”,同时也是很...
化工流程里的条件控制,根本不是什么玄学难点,更不是要你死...
一、需要温度计的实验 测反应混合溶液的温度 1.测溶解度 2.由乙...