
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、比较[H+]与[OH-]的大小
![]() H++CO32-
H++CO32-
![]() H2CO3+OH-
H2CO3+OH-
二、比较[CO32-]与[OH-]的大小
![]() H++HCO3-
H++HCO3-
![]() H++CO32-
H++CO32-
以上两式相减得:
将以上三式代入③式,得:
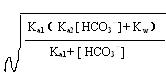
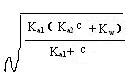
当Ka2c>20Kw时,⑤中的Kw可忽略,得:
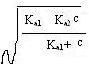
当c>20
Ka1时,⑤中的
Ka1+c≈c,得:
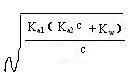
当Ka2c>20Kw和c>20 Ka1时,⑥⑦均可进一步化简,得:
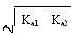
利用上式可以计算出NaHCO3溶液中的

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
莫尔法和佛尔哈德法是分析化学中沉淀滴定法的两种经典方法,...
...
所谓缓冲溶液,是指能维持溶液的酸度,使溶液的pH不因外加少...
...
什么是PH?PH是拉丁文“Pondushydrogenii”一词的缩写(Pondus=压强、压...
一、水的离子积计算 水的离子积( K w )是一个使用频率较高的化...