
|
学习小专题 |
 为什么酸性:硫醇>醇?
日期:2025-09-12 16:10:03
点击:1356
好评:0
为什么酸性:硫醇>醇?
日期:2025-09-12 16:10:03
点击:1356
好评:0
为什么硫醇和硫酚酸性大于相对应的醇和酚,主要有以下两个原因: 硫醇和硫酚中的硫,和醇酚的氧杂化方式一样,都是sp 3 杂化,两对孤对电子分别占据一个sp 3 杂化轨道,剩下的两个sp 3 分别与碳和氢形成σ键。 硫的sp 3 轨道比较扩散,体积比较大。与氢形成σ键时,氢的...
 如何判断强酸弱酸中强酸?
日期:2025-03-18 09:34:49
点击:1157
好评:0
如何判断强酸弱酸中强酸?
日期:2025-03-18 09:34:49
点击:1157
好评:0
鲍林在研究含氧酸时,将其化学式一般写作 HRO,其中 R 代表中心原子,羟基(–OH)与非羟基氧原子共存。鲍林发现,含氧酸的酸性主要取决于分子中非羟基氧原子(n)的数量。当 n 增加时,R 原子的氧化态提高,其电负性增强,从而对羟基氧起到较强的电子拉吸作用,使 O–H...
 常见的酸性强弱顺序
日期:2024-07-15 10:33:12
点击:5643
好评:0
常见的酸性强弱顺序
日期:2024-07-15 10:33:12
点击:5643
好评:0
1.常见的弱酸的酸性强弱顺序 CHCHOHCOOH(乳酸)CHCOOH(苯甲酸)CH=CHCOOH(丙烯 酸)CHCOOH(醋酸)CHCOOH(丙酸)HCO(碳酸)HS(氢硫 酸)HClO(次氯酸)HBO(硼酸) HSiO(偏硅酸)CHOH(苯酚) 2.常见的强酸的酸性强弱顺序 HClO(高氯酸)HI(氢碘酸)HBr(氢溴酸)HCl(盐酸)HSO(硫酸)HNO(硝酸...
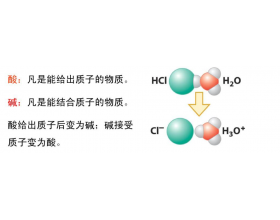 拉平效应和区分效应
日期:2024-01-16 08:29:58
点击:1043
好评:0
拉平效应和区分效应
日期:2024-01-16 08:29:58
点击:1043
好评:0
HCI、HI、HNO 3 、HClO 4 等强酸在水中“完全电离”,因而它们同浓度水溶液的pH相同,这意味着它们酸的强度是相同的。然而,这些强酸结构中与可电离氢原子结合的化学键并不相同,为什么电离能力相同呢? 我们不能忘记,酸在水中电离出氢离子是与水分子作用的结果: 强酸在...
 为什么强酸在冰醋酸中可以比较出其酸性强弱?
日期:2024-01-16 08:00:01
点击:987
好评:0
为什么强酸在冰醋酸中可以比较出其酸性强弱?
日期:2024-01-16 08:00:01
点击:987
好评:0
问:为什么强酸在冰醋酸中可以比较出其酸性强弱? 想要回答这个问题,还是得回到酸电离的机理上。涉及到溶剂的区分和 拉平效应 。 以在水溶液中的弱酸醋酸为例: CH 3 COOH+H 2 O CH 3 COO - +H 3 O + 醋酸分子在水中发生电离的时候,其实是醋酸分子和水分子之间发生反...
 常见弱酸酸性强弱顺序
日期:2022-07-30 18:42:45
点击:12264
好评:0
常见弱酸酸性强弱顺序
日期:2022-07-30 18:42:45
点击:12264
好评:0
中学化学常见弱酸有:H 2 SiO 3 (偏硅酸)、 n (氢氰酸)、H 2 CO 3 (碳酸)、HF(氢氟酸,较少见)、CH 3 COOH(也作C 2 H 4 O 2 乙酸,又叫醋酸)、H 2 S(氢硫酸)、HClO(次氯酸)、HNO 2 (亚硝酸,较少见)、中学范围内的所有的有机酸(中学不学习有机强酸)、HNC(雷酸)等。没有特殊...
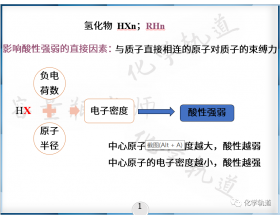 非金属氢化物的酸性变化规律
日期:2022-03-25 10:24:48
点击:1805
好评:0
非金属氢化物的酸性变化规律
日期:2022-03-25 10:24:48
点击:1805
好评:0
以酸碱电离理论的角度看,大多数非金属氢化物溶于水并且显酸性,例如 HCl ,也有显碱性的,例如 NH 3 ,但是像 CH 4 不溶于水, SiH 4 水解。 放 宽眼界 ,以酸碱质子理论的角度不再局限于水溶液中,能解离出质子的都是酸,所以非金属氢化物都可以看做是酸,强弱不同的...
 常见酸的酸性强弱
日期:2020-04-08 22:23:22
点击:14401
好评:0
常见酸的酸性强弱
日期:2020-04-08 22:23:22
点击:14401
好评:0
HClO 4 >HI>HBr>HCl>HNO 3 >H 2 SeO 4 >H 2 SO 4 >HClO 3 (以上为强酸)>H 2 C 2 O 4 (草酸)>H 2 SO 3 >H 3 PO 4 >CH 3 COCOOH(丙酮酸)>HNO 2 >HF>HCOOH>(以上为中强酸)C 3 H 6 O 3 (乳酸)>C 6 H 5 COOH(苯甲酸)>CH 2 =CH-COOH(丙烯酸)>CH 3 COOH>C ...
 一百个定性的比较总结文档
日期:2018-04-13 10:33:21
点击:385
好评:0
一百个定性的比较总结文档
日期:2018-04-13 10:33:21
点击:385
好评:0
一百个定性的比较总结文档...
 氧化性酸全面解读
日期:2018-03-14 11:44:14
点击:5897
好评:0
氧化性酸全面解读
日期:2018-03-14 11:44:14
点击:5897
好评:0
无机含氧酸可以的分子式为HmROn,其通式可以写成Hl-Rm-(OH)n,〔其中l,m可以为0,n≥0〕,也可写成ROm-n(OH)n,其中R称为成酸元素,无机含氧酸在水溶液中的酸强度取决于酸分子中羟基-O-H的电离程度,也可以用Pka值来衡量。酸分子羟基中的质子在电离过程中脱离氧原子,转...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。