
|
学习小专题 |
 水的电离和溶液的酸碱性之思维导图
日期:2019-07-30 08:24:43
点击:6270
好评:0
水的电离和溶液的酸碱性之思维导图
日期:2019-07-30 08:24:43
点击:6270
好评:0
...
 关于水电离的问题集
日期:2016-02-02 22:20:40
点击:17833
好评:0
关于水电离的问题集
日期:2016-02-02 22:20:40
点击:17833
好评:0
水是一种极弱的电解质,在常温下能电离出极少量的H + 和OH - ,存在着电离平衡, 在解答有关水电离的问题时,要掌握以下的知识和规律。 1. K w = c (H + ) c (OH - )。由于水中 c (H + )= c (OH - ),纯水总是中性的。 2. 不能认为 c (H + )或 c (OH - )等于10 -7 m...
在课堂上分析影响水的电离平衡的因素时,学生一般对于升温、加酸、加碱、加可水解的盐对水的电离平衡的影响很容易理解掌握。而当我问到加入易与水反应的物质,如 Na 、 F 2 、 CO 2 、 NH 3 等,对水的电离平衡的影响如何呢?思考一会儿之后,有的学生不作声,有的学生...
 “水的电离”题型归类
日期:2016-02-02 21:08:20
点击:10612
好评:0
“水的电离”题型归类
日期:2016-02-02 21:08:20
点击:10612
好评:0
一、酸、碱溶液中由水电离产生的[H + ] 水 、[OH - ] 水 的计算 1.酸溶液中,[H + ] 水 =[OH - ] 水 =[OH - ]=K w /[H + ] (1) 2.碱溶液中,[H + ] 水 =[OH - ] 水 =[H + ]=K w /[OH - ] (2) (1)(2)两式中[H + ]、[OH - ]表示该溶液中H + 、OH - 的总物质的量...
 水的电离方程式所蕴含的几组关系
日期:2016-02-02 20:07:49
点击:6270
好评:25
水的电离方程式所蕴含的几组关系
日期:2016-02-02 20:07:49
点击:6270
好评:25
水是一种极弱的电解质,能够发生微弱的电离,存在着电离平衡。在一定温度下,[H + ]与[OH - ]的乘积是一个常数,即[H + ][OH - ]=KW,KW叫做水的离子积常数,简称水的离子积。 通过水的电离方程式,可以发现它蕴含了如下几组关系,在我们教学和学习中,都至关重要。现...
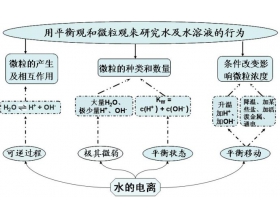 水的电离知识网络图
日期:2016-01-18 18:07:23
点击:3597
好评:0
水的电离知识网络图
日期:2016-01-18 18:07:23
点击:3597
好评:0
...
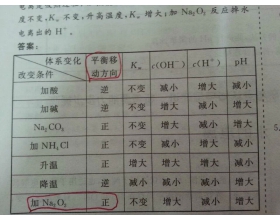 过氧化钠为什么对水的电离促进?
日期:2015-01-28 09:10:32
点击:2083
好评:0
过氧化钠为什么对水的电离促进?
日期:2015-01-28 09:10:32
点击:2083
好评:0
能消耗水中的氢离子或是氢氧根离子的反应都可以促进。过氧化钠其实是双氧水的正盐。而双氧水是弱酸。所以在本质上过氧化钠是强碱弱酸盐。要水解。水解在本质上就是促进水的电离。...
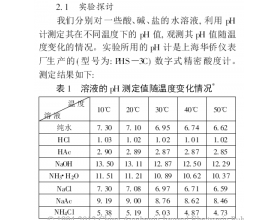 温度越高,酸的pH越小,碱的pH越大吗?
日期:2015-01-27 17:27:54
点击:2356
好评:0
温度越高,酸的pH越小,碱的pH越大吗?
日期:2015-01-27 17:27:54
点击:2356
好评:0
温度越高,酸的pH越小,碱的pH越大吗?很显然从图表得知不一定,因为不能单纯考虑酸碱盐的变化情况,还有考虑到水的电离情况的变化。...
 用简单的实验说明水能发生微弱的电离
日期:2014-07-20 15:47:45
点击:1204
好评:0
用简单的实验说明水能发生微弱的电离
日期:2014-07-20 15:47:45
点击:1204
好评:0
前不久,有机会听了福州一中陈曦老师给高二学生讲“水的电离”。陈老师利用学生熟悉的饮用瓶装矿泉水、纯净水和万用表,引导学生观察演示实验,通过师生互动讨论,深入浅出地让学生认识了水的电离特点,建立了“水是极弱电解质”和“水的离子积”的概念。 陈老师首先配合关...
 纯水的电离度是多大?
日期:2012-05-15 18:26:17
点击:7772
好评:0
纯水的电离度是多大?
日期:2012-05-15 18:26:17
点击:7772
好评:0
生活中,我们一般会认为纯水是不导电的。但根据精确的实验证明,水是一种极弱的电解质,它能微弱地电离,生成水合氢离子和氢氧根离子。其电离方程式可表示为: H 2 O+H 2 O H 3 O + +OH - 可简写为:H 2 O H + +OH - ,从纯水的导电实验测得,在25℃(常温)时,纯水中H + 和...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。