
|
学习小专题 |
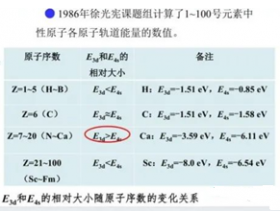 3d、4s轨道的能量谁更高?
日期:2024-04-07 07:49:26
点击:1895
好评:1
3d、4s轨道的能量谁更高?
日期:2024-04-07 07:49:26
点击:1895
好评:1
多电子原子中,在考虑某个电子时,可以把其他电子对其排斥作用看作削弱了原子核对它的吸引作用,这种由于其他电子的排斥而使原子核对某个电子吸引作用的减弱称为 屏蔽效应 。 电子层数越小的电子在离原子核越近的地方出现几率越大,但在同一电子层中不同轨道上的电子钻到离...
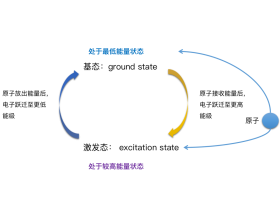 基态与激发态,构造原理与电子排布式解读
日期:2023-10-07 09:16:16
点击:2135
好评:0
基态与激发态,构造原理与电子排布式解读
日期:2023-10-07 09:16:16
点击:2135
好评:0
基态和激发态 什么是光谱? 光谱:不同元素的原子发生跃迁时会 吸收 ( 基态→激发态 )或 释放 ( 激发态→基态 )不同的光,可以用光谱仪摄取各种元素的电子的吸收光谱或发射光谱, 总称原子光谱 。 光谱分析:在现代化学中,常利用原子光谱上的 特征谱 线来 鉴定元素...
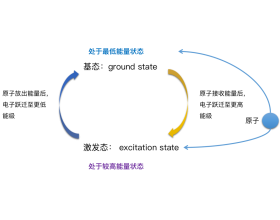 概念辨析:基态与激发态及构造原理与电子排布式
日期:2023-01-02 15:47:00
点击:3176
好评:0
概念辨析:基态与激发态及构造原理与电子排布式
日期:2023-01-02 15:47:00
点击:3176
好评:0
基态和激发态 什么是光谱? 光谱:不同元素的原子发生跃迁时会吸收(基态→激发态)或释放(激发态→基态)不同的光,可以用光谱仪摄取各种元素的电子的吸收光谱或发射光谱,总称原子光谱。 光谱分析:在现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为光谱分...
 为什么原子核外电子最外层不超过8个,次外层不超过18个?
日期:2021-12-17 09:36:05
点击:12780
好评:2
为什么原子核外电子最外层不超过8个,次外层不超过18个?
日期:2021-12-17 09:36:05
点击:12780
好评:2
原子核外的电子排布,最外层不超过8个,次外层不超过18 个,这种构型是由于电子能级发生交错而造成的。 由各亚层能量高低顺序:1s, 2s2p, 3s3p, 4s3d4f,5s4d5p, 6s4f5d6p……可知,如最外层是第四层,则在第五能层出现之前仅有4s和4p轨道可填充电子,最多也只为8个。同...
 怎样比较原子轨道中电子能量的大小?
日期:2021-08-23 18:58:27
点击:856
好评:0
怎样比较原子轨道中电子能量的大小?
日期:2021-08-23 18:58:27
点击:856
好评:0
...
 构造原理与屏蔽效应、钻穿效应的关系
日期:2021-06-15 15:54:29
点击:4487
好评:0
构造原理与屏蔽效应、钻穿效应的关系
日期:2021-06-15 15:54:29
点击:4487
好评:0
1.原子轨道能级图 多电子体系中,电子不仅受到原子核的作用,而且受到其余电子的作用,故能量关系复杂。所以,多电子体系中,电子或轨道的能量不只由主量子数n决定,也与角量子数l有关。 1)屏蔽效应 主量子数n相同,角量子数l不同的原子轨道,l越大,能量越高。 n相同l不同的...
 为什么多电子原子的电子能级产生了“能级交错”现象?
日期:2020-12-07 09:46:11
点击:4009
好评:1
为什么多电子原子的电子能级产生了“能级交错”现象?
日期:2020-12-07 09:46:11
点击:4009
好评:1
在多电子原子中,不但原子核对电子存在引力,而且还存在 电子间的相互排斥。内层电子对外层电子的排斥,相当于核电荷 对外层电子引力的减弱,这就是内层电子对外层电子的屏蔽效应。 同一电子层中屏蔽效应的大小顺序如下:nsnpndnf。 由于各电子层中的s电子对同层其他能...
 微课视频之酷学习:构造原理和电子排布式
日期:2020-03-03 14:28:16
点击:249
好评:0
微课视频之酷学习:构造原理和电子排布式
日期:2020-03-03 14:28:16
点击:249
好评:0
第1集:构造原理和电子排布式...
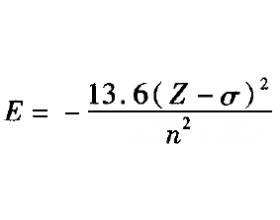 按构造原理最后填充的电子在反应中是否最先失去?
日期:2019-06-10 21:40:10
点击:1593
好评:0
按构造原理最后填充的电子在反应中是否最先失去?
日期:2019-06-10 21:40:10
点击:1593
好评:0
按构造原理最后填充的电子在反应中是否最先失去? 答:不一定。例如铜的电子排布式为1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 1 或[ Ar]3d 10 4s 1 ,电子先填入4s后再填入3d,在失去电子成为离子时却先失去4s电子。 定性分析 :原因是失去电子成为离子,核电荷数不变电子数减...
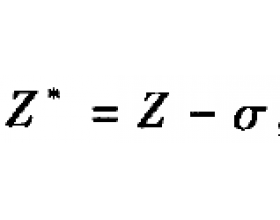 为什么有能级交错现象?
日期:2019-06-10 21:33:54
点击:4998
好评:1
为什么有能级交错现象?
日期:2019-06-10 21:33:54
点击:4998
好评:1
在多电子原子中,一个电子不仅受到原子核的引力,而且还要受到其他电子的排斥力。 这种排斥力显然要削弱原子核对该电子的吸引,可以认为排斥作用部分抵消或屏蔽了核电荷对该电子的作用,相当于使该电子受到的有效核电荷数减少了。 于是有 ,式中 为有效核电荷,z为核电荷,...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。