
|
学习小专题 |
 疑难杂症之化学反应的方向—熵、吉布斯自由能小专题
日期:2026-04-20 16:54:38
点击:108
好评:0
疑难杂症之化学反应的方向—熵、吉布斯自由能小专题
日期:2026-04-20 16:54:38
点击:108
好评:0
化学反应的方向—熵、吉布斯自由能小专题。...
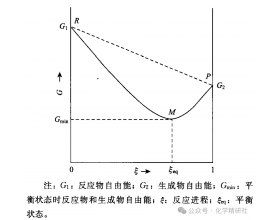 可逆反应的自发性能否用吉布斯自由能变(ΔG)判断
日期:2025-10-16 09:59:58
点击:455
好评:0
可逆反应的自发性能否用吉布斯自由能变(ΔG)判断
日期:2025-10-16 09:59:58
点击:455
好评:0
在化学热力学中,吉布斯自由能变(ΔG)是判断反应自发性的核心判据,其核心规律 “ΔG0 时反应自发,ΔG0 时反应非自发,ΔG=0 时反应达平衡” 已成为判断不可逆反应自发性的经典依据。然而,可逆反应 “同一条件下正、逆反应可同时进行” 的特性,常使学习者产生困惑...
 浅谈用“ΔG =ΔH-TΔS”对反应产物的分析
日期:2023-02-26 17:59:35
点击:12894
好评:0
浅谈用“ΔG =ΔH-TΔS”对反应产物的分析
日期:2023-02-26 17:59:35
点击:12894
好评:0
1 、焦炭在高温下与水蒸气的反应。本反应的主要产物是 CO 和 H 2 ,并非 CO 2 和 H 2 。由于化学反应 C(s)+H 2 O(g)=CO(g)+H 2 (g) 的Δ H y = ﹢ 132kJ/mol 、Δ G y = ﹢ 91kJ/mol 、Δ S y = ﹢ 133J/(K · mol) ,由Δ G y = ﹢ 91kJ/mol > 0 可知反应不能自发正向...
 巧用“自由能”判断化学反应方向
日期:2020-11-26 17:17:34
点击:1290
好评:0
巧用“自由能”判断化学反应方向
日期:2020-11-26 17:17:34
点击:1290
好评:0
第二页...
 应用△G定量研究中学化学中的若干问题
日期:2020-11-26 17:16:28
点击:1236
好评:0
应用△G定量研究中学化学中的若干问题
日期:2020-11-26 17:16:28
点击:1236
好评:0
第二页 第三页 第四页 第五页 第六页 第七页 第八页...
 巧用吉布斯自由能化解判断,化学反应的方向的疑难问题
日期:2020-11-26 17:03:03
点击:1031
好评:0
巧用吉布斯自由能化解判断,化学反应的方向的疑难问题
日期:2020-11-26 17:03:03
点击:1031
好评:0
化学反应体系趋于高能态向低能态转化。 对于放热反应来 说,是从高能向低能转变,故是一种自发进行的趋势。 所以一般 放热反应具有自发性, 即Δ H <0自发倾向大,Δ H >0非自发倾向 大。 虽然几乎所有的焓变小于零的放热反应都是自发的,但是 有不少的焓变大于零的吸热反...
 公开课短片-吉布斯自由能变与自发性
日期:2013-05-03 11:20:00
点击:571
好评:0
公开课短片-吉布斯自由能变与自发性
日期:2013-05-03 11:20:00
点击:571
好评:0
网易公开课视频-吉布斯自由能变与反应自发性。来源于可汗学院,虽说是大学的基础化学内容,可做为高中阶段复习或扩展内容,很通俗易懂。...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。