
|
С§П°РЎЧЁМв |
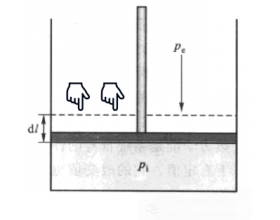 мКұдЎчHҫНКЗ·ҙУҰИИВрЈҝ
ИХЖЪЈә2024-09-21 17:48:07
өг»чЈә409
әГЖАЈә0
мКұдЎчHҫНКЗ·ҙУҰИИВрЈҝ
ИХЖЪЈә2024-09-21 17:48:07
өг»чЈә409
әГЖАЈә0
ДЬБҝ¶аЦЦ¶аСщЈ¬НЁіЈАҙЛөЈ¬МеПөөДЧЬДЬБҝ°ьАЁХыМеФЛ¶ҜөД¶ҜДЬЎўНвБҰіЎЦРөДО»ДЬЎўИИБҰС§ДЬЎЈИз№ыјЩ¶ЁМеПөКЗҫІЦ№өДЗТОЮМШКвНвБҰіЎҙжФЪЈ¬ҙЛКұМеПөҫНЦ»РиТӘҝјВЗИИБҰС§ДЬЈ¬јҙДЪДЬUЎЈ ИИБҰС§ДЬКЗЦёМеПөДЪ·ЦЧУФЛ¶ҜөДЖҪ¶ҜДЬЎўЧӘ¶ҜДЬЎўХс¶ҜДЬЎўөзЧУј°әЛөДДЬБҝЈ¬ТФј°·ЦЧУУл·ЦЧУПа»ҘЧч...
 ИзәОАнҪв·ҙУҰИИУлмКұдөДөҘО»Јҝ
ИХЖЪЈә2021-09-13 14:41:38
өг»чЈә969
әГЖАЈә0
ИзәОАнҪв·ҙУҰИИУлмКұдөДөҘО»Јҝ
ИХЖЪЈә2021-09-13 14:41:38
өг»чЈә969
әГЖАЈә0
ФЪТАҫЭ»ҜС§ҝОіМұкЧјұаРҙөДЦРС§»ҜС§ҪМІДЦРЈ¬НЁіЈ¶ј»бУРПВБРИИ»ҜС§·Ҫ іМКҪЈә 2H 2 (g) Ј« O 2 (g) =2H 2 O(1) ҰӨ H =Јӯ571. 1 kJ mol Јӯ1 H 2 (g)Ј«Ј«O 2 (g)= H 2 O(1) ҰӨ H =Јӯ285. 8 kJ mol Јӯ1 ФЪ»ҜС§ҪМС§ЦРЈ¬С§ЙъГЗіЈіЈ»бІъЙъПВБРА§»у:ФЪИИ»ҜС§·ҪіМКҪЦРЈ¬ҰӨ H өДөҘО»...
 ·ҙУҰИИУлмКұдКЗТ»»ШКВВр?
ИХЖЪЈә2018-08-05 15:20:24
өг»чЈә22904
әГЖАЈә1
·ҙУҰИИУлмКұдКЗТ»»ШКВВр?
ИХЖЪЈә2018-08-05 15:20:24
өг»чЈә22904
әГЖАЈә1
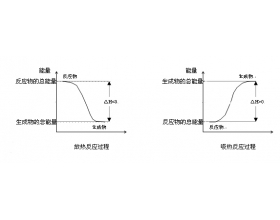
ОӘКІГҙІ»Н¬ҪМІДЦР¶ФмКұдөДГиКцІ»Н¬ДШЈ¬мКұдУл·ҙУҰИИЦ®јдөД№ШПөИзәОЈҝ ФЪИИБҰС§ЦРЈ¬УГQұнКҫ·ҙУҰ№эіМЦРөДИИБҝұд»ҜЎЈИф·ҙУҰОьИИЈ¬ФтQ0; Иф·ҙУҰ·ЕИИЈ¬ФтQ0ЎЈөұМеПөҙҰУЪұд»Ҝ№эіМКұ(·ҙУҰОпЧӘұдОӘЙъіЙОпТІКЗМеПө өДұд»ҜЈ©Ј¬МеПөУл»·ҫіЦ®јдҙжФЪНј1 - 8ЛщКҫөДДЬБҝҪ»»»ЎЈ өұМеПөұд»Ҝ»Ц...
 ОўҝОКУЖөЈә·ҙУҰИИ
ИХЖЪЈә2018-07-18 15:45:31
өг»чЈә283
әГЖАЈә0
ОўҝОКУЖөЈә·ҙУҰИИ
ИХЖЪЈә2018-07-18 15:45:31
өг»чЈә283
әГЖАЈә0
ОўҝОКУЖөЈә·ҙУҰИИУлёЯҝјөдРНАэМв·ЦОцЎЈ...
 ·ҙУҰИИЎўЦРәНИИЎўИјЙХИИөДБӘПөУлЗшұр
ИХЖЪЈә2017-09-21 15:40:00
өг»чЈә1265
әГЖАЈә0
·ҙУҰИИЎўЦРәНИИЎўИјЙХИИөДБӘПөУлЗшұр
ИХЖЪЈә2017-09-21 15:40:00
өг»чЈә1265
әГЖАЈә0
·ҙУҰИИ ЦРәНИИ ИјЙХИИ ә¬Те »ҜС§·ҙУҰ№эіМЦР·Еіц»тОьКХөДИИБҝ ФЪПЎИЬТәЦРЈ¬ЗҝЛбәНЗҝјо·ўЙъЦРәН·ҙУҰ¶шЙъіЙ1 mol H 2 O(l)КұЛщ·ЕіцөДИИБҝ ФЪ101 KPaКұЈ¬1 mol ОпЦКНкИ«ИјЙХЙъіЙОИ¶ЁөДСх»ҜОпКұЛщ·ЕіцөДИИБҝ ·ҙУҰМШөг ИОәО·ҙУҰ ЦРәН·ҙУҰ ИјЙХ·ҙУҰ ОпЦКЧҙМ¬ ОпЦКөДЧҙМ¬ТӘИ·¶Ё ...
 ·ҙУҰИИЎўЦРәНИИЎўИјЙХИИөДБӘПөУлЗшұр
ИХЖЪЈә2016-01-31 21:32:14
өг»чЈә13608
әГЖАЈә1
·ҙУҰИИЎўЦРәНИИЎўИјЙХИИөДБӘПөУлЗшұр
ИХЖЪЈә2016-01-31 21:32:14
өг»чЈә13608
әГЖАЈә1
·ҙУҰИИКЗҪьјёДкёЯҝјөДЦШөгДЪИЭЦ®Т»Ј¬МвРНТ»°гОӘСЎФсәНМоҝХЈ¬ҝјІйөДДЪИЭЦчТӘУРЈәИИ»ҜС§·ҪіМКҪөДХэОуЕР¶ПЎўұИҪП·ҙУҰИИөДҙу...
 »ҜС§јьУл·ҙУҰИИ
ИХЖЪЈә2016-01-31 19:53:22
өг»чЈә9966
әГЖАЈә0
»ҜС§јьУл·ҙУҰИИ
ИХЖЪЈә2016-01-31 19:53:22
өг»чЈә9966
әГЖАЈә0
»ҜС§·ҙУҰөДКөЦККЗҫЙ»ҜС§јьөДЖЖ»өәНРВ»ҜС§јьөДРОіЙЈ¬ЖЖ»ө»ҜС§јьРиТӘОьКХДЬБҝЈ¬РОіЙ»ҜС§јьРиТӘ·ЕіцДЬБҝЎЈ ·ҙУҰИИ = ·ҙУҰОпөДЧЬјьДЬ - ЙъіЙОпөДЧЬјьДЬЎЈІ»ДЬёщҫЭ·ҙУҰОпУлЙъіЙОпөДОИ¶ЁРФАҙЕР¶П·ҙУҰКЗ·ЕИИ»№КЗОьИИЈ¬ёьІ»ДЬёщҫЭ·ҙУҰКЗ·сРиТӘјУИИАҙЕР¶ПЈ¬ИзәПіЙ°ұ·ҙУҰЈ¬·ҙУҰОп...
 ёЯҝј·ҙУҰИИОКМвҪв·ЁАэМё
ИХЖЪЈә2016-01-31 19:51:10
өг»чЈә15438
әГЖАЈә0
ёЯҝј·ҙУҰИИОКМвҪв·ЁАэМё
ИХЖЪЈә2016-01-31 19:51:10
өг»чЈә15438
әГЖАЈә0
·ҙУҰИИКЗСРҫҝ»ҜС§·ҙУҰЦРДЬБҝұд»ҜөДЦШТӘёЕДоЈ¬·ҙУҰИИОКМвФтКЗёЯҝјөДЦШөгДЪИЭЈ¬ҙҰАнәГПа№ШМвДҝөД№ШјьКЗЙоҝМАнҪвёЕДоЈ¬ХЖОХҪвМв·Ҫ·ЁЎЈ Т»ЎўёЕДоұҫЦКЖКОц ИОәО»ҜС§·ҙУҰҪшРР№эіМЦР¶ј°йЛжЧЕДЬБҝөДұд»ҜЈ¬¶шХвЦЦДЬБҝіЈТФИИДЬөДРОКҪұнПЦіцАҙЈ¬ҙЛИИДЬөДҙуРЎЦ®¶ИБҝТФј°·ҙУҰ№эіМЦР...
 ·ҙУҰИИЦРөДјёёцДСөгҪвОц
ИХЖЪЈә2016-01-31 19:40:58
өг»чЈә16341
әГЖАЈә0
·ҙУҰИИЦРөДјёёцДСөгҪвОц
ИХЖЪЈә2016-01-31 19:40:58
өг»чЈә16341
әГЖАЈә0
ФЪөұҪсЙз»бЦРЈ¬ИЛАаЛщРиДЬБҝҫшҙуІҝ·ЦКЗУЙ»ҜС§·ҙУҰІъЙъөДЈ¬ТтҙЛЈ¬СРҫҝС§П°»ҜС§·ҙУҰЦРөД·ҙУҰИИЈ¬¶ФУЪИЛГЗід·ЦАыУГДЬФҙЈ¬јхЙЩ»·ҫіОЫИҫКЗЦБ№ШЦШТӘөДЎЈЛщТФУР№Ш·ҙУҰИИөДЦӘК¶ТІіЙОӘёЯҝјЦРөДЦШТӘҝјөгЎЈФЪС§П°·ҙУҰИИКұЈ¬УРИзПВјёёцДСөгУҰТэЖрОТГЗөДЧўТвЎЈ 1 ХэИ·АнҪвЗшұрИэИИёЕ...
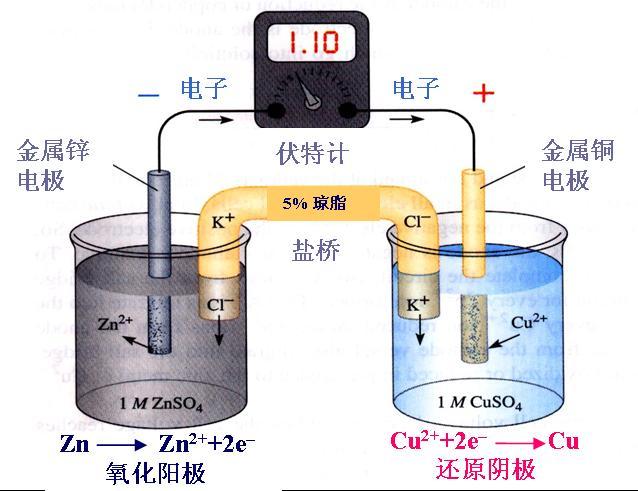 №«ҝӘҝО¶МЖ¬-мКУл·ҙУҰИИ
ИХЖЪЈә2013-05-03 11:02:35
өг»чЈә440
әГЖАЈә0
№«ҝӘҝО¶МЖ¬-мКУл·ҙУҰИИ
ИХЖЪЈә2013-05-03 11:02:35
өг»чЈә440
әГЖАЈә0
НшТЧ№«ҝӘҝОКУЖө-мКЈЁөЪТ»јҜЈ©Ул·ҙУҰИИЈЁөЪ¶юјҜЈ©ЎЈАҙФҙУЪҝЙә№С§ФәЈ¬ЛдЛөКЗҙуС§өД»щҙЎ»ҜС§ДЪИЭЈ¬ҝЙЧцОӘёЯЦРҪЧ¶ОёҙП°»тА©Х№ДЪИЭЈ¬әЬНЁЛЧТЧ¶®ЎЈ...
 »¶Уӯ¶©ФДНшХҫ¶ҜМ¬Ј¬КЦ»ъЙЁТ»ЙЁҫНҝЙТФЎЈ
»¶Уӯ¶©ФДНшХҫ¶ҜМ¬Ј¬КЦ»ъЙЁТ»ЙЁҫНҝЙТФЎЈ »¶УӯК№УГ»ҜС§ЧФП°КТAPPЈ¬ЙЁВлҫНҝЙПВФШЎЈ
»¶УӯК№УГ»ҜС§ЧФП°КТAPPЈ¬ЙЁВлҫНҝЙПВФШЎЈ