
|
学习小专题 |

|
学习小专题 |
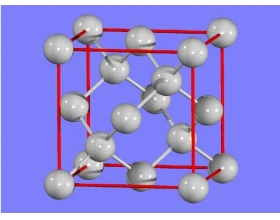 [注解与辨疑f] 金刚石的晶胞分析 作者:何清松 来源:未知 日期:2015-05-29 21:27:29 点击:92867 所属专题:金刚石晶胞
[注解与辨疑f] 金刚石的晶胞分析 作者:何清松 来源:未知 日期:2015-05-29 21:27:29 点击:92867 所属专题:金刚石晶胞
金刚石晶胞:面心立方结构,共有8粒碳原子,分别位于八个角,每角位占1/8粒,六个面心,每面占1/2粒,其余四整粒处于角原子及近邻面心原子间(底部对角两粒,顶部对角两粒),与旁边的四粒碳原子以共价键结合,组成了四个四面体。 金刚石属于面心立方晶胞,即C原子处在...
 [注解与辨疑f] 材料特性 作者:邬兆宇 来源:未知 日期:2022-11-23 09:02:17 点击:7486 所属专题:金属通性
[注解与辨疑f] 材料特性 作者:邬兆宇 来源:未知 日期:2022-11-23 09:02:17 点击:7486 所属专题:金属通性
硬度(Hardness) -是材料抵抗外物刺入的一种能力。用硬度试验器来试验是现代试验硬度常用的方法。最常用的试验法有洛氏硬度试验洛氏硬度试验机利用钻石冲入金属的深度来测定金属的硬度,冲入深度愈大,硬度愈...
 [注解与辨疑f] 晶体熔沸点的比较及应用 作者:甑炳杨 来源:未知 日期:2012-10-25 10:40:10 点击:26868 所属专题:晶体性质 熔点 沸点
[注解与辨疑f] 晶体熔沸点的比较及应用 作者:甑炳杨 来源:未知 日期:2012-10-25 10:40:10 点击:26868 所属专题:晶体性质 熔点 沸点
物质的熔沸点是物质的重要物理性质,物质熔沸点的高低与构成该物质的晶体类型及晶体内部微粒间的作用力有关,比较不同物质的熔沸点,根据不同情况有不同的依据,不同的规律,现分类解析如下: 一、根据作用力类型和大小比较熔沸点 1 、不同晶体类型的物质 (1)、一般情况下...
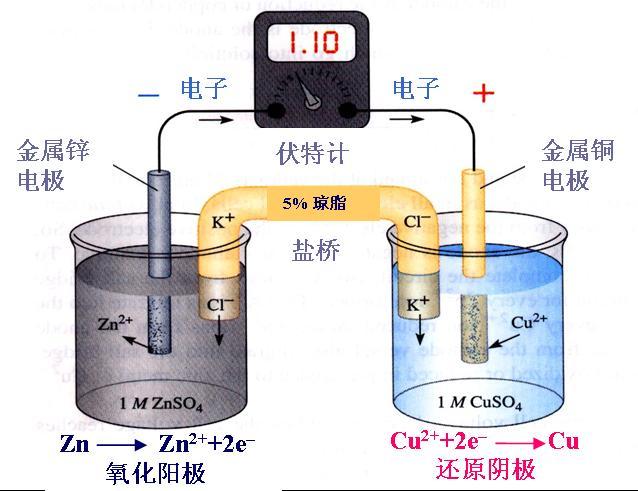 [注解与辨疑f] 晶体结构知识问答 作者:安勃 来源:未知 日期:2016-01-30 14:27:46 点击:10776 所属专题:晶体结构
[注解与辨疑f] 晶体结构知识问答 作者:安勃 来源:未知 日期:2016-01-30 14:27:46 点击:10776 所属专题:晶体结构
1. 哪类晶体中存在单个分子? 只有分子晶体中存在单个分子,它们的化学式一般是分子式。其他各类晶体中都没有单个分子存在,在固态时,它们只有化学式。 2. 几类晶体或分子中,参与成键作用的电子的属性有何区别? 在离子晶体中,阴、阳离子以离子键结合,成键时,电子...
 [注解与辨疑f] 晶体学习中的“一定与不一定” 作者:陈丽娟 来源:未知 日期:2016-01-30 14:32:37 点击:9139 所属专题:晶体结构与性质 是非判断
[注解与辨疑f] 晶体学习中的“一定与不一定” 作者:陈丽娟 来源:未知 日期:2016-01-30 14:32:37 点击:9139 所属专题:晶体结构与性质 是非判断
在学习物质结构的过程中,学生往往不能准确把握一些概念和规律,理解和认识上存在很多误区。下面对晶体知识学习中碰到的问题归纳如下: 1.分子晶体不一定都存在共价键,如希有气体形成的分子晶体;分子晶体中一定存在分子间作用力。 2.离子晶体中不一定都含有金属阳离...
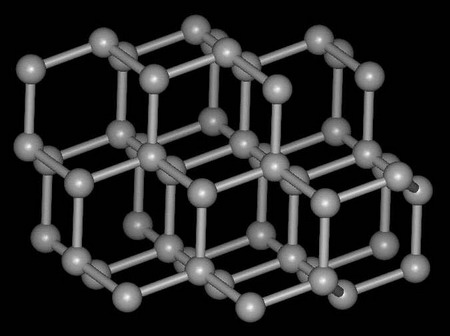
 [注解与辨疑f] 石墨晶体结构与性质 作者:杨董 来源:未知 日期:2016-01-30 14:33:46 点击:6640 所属专题:石墨晶胞
[注解与辨疑f] 石墨晶体结构与性质 作者:杨董 来源:未知 日期:2016-01-30 14:33:46 点击:6640 所属专题:石墨晶胞
在该晶体中,同层的碳原子采用sp2杂化轨道以σ键与其他碳原子连接成六元环形的蜂窝式层状结构,碳原子之间的结合力很强,极难破坏,所以石墨的熔点很高,化学性质很稳定。另外,每个碳原子都有垂直于每层平面的p轨道,而且p轨道相互平行,这些p电子可形成离域π键 距离...
 [注解与辨疑f] 金属同非金属的区别 作者:王欣华 来源:未知 日期:2016-01-30 14:34:55 点击:6774 所属专题:金属通性
[注解与辨疑f] 金属同非金属的区别 作者:王欣华 来源:未知 日期:2016-01-30 14:34:55 点击:6774 所属专题:金属通性
金属同非金属的区别,主要表现在以下几方面: (1)原子结构 金属原子的外层电子构型一般为ns 1-2 或ns 2 np 1-4 或(n-1)d 1-10 ns 1-2 ,最外层电子数较少(少数最外层电子数较多的金属元素,其电子层数也较多),原子半径比同周期非金属元素大。非金属元素原子的外层电子...
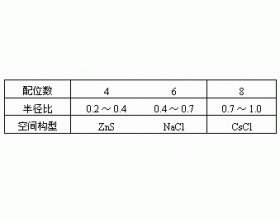 [注解与辨疑f] 离子晶体中离子的配位数 作者:爱莉 来源:未知 日期:2022-04-06 17:35:15 点击:8761 所属专题:离子晶体 晶胞配位数
[注解与辨疑f] 离子晶体中离子的配位数 作者:爱莉 来源:未知 日期:2022-04-06 17:35:15 点击:8761 所属专题:离子晶体 晶胞配位数
与中心离子(或原子)直接成键的离子(或原子)称为配位离子(或原子)。配位离子(或原子)的数目称为配位数,如在氯化钠晶体中,钠和氯的配位数都是6。离子晶体是通过离子键结合而成的,离子键的一个特点是没有方向性。离子是一个带电的质点(近似地认为是球体),根据静电学理...
 [注解与辨疑f] 混合型晶体 作者:童建军 来源:未知 日期:2016-01-30 14:41:14 点击:6301 所属专题:混合型晶体 石墨
[注解与辨疑f] 混合型晶体 作者:童建军 来源:未知 日期:2016-01-30 14:41:14 点击:6301 所属专题:混合型晶体 石墨
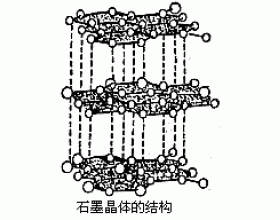
混合型晶体之一 除四种基本晶体类型外,还有一系列过渡型晶体,因为这些晶体中微粒间的作用力不只一种,所以常称为混合键型晶体。常见的混合键型晶体有层状结构和链状结构两种。石墨是一种典型的层状混合键型晶体,层内碳原子间有金属键,相邻碳原子间有共价键,层间有...
 [注解与辨疑f] AB型离子晶体的结构 作者:王欣华 来源:未知 日期:2017-04-25 16:06:17 点击:6407 所属专题:氯化钠晶胞 氯化铯晶胞 硫化锌晶胞
[注解与辨疑f] AB型离子晶体的结构 作者:王欣华 来源:未知 日期:2017-04-25 16:06:17 点击:6407 所属专题:氯化钠晶胞 氯化铯晶胞 硫化锌晶胞
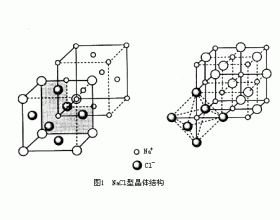
组成比为1∶1的离子晶体称为AB型离子晶体,它是离子晶体中最简单的一类。AB型离子晶体最常见的基本结构有NaCl型、CsCl型和ZnS型。 (1)NaCl型 NaCl型离子晶体中,每个离子被6个带相反电荷的离子包围,阴离子和阳离子的配位数都为6。常见的NaCl型离子晶体有碱金属元素(铯...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。在目前有些资料中,提及石墨中含有金属键。下面我们通过4种版本(人教版、鲁科版、苏...
金刚石硬度比石墨大得多,缘于金刚石的“均匀一体化”的空间网状结构,无论从哪个方向...
键能,常见有共价键的键能:使1mol 某共价键断裂所需的能量(键焓,kJ/mol)。 不说离子...
01原子结构 HCP,即密排六方晶格(Hexagonal Close Packed),是晶体结构的一种,其原...
硬度(Hardness) -是材料抵抗外物刺入的一种能力。用硬度试验器来试验是现代试验硬度常...
现行高中教材给出二氧化硅晶体的平面结构如下图1。该示意图准确地表示了二氧化硅晶体...
一、金属晶体的紧密堆积 二、体心立方堆积 三、面心立方堆积 四、六方最密堆积...
一、简单立方 二、面向立方 三、体心立方 四、立方...