
|
学习小专题 |

|
学习小专题 |
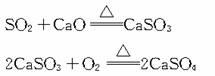 [注解与辨疑9] 工业消除二氧化硫常用的方法 作者:汪谦 来源: 日期:2016-01-28 19:43:34 点击:31387 所属专题:二氧化硫 大气污染
[注解与辨疑9] 工业消除二氧化硫常用的方法 作者:汪谦 来源: 日期:2016-01-28 19:43:34 点击:31387 所属专题:二氧化硫 大气污染
二氧化硫是空气中有害气体的罪魁祸首。当空气中二氧化硫的含量达到百万分之0.1~1时,植物、建筑物的结构材料就会严重受损;若达到百万分之1~10时,会引起人的呼吸道痉挛、流泪、咳嗽甚至死亡;若达到万分之一时,一切生命都会完结。因此我国规定:厂矿周围上空的空气...
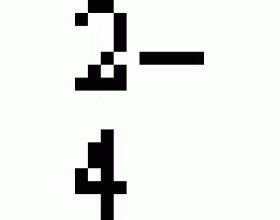 [注解与辨疑9] 硫酸根离子的检验讨论 作者:董啸 来源: 日期:2016-01-21 11:50:06 点击:11148 所属专题:硫酸根离子 离子检验
[注解与辨疑9] 硫酸根离子的检验讨论 作者:董啸 来源: 日期:2016-01-21 11:50:06 点击:11148 所属专题:硫酸根离子 离子检验
鉴定某未知溶液中是否含有SO ,这不是一个简单问题。它涉及到试剂选择和操作程序两个关键点的合理组合。因为,除应考虑Ag + 的常规干扰外,还必须考虑SO 、CO 、PO 等离子的干扰,否则将会产生以下错误。 1.误将Ag + 鉴定为SO 如向某未知溶液中滴加BaCl 2 溶...
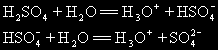 [注解与辨疑9] 稀释浓硫酸时为什么会放出大量的热? 作者:陈阳 来源: 日期:2025-08-07 15:09:42 点击:3748 所属专题:浓硫酸稀释
[注解与辨疑9] 稀释浓硫酸时为什么会放出大量的热? 作者:陈阳 来源: 日期:2025-08-07 15:09:42 点击:3748 所属专题:浓硫酸稀释
当硫酸溶解于水时,包括两个过程,硫酸分子向水中扩散是物理过程,这个过程要吸收一定的热量;另一过程是化学过程,即硫酸分子跟水分子化合,生成水合氢离子,这个过程要放出一定的热量。整个过程可以表示如下: 总的反应可表示为: 硫酸跟水能生成相当稳定的水合物,...
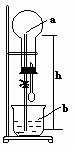 [注解与辨疑9] 漫话喷泉实验 作者:王瑜 来源: 日期:2016-01-21 12:14:08 点击:7809 所属专题:喷泉实验
[注解与辨疑9] 漫话喷泉实验 作者:王瑜 来源: 日期:2016-01-21 12:14:08 点击:7809 所属专题:喷泉实验
氯化氢等气体在喷泉实验中形成的美丽喷泉让人难以忘怀,那么喷泉形成的原理是什么呢?如何诱发喷泉的形成呢?用于作喷泉实验的气体的性质又有什么特点呢? 一、喷泉实验形成的物理原因 众所周知:公园、广场上的喷泉产生的原因是水承受的压强大于大气压。氯化氢气体、...
 [注解与辨疑9] 浓硫酸的脱水性与吸水性区别 作者:赵亭 来源: 日期:2019-06-03 21:38:06 点击:22420 所属专题:浓硫酸 脱水性 吸水性
[注解与辨疑9] 浓硫酸的脱水性与吸水性区别 作者:赵亭 来源: 日期:2019-06-03 21:38:06 点击:22420 所属专题:浓硫酸 脱水性 吸水性
在浓硫酸中,硫酸主要以分子形式存在。由于硫酸分子易与水分子化合形成水合分子,因此,浓硫酸具有吸水性和脱水性。 浓硫酸的吸水性是指能吸收游离的水或结晶水合物中的水,如:浓硫酸敞开放置增重;浓硫酸做干燥剂;浓硫酸使无水硫酸铜由蓝变白。 浓硫酸的脱水性是指...
 [注解与辨疑9] 为什么酒精、氨水的密度越小,浓度越小? 作者:朱康 来源: 日期:2016-01-21 12:24:57 点击:3978 所属专题:氨水 浓度与密度
[注解与辨疑9] 为什么酒精、氨水的密度越小,浓度越小? 作者:朱康 来源: 日期:2016-01-21 12:24:57 点击:3978 所属专题:氨水 浓度与密度
以酒精为例。水的密度是1g/cm 3 ,无水酒精的相对密度是0.7893g/cm 3 。由于酒精和水可以无限互溶,既有水多醇少的稀溶液,也可以是醇多水少的浓溶液。如果是前者,稀酒精溶液的密度当然趋于1,如果是后者,酒精浓溶液的密度自然小到趋于0.7893。 同理,氨水的密度...
 [注解与辨疑9] 浓硝酸能当漂白剂使用吗? 作者:胡中宇 来源: 日期:2016-01-21 11:23:12 点击:6242 所属专题:浓硝酸 漂白剂
[注解与辨疑9] 浓硝酸能当漂白剂使用吗? 作者:胡中宇 来源: 日期:2016-01-21 11:23:12 点击:6242 所属专题:浓硝酸 漂白剂
在说到浓硝酸的性质的时候,通常有这样的总结:第一,强酸性,即具有酸的通性;第二,不稳定性,即硝酸越浓,见光或热,越容易分解;第三,能与有机物反应,即制取TNT,硝化甘油等;第四,强氧化性,即无论浓稀都具有强的氧化性。在有的总结中,还会说到硝酸具有腐蚀性...
 [注解与辨疑9] 溴蒸汽和NO2都是红棕色气体,怎样鉴别呢? 作者:黄增春 来源: 日期:2016-01-21 11:09:42 点击:8865 所属专题:溴单质 二氧化氮 物质鉴别04
[注解与辨疑9] 溴蒸汽和NO2都是红棕色气体,怎样鉴别呢? 作者:黄增春 来源: 日期:2016-01-21 11:09:42 点击:8865 所属专题:溴单质 二氧化氮 物质鉴别04
思路一 、能否用 湿润的碘化钾-淀粉试纸 ? 上图的实验结果告诉我们:不能!原来 Br 2 和NO 2 都具有较强的氧化性,都可以将I - 氧化为碘单质 ! 思路二 、 加水试试 !结果左边的瓶中气体颜色褪去,溶液呈现无色,说明为NO 2 :3NO 2 +H 2 O=2HNO 3 +NO ,生成的硝酸...
 [注解与辨疑9] “氮及其化合物”学习误区指要 作者:徐志宏 来源: 日期:2016-01-21 11:05:57 点击:11304 所属专题:氮及其化合物
[注解与辨疑9] “氮及其化合物”学习误区指要 作者:徐志宏 来源: 日期:2016-01-21 11:05:57 点击:11304 所属专题:氮及其化合物
在化学学习过程中,考虑得比较多的常常是问题中规律性的一面,而忽略其中的特殊性,从而导致认识上的误区。氮族元素中的这种情况尤其多。现归纳如下。 误区 1 氮气化学性质不活泼,故氮元素是不活泼的非金属元素。 评析 : 判断元素非金属性强弱可以从其气态氢化物稳定...
 [注解与辨疑9] 氧化性酸和酸的氧化性概念辨析 作者:徐志宏 来源: 日期:2016-01-21 11:02:56 点击:6190 所属专题:氧化性酸
[注解与辨疑9] 氧化性酸和酸的氧化性概念辨析 作者:徐志宏 来源: 日期:2016-01-21 11:02:56 点击:6190 所属专题:氧化性酸
(1) 酸的氧化性:是指氢离子获得电子的能力,氢是H+的氧化性,是酸的通性离子显氧化性,由于任何酸都有不同程度电离出H+的能力,因此在某些反应中酸作氧化剂,其实质上是H+作氧化剂。如:锌与盐酸或稀H 2 SO 4 的反应,都可以用Zn+2H+=Zn2++H2,该离子方程式表...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
一、总方法:接触法 整个工业制硫酸分为三个阶段、三个设备、...
1.硫代硫酸钠(Na 2 S 2 O 3 ): Na 2 S 2 O 3 ·5H 2 O俗名海波或大苏打,...
...
磷作为周期表第 ⅤA 族核心元素,兼具 “生命不可替代性”(构...
硫酸盐 俗名 颜色 用途 2CaSO 4 H 2 O 熟石膏 白色 CaSO 4 2H 2 O 生石膏...
...
1.在二元化合物中,如果电正性的金属元素仅出现两种氧化态时...
合金的熔点一定低于各成分金属吗?教材只是说合金的硬度、熔...