
|
学习小专题 |

|
学习小专题 |
 [方法与规律e] 杂化轨道的判断 作者:化学自习室 来源:未知 日期:2023-01-10 10:01:48 点击:4106 所属专题:杂化类型判断
[方法与规律e] 杂化轨道的判断 作者:化学自习室 来源:未知 日期:2023-01-10 10:01:48 点击:4106 所属专题:杂化类型判断
一、基本方法 最基本的常规方法,是根据 VSEPR 判断。由于 Vp (价层电子对数) =Lp (孤电子对数) + Bp ( σ 键电子对数),而杂化轨道要么用来容纳孤电子对( Lp ),要么填充 1 个电子用来形成 σ 键( Bp )。因此 杂化轨道数就等于 Vp 数 。 (中学教材只涉及了 ...
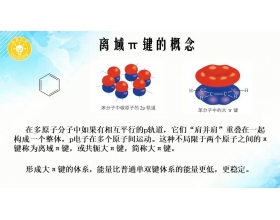 [方法与规律e] 电子式法快速判断大π键类型 作者:叶昌平 来源:启迪化学 日期:2022-08-13 09:14:16 点击:3385 所属专题:大π键
[方法与规律e] 电子式法快速判断大π键类型 作者:叶昌平 来源:启迪化学 日期:2022-08-13 09:14:16 点击:3385 所属专题:大π键
作者说解:离域π键的类型可依据概念进行判断、或依据等电子原理判断、或用电子式快速分析判断。在高中不宜讲解过深、过于复杂,更不应该作为一个知识点做系统补充,2017年全国卷二考察N5-离子的大 π 键类型是基于信息和能力的考察,主要考察学生对于原子轨道和轨道间...
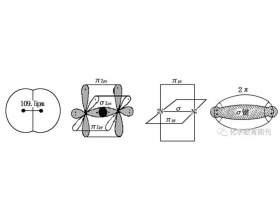 [方法与规律e] 氮及其化合物的分子空间结构分析 作者:张仿刚 来源:化学教育期刊 日期:2022-07-29 10:23:13 点击:14707 所属专题:氮及其化合物 分子空间结构判断
[方法与规律e] 氮及其化合物的分子空间结构分析 作者:张仿刚 来源:化学教育期刊 日期:2022-07-29 10:23:13 点击:14707 所属专题:氮及其化合物 分子空间结构判断
氮原子的价电子结构为2s22p3,电负性仅次于氟与氧,能与其他元素形成较强的化学键,存在多种价态,高中生很难正确把握氮及其化合物的结构,笔者对此进行理论分析和结构总结,以期有助于师生的正确理解。 根据中心原子成键时杂化方式的不同,本文将氮及其化合物分成四大...
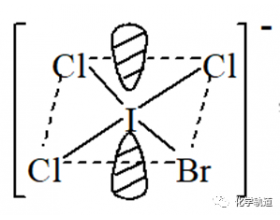 [方法与规律e] 一个多卤离子的空间结构 作者:化学自习室 来源:未知 日期:2022-07-29 10:12:55 点击:1029 所属专题:分子空间结构判断
[方法与规律e] 一个多卤离子的空间结构 作者:化学自习室 来源:未知 日期:2022-07-29 10:12:55 点击:1029 所属专题:分子空间结构判断
题目: 根据VSEPR理论,对于IBrCl3-: (1)计算其中心原子的价层电子对数; (2)画出几何构型; (3)指出孤电子对数; (4)给出分子构型的名称; (5)对分子结构中键角可能偏离理想构型的情况给予简单说明。 解析: 中心原子:I 配位原子(共4个):1个Br-,3个Cl-...
 [方法与规律e] 化学平衡图像疑难问题:最高点一定是平衡点吗? 作者:化学自习室 来源:未知 日期:2021-11-30 16:32:51 点击:1628 所属专题:化学平衡图像
[方法与规律e] 化学平衡图像疑难问题:最高点一定是平衡点吗? 作者:化学自习室 来源:未知 日期:2021-11-30 16:32:51 点击:1628 所属专题:化学平衡图像
【思考】 最高 点一定就是平衡点吗? 最高 点后一定是平衡移动吗?先来看几道高考题 1 .( 2019 江苏)在恒压、 NO 和 O 2 的起始浓度一定的条件下,催化反应相同时间,测得不同温度下 NO 转化为 NO 2 的转化率如图中实线所示 ( 图中虚线表示相同条件下 NO 的平衡转化...
 [方法与规律e] 快速判断非ABn型分子或离子杂化方式 作者:胡明生 来源:化学一点通 日期:2021-11-30 15:01:56 点击:1603 所属专题:杂化类型判断
[方法与规律e] 快速判断非ABn型分子或离子杂化方式 作者:胡明生 来源:化学一点通 日期:2021-11-30 15:01:56 点击:1603 所属专题:杂化类型判断
众所周知,价电子对互斥理论可以比较容易的判断AB n 型分子或离子的中心原子A的杂化方式。那么非AB n 型分子如何处理呢?根据该理论中心原子价层电子对计算方法我们知道H及X(卤素)提供一个价层电子,O或S不提供价层电子。所以我们可以总结出几条法则: ①增X减H或减X增氢中...
 [方法与规律e] 分子极性如何判断?四步就能搞定 作者:化学自习室 来源:未知 日期:2021-08-26 09:04:34 点击:1141 所属专题:分子极性
[方法与规律e] 分子极性如何判断?四步就能搞定 作者:化学自习室 来源:未知 日期:2021-08-26 09:04:34 点击:1141 所属专题:分子极性
化学键学习过程中我们会遇到一个概念,就是化学键的极性,如何判断化学键的极性以及分子的极性也是高种化学考察的一个重要知识点,高一正在学习或者刚刚学过这部分的同学们一定要仔细看哦~ 分子极性判断方法 STEP1、共价键的极性判断 化学键有无极性,是相对于共价键而...
 [方法与规律e] 怎样从形成方式上区分不同的共价键? 作者:化学自习室 来源:未知 日期:2021-08-23 20:50:09 点击:378 所属专题:共价键分类
[方法与规律e] 怎样从形成方式上区分不同的共价键? 作者:化学自习室 来源:未知 日期:2021-08-23 20:50:09 点击:378 所属专题:共价键分类
...
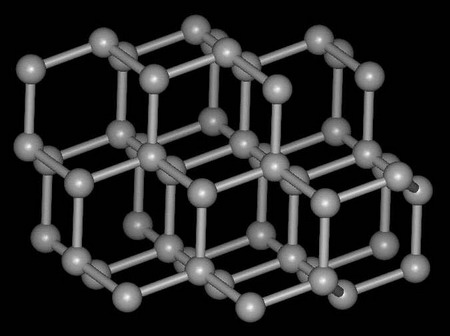 [方法与规律e] 怎样分析分子的极性? 作者:化学自习室 来源:未知 日期:2021-08-23 19:30:04 点击:1317 所属专题:分子极性
[方法与规律e] 怎样分析分子的极性? 作者:化学自习室 来源:未知 日期:2021-08-23 19:30:04 点击:1317 所属专题:分子极性
分子内存在正、负两极的分子称为极性分子,分子内不存在正、负 两极的分子称为非极性分子。分子是否有极性,其直接原因是分子内 正电荷的中心与负电荷的中心是否重合在同一点上。而这又是由分子的几何对称性、分子内共价键的极性共同决定的。 只有极性键才满足原子间的共用...
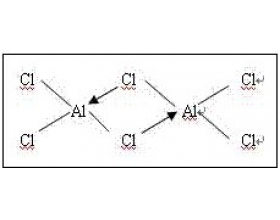 [方法与规律e] 怎么判断配合物的配位数? 作者:化学自习室 来源:未知 日期:2022-04-06 17:26:09 点击:9099 所属专题:配合物配位数
[方法与规律e] 怎么判断配合物的配位数? 作者:化学自习室 来源:未知 日期:2022-04-06 17:26:09 点击:9099 所属专题:配合物配位数
配合物的配位数是指直接同中心离子(或原子)配位的原子数目。高中化学配合物的配位数可按如下方法判断: 1.配合物的配位数等于配位原子及配位体的数目 有两种情况: (1)配位原子数目、配位体数目、中心离子与配位原子形成的配位键键数均相等 例如[Ag(NH3)2]NO3、[Cu(N...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。1.σ键与π键 σ键:原子轨道沿着轨道对称轴的方向“头碰头”重叠形成的共价键。 π键...
配位化合物的空间构型: 二配位:直线型;四配位:正四面体型或平面正方形;六配位(无...
1、当中心离子(或原子)与多基配体配合时,配位数可以等同于配位原子的数目,但不是配...
一、 知识储备 1、 手性 手性 ( chirality ) 一词指一个物体不能与其镜像相重合 。 ...
人的左手和右手互为实物和镜像关系,彼此不能重合。手的这种特征在其他物质中也广泛存...
对于ABn型分子, 其中:①a表示中心原子的价电子数; 对主族元素:a=最外层电子数; ...
固态氨的障构比冰的复杂.每一个氮原子周围有6个最邻近 的氮原子,它们之间的距离为3.3...
分子的立体结构是指其原子在空间的排布,可以用现代实验手段测定。例如,通过分子或离...