
|
学习小专题 |

|
学习小专题 |
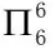 [注解与辨疑e] 高中常见微粒中的大π键问题 作者:化学自习室 来源:未知 日期:2020-01-31 11:54:32 点击:16760 所属专题:大π键
[注解与辨疑e] 高中常见微粒中的大π键问题 作者:化学自习室 来源:未知 日期:2020-01-31 11:54:32 点击:16760 所属专题:大π键
在最近几年全国卷高考化学试题的物质结构与性质选做题中,经常涉及到大π键的考查。例如:2017年全国卷II分子中的大π键可用符号表示,其中 m 代表参与形成的大π键原子数, n 代表参与形成大π键的电子数(如苯分子中的大π键可表示 ),则N 5 - 中的大π键应表示为(答...
 [注解与辨疑e] HF分子间氢键比水分子间氢键强,为什么水的沸点比HF高? 作者:化学自习室 来源:未知 日期:2024-03-13 08:30:45 点击:5535 所属专题:氢键与熔沸点 氟化氢
[注解与辨疑e] HF分子间氢键比水分子间氢键强,为什么水的沸点比HF高? 作者:化学自习室 来源:未知 日期:2024-03-13 08:30:45 点击:5535 所属专题:氢键与熔沸点 氟化氢
液体气化时除了破坏分子间作用力外,还必须破坏分子间氢键,需要消耗更多的能量。计算表明,氢键的键能要占水分子之间的分子间作用力总量的5/6。H 2 O和HF的熔点、沸点异常地高,就是由于这些分子间存在着氢键的缘故。 物质分子间若形成氢键,有可能发生缔合现象。液态H...
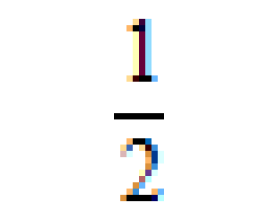 [注解与辨疑e] 杂化轨道理论的基本要点及类型 作者:化学自习室 来源:未知 日期:2020-01-01 11:17:34 点击:33118 所属专题:杂化轨道理论 杂化类型判断
[注解与辨疑e] 杂化轨道理论的基本要点及类型 作者:化学自习室 来源:未知 日期:2020-01-01 11:17:34 点击:33118 所属专题:杂化轨道理论 杂化类型判断
什么叫杂化? 同一原子的能量相近的原有的原子轨道“混杂”起来,重新组合形成新轨道的过程,叫做杂化。 什么叫杂化轨道? 新组合的原子轨道叫做杂化轨道。 为什么要杂化? 杂化轨道形成的化学键的强度更大,体系的能量更低。 杂化的动力: 受周围原子的影响。 为什么杂...
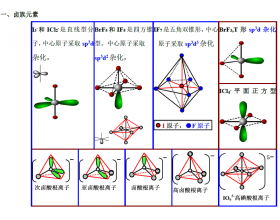 [注解与辨疑e] 常见分子的杂化方式图谱 作者:化学自习室 来源:未知 日期:2019-12-06 22:24:08 点击:5528 所属专题:杂化类型判断
[注解与辨疑e] 常见分子的杂化方式图谱 作者:化学自习室 来源:未知 日期:2019-12-06 22:24:08 点击:5528 所属专题:杂化类型判断
四、碳族 五、硼族 六、碱金属和碱土金属 七、铁...
 [注解与辨疑e] ClO2分子为什么是sp2杂化? 作者:化学自习室 来源:未知 日期:2019-06-28 09:15:41 点击:18346 所属专题:杂化类型判断
[注解与辨疑e] ClO2分子为什么是sp2杂化? 作者:化学自习室 来源:未知 日期:2019-06-28 09:15:41 点击:18346 所属专题:杂化类型判断
中学化学在讲授分子杂化类型时,首先根据公式计算出孤电子对数目 对于AB n 型分子。中心原子上的孤电子对数:1/2(a—nb)=1/2(A的价电子数-▕B的化合价▏×B的个数)=1/2(7-2×2)=1.5。孤电子对数为1.5,说明有一个单电子,同样占据一个轨道。把孤电子对数看作2,另外C...
 [注解与辨疑e] 氢键的形成对物质性质有哪些影响? 作者:化学自习室 来源:未知 日期:2019-06-13 10:02:40 点击:19993 所属专题:氢键02
[注解与辨疑e] 氢键的形成对物质性质有哪些影响? 作者:化学自习室 来源:未知 日期:2019-06-13 10:02:40 点击:19993 所属专题:氢键02
氢键通常是物质在液态时形成的,但形成后也能继续存在于某些晶态甚至气态物质中,氢键的形成对物质性质的影响主要有几点。 (1) 对物质熔沸点的影响。 分子间能形成氢键的物质,一般都具有较高的熔点和沸点,这是因为固体熔化或液体气化时除了破坏范德华力外,还必须破坏分子...
 [注解与辨疑e] 什么是“相似相溶原理”及在工业生产和实际 生活中用途? 作者:化学自习室 来源:未知 日期:2019-06-13 09:55:41 点击:4093 所属专题:相似相溶
[注解与辨疑e] 什么是“相似相溶原理”及在工业生产和实际 生活中用途? 作者:化学自习室 来源:未知 日期:2019-06-13 09:55:41 点击:4093 所属专题:相似相溶
1、 什么是“相似相溶原理”? 解答: “相似相溶原理”是一个关于物质溶解性的经验规律,其内涵是“结构相似的化合物容易互相混溶,结构相差很大的化合物不易互溶”。其中“结构”二字主要有两层含义:一是指物质结合在一起所依靠的化学键类型,对于由分子结合成的物质,主...
 [注解与辨疑e] 常见的等电子体实例 作者:化学自习室 来源:未知 日期:2022-11-21 08:39:14 点击:4016 所属专题:等电子体
[注解与辨疑e] 常见的等电子体实例 作者:化学自习室 来源:未知 日期:2022-11-21 08:39:14 点击:4016 所属专题:等电子体
常见的等电子体实例: 原子总数(原子核数) 价电子数总数 举例 结构 单原子(单核) 8 Ne,N 3- ,O 2- ,F - ,Na + ,Mg 2+ ,Al 3+ 18 Ar,S 2- ,Cl - ,K + ,Ca 2+ 核外电子总数为10电子 Ne, HF, H 2 O, NH 3 , CH 4 (分子类) Na + , Mg 2+ , NH 4...
 [注解与辨疑e] σ键一定比π键牢固吗? 作者:龙阜 来源:未知 日期:2019-06-05 10:26:27 点击:10690 所属专题:σ键 π键
[注解与辨疑e] σ键一定比π键牢固吗? 作者:龙阜 来源:未知 日期:2019-06-05 10:26:27 点击:10690 所属专题:σ键 π键
σ键一定比π键牢固吗? 答:在有机化合物中,碳原子之间形成的π键的重叠程度要比σ键的重叠程度小的多,所以C和C原子间形成σ键一定比π键牢固。一般 σ 键比 π 键牢固,但也有特例,如N 2 中π键比σ键牢固。 由表3不难看出N 2 中π键比σ键牢固,而 C和C原子间形成σ键...
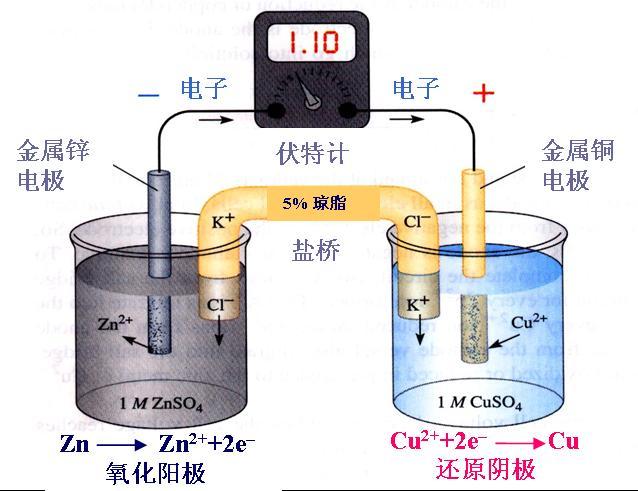 [注解与辨疑e] 等电子体的结构相似,性质一定相似吗? 作者:龙阜 来源:未知 日期:2022-11-21 08:39:32 点击:3708 所属专题:等电子体
[注解与辨疑e] 等电子体的结构相似,性质一定相似吗? 作者:龙阜 来源:未知 日期:2022-11-21 08:39:32 点击:3708 所属专题:等电子体
等电子体的结构相似,性质一定相似吗? 答:等电子体的结构相似,性质不一定相似。 如CO和N 2 物理性质相近,但它们的化学性质有显著差异。 由同主族元素构成的等电子体,如卤素单质及其氢化物,它们的性质有较多相似性; 其他等电子体,如O 3 和SO 3、 H 3 O + 和NH 3 ...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
冠醚是一类大环多醚化合物,其分子结构呈环状,环上均匀分布...
在高考备考化学试卷里,经常会遇到含钯的催化剂。本文将就钯...
在离子晶体中存在离子极化现象,使得离子键带有一定共价键的...
【情境】:你注意到我们每天都离不开的水有什么反常之处吗?...
氢键的大小(强度)可以通过多种因素来比较,这些因素包括氢键...
...
EDTA(Ethylenediaminetetraacetic acid,乙二胺四乙酸)是一种具有广泛...
说明:本文介绍了配位化合物的基本概念和构成要素,包括中心...