
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
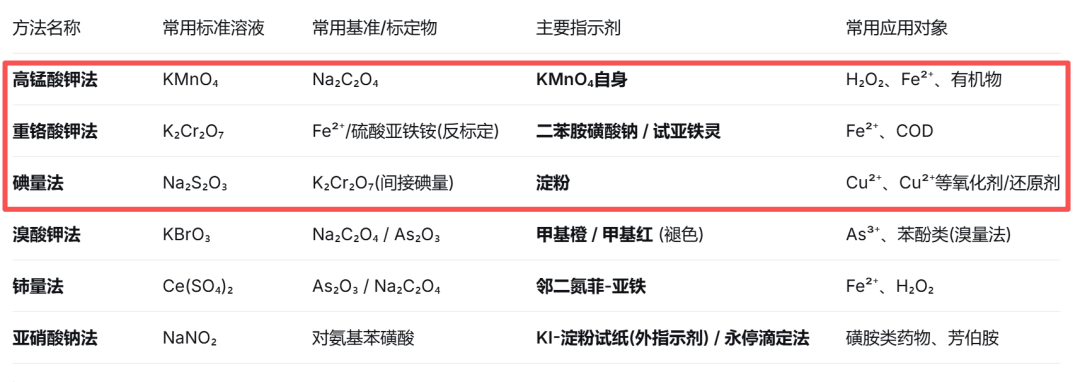
氧化还原滴定法以氧化还原反应为基础,根据滴定剂命名,主要包括高锰酸钾法、重铬酸钾法、碘量法、溴酸钾法、铈量法、亚硝酸钠法等。
以下分别列出其标准溶液的标定方程式、常见应用测定及使用的指示剂。
一、高锰酸钾法>
高锰酸钾法以KMnO₄为标准溶液,在强酸性溶液中被还原为Mn²⁺,是一种强氧化剂。基本原理——不同介质中MnO₄⁻的还原产物不同,酸性条件(H₂SO₄)下还原为Mn²⁺ (无色),应用最广;KMnO₄本身为紫红色,微量即呈粉红色,常可作自身指示剂。
1. KMnO₄标准溶液的配制和标定(以草酸钠或二水合草酸为基准物质)
配制:称取稍多于理论量的KMnO₄,溶于水,加热煮沸(去除还原性杂质),用玻璃滤器(或砂芯漏斗)过滤除去MnO2,储于棕色瓶中暗处保存。
标定方程式(在H₂SO₄介质中)——:
2MnO₄⁻ + 5C₂O₄²⁻ + 16H⁺ → 2Mn²⁺ + 10CO₂↑ + 8H₂O
指示剂:KMnO₄自身(自身指示剂),化学计量点后过量半滴
颜色变化:溶液由无色(近终点)→ 微红(粉红色保持30秒不褪)
条件:温度70~85℃(反应慢,需加热)、H₂SO₄介质、滴定初始速度要慢(因Mn²⁺自催化),终点粉红色保持30秒不褪。
2. 应用测定——直接滴定
2MnO₄⁻ + 5H₂O₂ + 6H⁺ → 2Mn²⁺ + 5O₂↑ + 8H₂O
MnO₄⁻ + 5Fe²⁺ + 8H⁺ → Mn²⁺ + 5Fe³⁺ + 4H₂O
二、重铬酸钾法
重铬酸钾法以K₂Cr₂O₇为标准溶液,在酸性介质(通常为稀H2SO4)中氧化性强,Cr₂O₇²⁻被还原为Cr³⁺(绿色)。
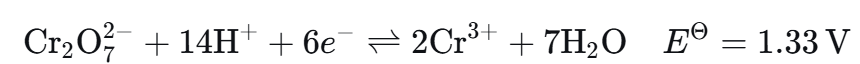

1. K₂Cr₂O₇标准溶液的配制与标定
K₂Cr₂O₇性质稳定,常用直接法配制标准溶液。必要时可用硫酸亚铁铵(NH₄)₂Fe(SO₄)₂进行反标定。
标定方程式(K₂Cr₂O₇与Fe²⁺的反应):
Cr₂O₇²⁻ + 6Fe²⁺ + 14H⁺ → 2Cr³⁺ + 6Fe³⁺ + 7H₂O
指示剂:重铬酸钾法自身颜色变化不明显(Cr₂O₇²⁻橙色 → Cr³⁺绿色,稀溶液中颜色浅,不易判断终点),因此必须使用氧化还原指示剂,即二苯胺磺酸钠 或 试亚铁灵
用二苯胺磺酸钠作指示剂时颜色变化:无色 → 紫色/紫红色——指示剂本身具有氧化还原性,其氧化型与还原型颜色不同。在滴定过程中,过量的Cr₂O₇²⁻(约超过0.1%~0.2%)将指示剂由还原态(无色)氧化为氧化态(紫红色);
变色电位:

用试亚铁灵作指示剂时颜色变化:黄色 → 蓝绿色 → 红褐色
2. 应用测定——直接滴定

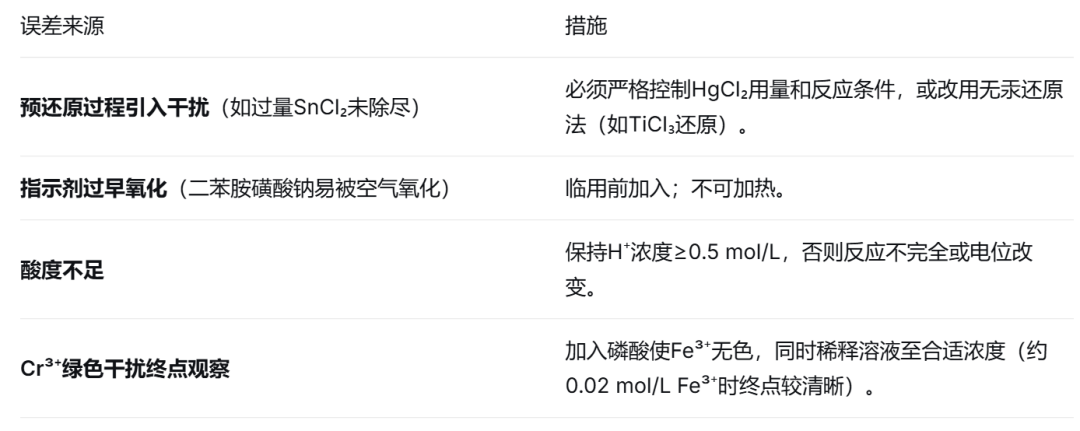
铁矿石中铁含量的测定(经典方法):用SnCl₂将Fe³⁺预还原为Fe²⁺,再用HgCl₂除去过量SnCl₂,最后以二苯胺磺酸钠为指示剂,用K₂Cr₂O₇滴定。
Cr₂O₇²⁻ + 6Fe²⁺ + 14H⁺ → 2Cr³⁺ + 6Fe³⁺ + 7H₂O (经典铁矿石分析法,预处理将Fe³⁺还原为Fe²⁺)
化学需氧量(COD)的测定——返滴定法:在强酸性条件下,K₂Cr₂O₇氧化水样中的还原性有机物,剩余Cr₂O₇²⁻用硫酸亚铁铵回滴。
用试亚铁灵作指示剂时颜色变化:黄色 → 蓝绿色 → 红褐色
重铬酸钾法最大的优点之一是可在盐酸介质中进行,因为K₂Cr₂O₇氧化Cl⁻的反应速率极慢(需加热或浓酸才明显),故测定含Cl⁻试样中的Fe²⁺时常用此法。
重铬酸钾法的一个突出优点是:K₂Cr₂O₇ 是基准物质(纯度≥99.95%,不易吸湿,高温下稳定),可以直接配制标准溶液,无需标定。
三、碘量法
碘量法利用I₂的氧化性和I⁻的还原性,分为直接碘量法(I₂滴定还原剂—升华碘溶于KI溶液l标定:用已标定的Na₂S₂O₃或用As₂O₃基准物质标定)和间接碘量法(利用I⁻还原待测物,释放的I₂用硫代硫酸钠Na₂S₂O₃滴定)。
1.基本原理:

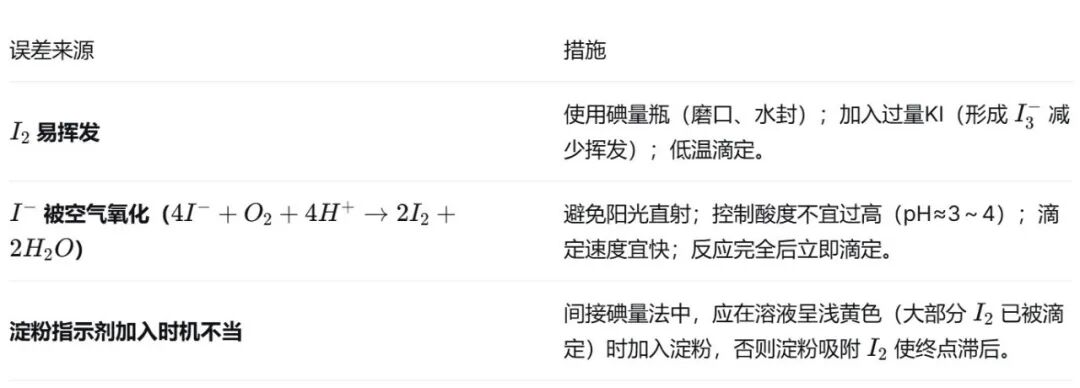
2. 误差来源及措施
1. Na₂S₂O₃标准溶液的配制与标定
Na₂S₂O₃不稳定,需间接配制并标定,用新煮沸冷却的蒸馏水(除去CO₂、O₂、杀菌)配制,加入少量Na₂CO₃使pH≈9~10;之后用KIO₃或K₂Cr₂O₇作基准物标定(置换碘量法)
标定方程式:基准物(如K₂Cr₂O₇)在酸性条件下与过量KI反应生成I₂,再用Na₂S₂O₃滴定:
Cr₂O₇²⁻ + 6I⁻ + 14H⁺ → 2Cr³⁺ + 3I₂ + 7H₂O
I₂ + 2S₂O₃²⁻ → 2I⁻ + S₄O₆²⁻
指示剂:可溶性淀粉溶液,与I₂ 形成深蓝色络合物,灵敏度高(10⁻⁵ M I₂ 即显色)。注意在稀KI存在下显色最佳。
颜色变化(用Na₂S₂O₃滴定生成的I₂):
深棕色 → 浅黄色(加淀粉)→ 蓝色 → 亮绿色(三价铬颜色)或无色
2. 应用测定(间接碘量法为主)
2Cu²⁺ + 4I⁻ → 2CuI↓ + I₂; I₂ + 2S₂O₃²⁻ → 2I⁻ + S₄O₆²⁻
Cr₂O₇²⁻ + 6I⁻ + 14H⁺ → 2Cr³⁺ + 3I₂ + 7H₂O;I₂ + 2S₂O₃²⁻ → 2I⁻ + S₄O₆²⁻
淀粉指示剂在间接碘量法中必须临近终点时加入(当I₂颜色呈淡黄色时),否则淀粉会吸附I₂导致结果偏低。
3. 误差来源和注意事项
四、溴酸钾法
溴酸钾法以KBrO₃为标准溶液,在酸性介质中是强氧化剂(BrO₃⁻ + 6H⁺ + 6e⁻ → Br⁻ + 3H₂O),可直接滴定还原性物质(如As³⁺、Fe²⁺等)。
1. KBrO₃标准溶液的配制与标定
KBrO₃性质稳定,可用直接法(基准物质)配制标准溶液。必要时可用基准物Na₂C₂O₄或As₂O₃标定:
BrO₃⁻ + 5Br⁻ + 6H⁺ → 3Br₂ + 3H₂O
2. 测定苯酚类有机物——溴量法(返滴定)、淀粉做指示剂,间接碘量法终点现象:
BrO₃⁻ + 5Br⁻ + 6H⁺ → 3Br₂ + 3H₂O;Br₂ + C₆H₅OH → 三溴苯酚↓ + HBr;
剩余Br₂ + 2I⁻ → I₂ + 2Br⁻;I₂ + 2S₂O₃²⁻ → 2I⁻ + S₄O₆²⁻
五、铈量法(硫酸铈法)
铈量法以Ce(SO₄)₂为标准溶液,利用Ce⁴⁺/Ce³⁺电对在酸性介质中的强氧化性进行滴定。
1. Ce(SO₄)₂标准溶液的配制与标定
基准物As₂O₃在HCl介质中用Ce⁴⁺滴定,以邻二氮菲-亚铁作指示剂。标定反应(以基准物As₂O₃为例):
As₂O₃ + 2OH⁻ → 2AsO₂⁻ + H₂O(溶解);
AsO₂⁻ + 2Ce⁴⁺ + 2H₂O → AsO₄³⁻ + 2Ce³⁺ + 4H⁺(滴定)
2. 应用测定——直接滴定、指示剂:邻二氮菲-Fe²⁺/橙红色 → 浅蓝色
Ce⁴⁺ + Fe²⁺ → Ce³⁺ + Fe³⁺;
2Ce⁴⁺ + H₂O₂ → 2Ce³⁺ + O₂ + 2H⁺
六、亚硝酸钠法
亚硝酸钠法主要基于重氮化反应,利用NaNO₂在酸性条件下与芳香伯胺发生重氮化反应。广泛用于药物分析(如磺胺类药物)。
1. NaNO₂标准溶液的标定
使用基准物对氨基苯磺酸(Ar-NH₂)在HCl介质中进行重氮化反应:
H₂N-C₆H₄-SO₃H + NaNO₂ + 2HCl → Ar-N₂⁺Cl⁻ + NaCl + 2H₂O
指示方法:
外指示剂:KI-淀粉试纸或溶液,终点时溶液点试纸变蓝(2HNO₂ + 2I⁻ + 2H⁺ → I₂ + 2NO + 2H₂O);
内指示剂:橙黄Ⅳ-亚甲蓝混合指示剂,终点由蓝绿色变蓝灰色;
常见化学方程式补充:
一、高锰酸钾法
1.标定反应(以草酸钠Na₂C₂O₄为基准物,H₂SO₄介质)
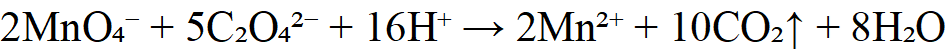
2.测定过氧化氢H₂O₂
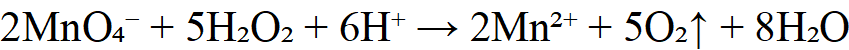
3.测定亚铁离子 Fe²⁺
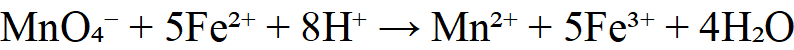
4.测定草酸根 C₂O₄²⁻(或草酸)
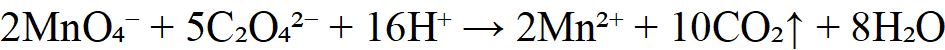
二、重铬酸钾法
1.标定反应(用硫酸亚铁铵或Fe²⁺标准溶液标定K₂Cr₂O₇,也可反标定)
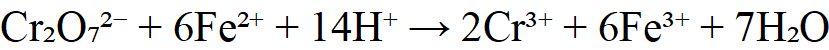
2.测定铁矿石中的全铁(Fe²⁺)
同上式,将试样还原为Fe²⁺后用K₂Cr₂O₇直接滴定。
3.化学需氧量(COD)测定(返滴定法)
(1)过量K₂Cr₂O₇氧化有机物(有机物被氧化为CO₂,Cr₂O₇²⁻被还原为Cr³⁺,一般不写具体有机物方程式)
(2)剩余Cr₂O₇²⁻用Fe²⁺标准溶液滴定
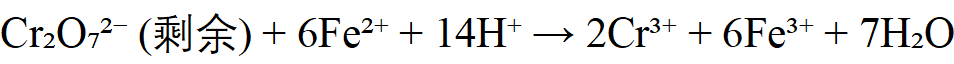
三、碘量法
碘量法分为直接碘量法(I₂滴定还原剂)和间接碘量法(待测物氧化I⁻生成I₂,再用Na₂S₂O₃滴定I₂)。
(一)直接碘量法(I₂ 标准溶液)
1.标定I₂溶液(用As₂O₃基准物)
As₂O₃先溶于碱:
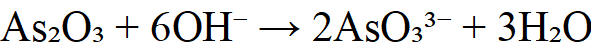
酸化后AsO₃³⁻变为H₃AsO₃,再用I₂滴定:
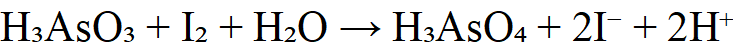
2.测定维生素C(抗坏血酸C₆H₈O₆)
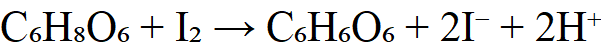
(二)间接碘量法(Na₂S₂O₃标准溶液)
3.标定Na₂S₂O₃溶液(用KIO₃;或K₂Cr₂O₇置换碘量法)
(1)KIO₃与过量KI在酸性介质中生成I₂
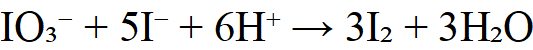
或K₂Cr₂O₇体系:
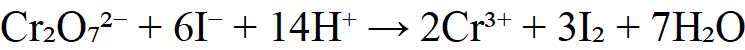
(2)生成的I₂用Na₂S₂O₃滴定
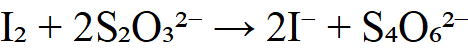
4.测定铜(Cu²⁺)
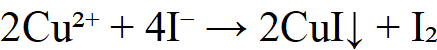
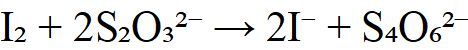
5.测定过氧化氢(H₂O₂)——间接法
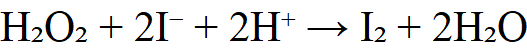
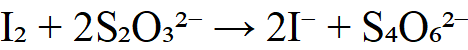
6.测定溶解氧(DO)—— Winkler 法(简化)
(1)Mn²⁺在碱性条件下被氧化为Mn(IV)氢氧化物
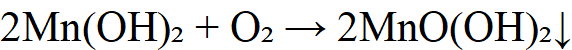
(2)酸化后MnO(OH)₂氧化I⁻生成I₂
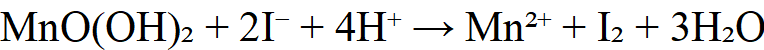
(3)I₂用Na₂S₂O₃滴定
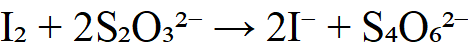

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
一、利用标准摩尔生成焓 例、已知:通常状态下,由最稳定的单...
【易错点01】弱电解质的判断有关的易错点 (1)在相同浓度、相同...
金属离子沉淀PH值表格(20℃) 金属离子浓度 10^-1 10^-2 10^-3 10^-4 1...
在高中化学的教学中,我们常常会将一些题目练习中总结出来的...
一.碱线 Fe(OH)3的溶度积,Ksp=[Fe3+][OH-]3,在直角坐标图中,[Fe...
沉淀转化不只看 K sp 大小!这些反应原理高中生必须掌握 在高中...