
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
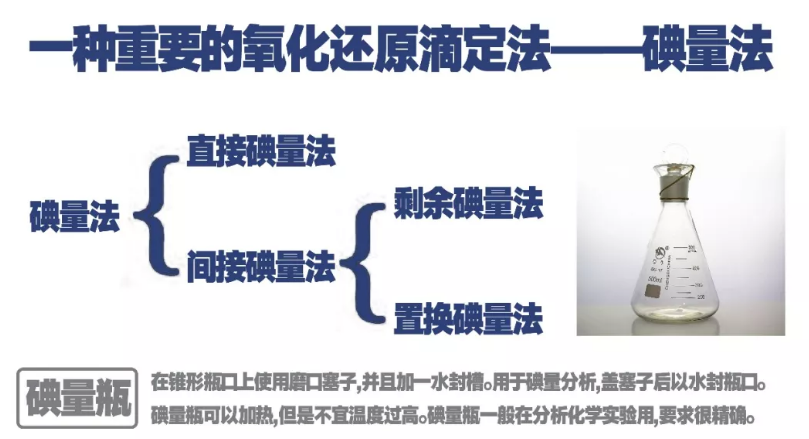
一、碘量法的基本原理
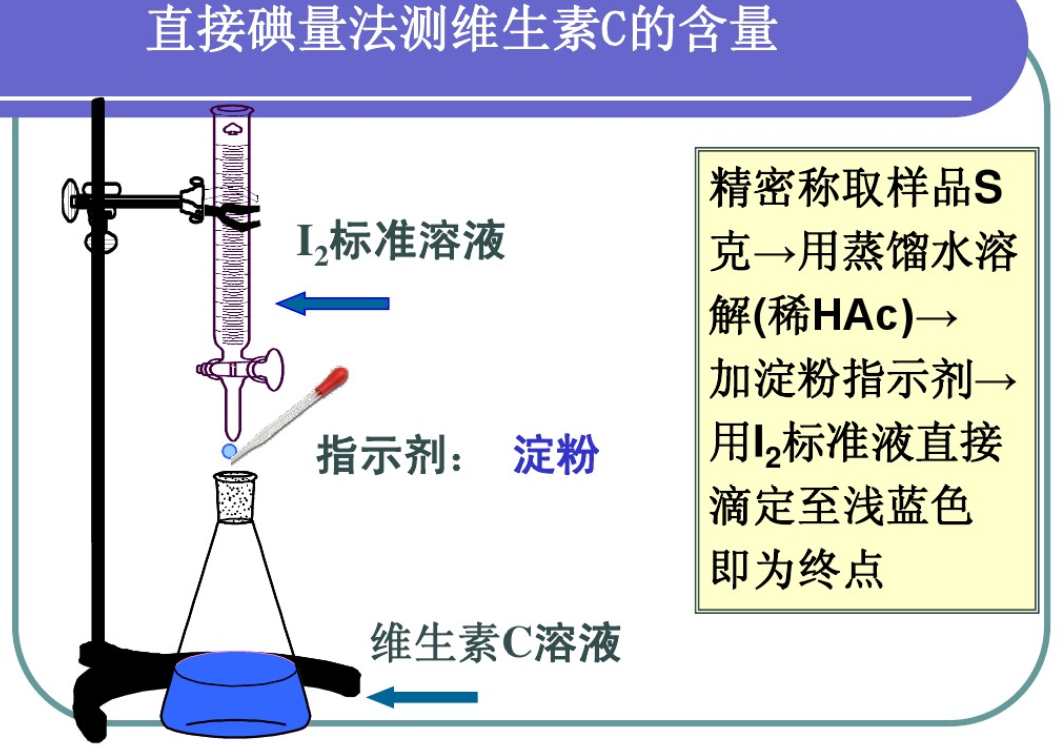
1、直接碘量法

直接碘量法是用碘滴定液直接滴定还原性物质的方法。在滴定过程中,I2被还原为I-:
![]()
直接碘量法只能在酸性、中性或弱碱性溶液中进行,如果溶液pH>9,可发生副反应使测定结果不准确。
直接碘量法可用淀粉指示剂指示终点。淀粉遇碘显蓝色,反应极为灵敏。化学计量点稍后,溶液中有过量的碘,碘与淀粉结合显蓝色而指示终点到达。
直接碘量法还可利用碘自身的颜色指示终点,化学计量点后,溶液中稍过量的碘显黄色而指示终点(但不灵敏)。


2、间接碘量法
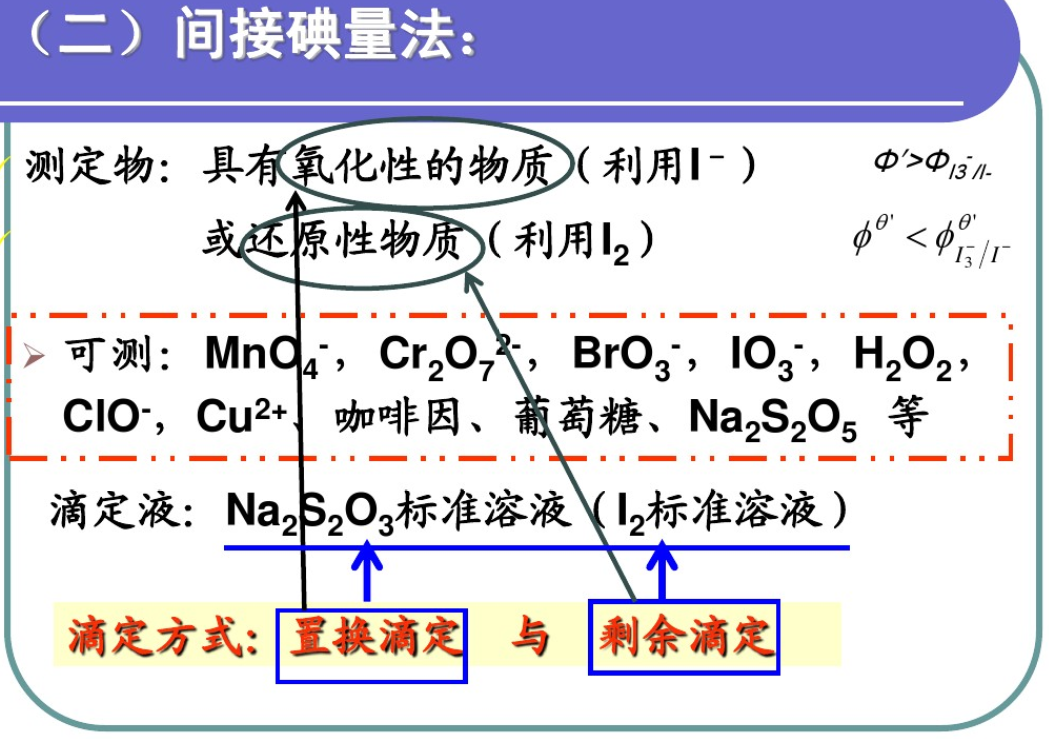





①剩余碘量法
剩余碘量法是在供试品(还原性物质)溶液中先加入定量、过量的碘滴定液,待I2与测定组分反应完全后,然后用硫代硫酸钠滴定液滴定剩余的碘,以求出待测组分含量的方法。滴定反应为:

使用剩余碘量法时,用淀粉作指示剂。淀粉指示剂应在近终点时加入,因为当溶液中有大量碘存在时,碘易吸附在淀粉表面,影响终点的正确判断。
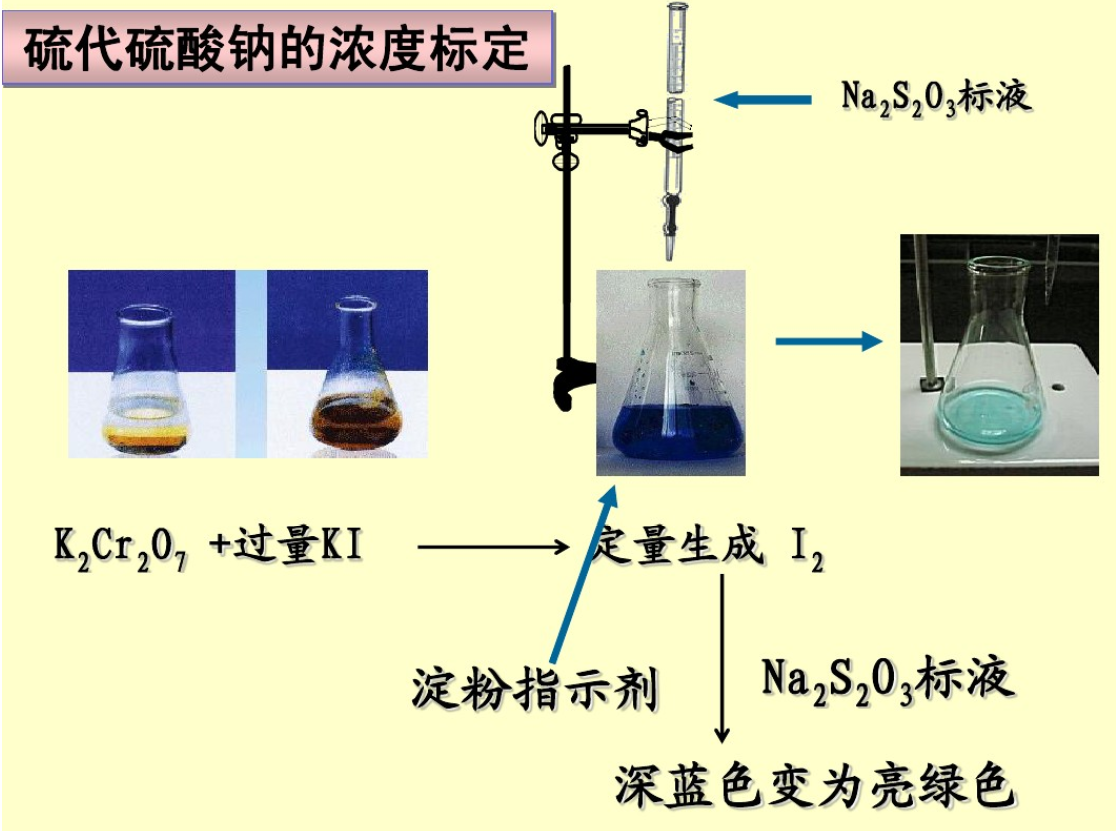
②置换碘量法
置换碘量法是先在供试品(氧化性物质)溶液中加入碘化钾,供试品将碘化钾氧化析出定量的碘,碘再用硫代硫酸钠滴定液滴定,从而可求出待测组分含量。滴定反应为:
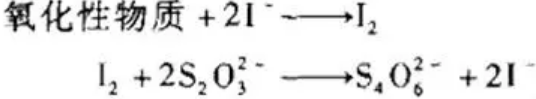
![]()




二、碘量法的应用



 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
【导读】化学界的“万能公式”亨德森-哈塞尔巴尔赫方程,就像...
一、先搞懂:Ksp到底是个啥? 很多同学一听到“溶度积常数”就...
在高中化学定量实验与高考考点中,碘量法是氧化还原滴定法里...
一、酸溶液的pH 强酸和弱酸的电离略有不同,下面我们分开阐述...
双指示剂法是一种利用两种具有不同变色范围的酸碱指示剂,在...
弱酸也可以制备强酸!!! 比如向 CuSO 4 溶液中加入 H 2 S 溶液生...