
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
平衡转化率=![]()
或:平衡转化率=![]()
平衡转化率=![]()
若要求某一时刻的转化率只要把平衡时的反应物浓度(或物质的量)改为某一时刻的反应物浓度(或物质的量)即可。
现将有关平衡转化率的问题小结如下:
1. 对有多种反应物的可逆反应达到平衡后加其一。这种情况不管状态如何均认为所加物本身转化率减小其它物质转化率增大
例1:![]() ,反应达到平衡后增大
,反应达到平衡后增大![]() 的浓度,则平衡向正反应方向移动,
的浓度,则平衡向正反应方向移动,![]() 的转化率增大,而
的转化率增大,而![]() 的转化率降低。
的转化率降低。
逆向运用:
例2.反应: 3A(g)+B(g) ![]() 3C(g)+2D(g)达到平衡后加入C求A的转化率
3C(g)+2D(g)达到平衡后加入C求A的转化率
分析:加入C促使D向A、B进一步转化故D向A、B转化的转化率增大而A、B向C、D转化的转化率减小。
2. 对只有一种反应物的可逆反应达到平衡后再加。
由于反应只有一种所以无论往反应物加多少量都可视为等比例增加反应物的用量,故认为有两种情况:
(1)恒温恒压:由于恒温恒压时等比例扩大或缩小反应物的用用量均与原平衡等效故转化率不变,各反应物和生成物的体积分数不变,各反应物和生成物物质量会跟原平衡相比,等比例增加,但浓度不变
(2)恒温恒容:此时可以看成反应叠加后,增大压强使平衡向气体总系数小方向移动,
例3.![]() ,反应达到平衡后,再向密闭容器中加入
,反应达到平衡后,再向密闭容器中加入![]() ,反应达到平衡时NO2、N2O4的物质的量(或物质的量浓度)均增大,颜色变深,NO2转化率增大。
,反应达到平衡时NO2、N2O4的物质的量(或物质的量浓度)均增大,颜色变深,NO2转化率增大。
分析:该反应可认为后加入NO2与原反应进行叠加,叠加后气体总体积增加,为了使体积维持不变,只能向体系加压从而引起叠加后的平衡向生成N2O4的方向移动。
逆向运用:
例4.![]() ,反应达到平衡后,再向密闭容器中加入N2O4,反应达到平衡时NO2、N2O4的物质的量(或物质的量浓度)均增大,颜色变深,N2O4向NO2转化的转化率减小。
,反应达到平衡后,再向密闭容器中加入N2O4,反应达到平衡时NO2、N2O4的物质的量(或物质的量浓度)均增大,颜色变深,N2O4向NO2转化的转化率减小。
分析:该反应可认为后加入NO2与原反应进行叠加,叠加后气体总体积增加(此时,NO2的量会比原来的多,)为了使体积维持不变,只能向体系加压从而引起叠加后的平衡向生成N2O4的方向移动。
例5. ![]() 反应达到平衡后,再向密闭容器中加入
反应达到平衡后,再向密闭容器中加入![]() ,达到平衡后,PCl3的物质的量会 ,(填“增加”还是“减少”)但是反应达到新的平衡时PCl5物质的量会 ,(填“增加”还是“减少”)
,达到平衡后,PCl3的物质的量会 ,(填“增加”还是“减少”)但是反应达到新的平衡时PCl5物质的量会 ,(填“增加”还是“减少”)![]() 的转化率 (填增大还是减小), PCl5在平衡混合物中的百分含量较原平衡时 ,(填“增加”还是“减少”)
的转化率 (填增大还是减小), PCl5在平衡混合物中的百分含量较原平衡时 ,(填“增加”还是“减少”)
答案:增加、增加、减小,增加
例6. ![]() 反应达到平衡后,再向密闭容器中加入HI,HI的平衡转化率 。H2的物质的量 ,I2的物质的量 。
反应达到平衡后,再向密闭容器中加入HI,HI的平衡转化率 。H2的物质的量 ,I2的物质的量 。
答案:不变,增加,增加
3. 对有多种反应物的可逆反应达到平衡时按等比例加入各种反应物。也有2种情况:
(1)恒温恒压:由于恒温恒压时等比例扩大或缩小反应物的用用量均与原平衡等效,故转化率不变,各反应物和生成物的体积分数不变,各反应物和生成物物质量会跟原平衡相比,等比例增加,但浓度不变。
(2)恒温恒容:此时可以看成反应叠加后,增大压强使平衡向气体总系数小方向移动。
例7.![]() 。在密闭容器中按
。在密闭容器中按![]() 的比例充入
的比例充入![]() 和
和![]() ,反应达到平衡后,若其它条件不变,再按
,反应达到平衡后,若其它条件不变,再按![]() 的比例充入
的比例充入![]() 和
和![]() ,反应重新达到平衡后,
,反应重新达到平衡后,![]() 和
和![]() 的平衡转化率都有等同程度的增大。即反应达到平衡后按物质的量的比例增大反应物浓度,达到新的化学平衡时,各反应物的转化率均有等同程度的增大。
的平衡转化率都有等同程度的增大。即反应达到平衡后按物质的量的比例增大反应物浓度,达到新的化学平衡时,各反应物的转化率均有等同程度的增大。
例8.![]() 。反应达到平衡后按比例增大反应物浓度,达到新的化学平衡时,各反应物的转化率均有等同程度的减小。
。反应达到平衡后按比例增大反应物浓度,达到新的化学平衡时,各反应物的转化率均有等同程度的减小。
总结:其实问题2、3都是等比例扩大或缩小反应物用量的问题,大家只要抓住这类问题的模型特征,便能轻松解决这类问题。
4.等温等压下对于有多种反应物的可逆反应达到平衡时不按比例加入各种反应物。一般先让加入量满足等,然后把多出来或少的看成是单独再加入减少的物质,利用问题一的办法来解决。(此类问题一般讨论恒温恒压)
例9.某温度下,在一容积可变的容器中,反应2A(g)+B(g)![]() 2C(g)达到平衡时,A、B、C的物质的量分别为4mol、2mol、4mol。保持温度和压强不变,平衡后再向体系中加各加入1molA和1molB
2C(g)达到平衡时,A、B、C的物质的量分别为4mol、2mol、4mol。保持温度和压强不变,平衡后再向体系中加各加入1molA和1molB
本题通过一边倒去后可得到原平衡的起始量为:
2A(g) + B(g)![]() 2C(g)
2C(g)
起始物质量/mol 8 4 0
加入1molA和1molB后起始物质量变为:
起始物质量/mol 9 5 0
所以我们可以把9molA和5molB看成先加9molA和4.5molB后满足等效(此时按问题3恒温恒压的情况来处理)后再单独加入0.5molB(此时可以再进一步按问题1处理)
特别注意:
1.解决这类问题一定要理解题型特征
2.要理解“等比例”所指的是与原平衡起始用量等比例,而不是与化学计量数等比例如
2A(g)+B(g)![]() 2C(g) 3种不同起始量是否等比例我们通过一边倒便很容易看出来
2C(g) 3种不同起始量是否等比例我们通过一边倒便很容易看出来
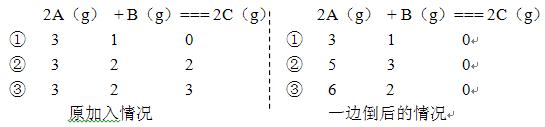
在上述3种加料中③与①是等比例,而②与①是不等例的。
例10.某温度下,在一容积可变的容器中,反应2A(g)+B(g)![]() 2C(g)达到平衡时,A、B、C的物质的量分别为4mol、2mol、4mol。保持温度和压强不变,平衡后再向体系中加各物质按下列情况加入平衡怎样移动?
2C(g)达到平衡时,A、B、C的物质的量分别为4mol、2mol、4mol。保持温度和压强不变,平衡后再向体系中加各物质按下列情况加入平衡怎样移动?
A.均加1mol, B.均减1mol

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
...
一、公式提出的背景 19世纪末,化学家们逐渐意识到温度对化学...
假设对于反应 a A(g) + b B(g) g G(g) + h H(g) 中各物质均为理想气体,...
例:某温度、起始压强为100 kPa下,若将2mol SO 2 和1molO 2 ,通入恒...
...
什么是活化能、能垒? 1 、能垒 活化分子含有的能参加化学反应...