
|
学习小专题 |

|
学习小专题 |
 [化学反应原理综合] 《化学反应原理》易忽略知识点 作者:化学自习室 来源:未知 日期:2019-05-16 15:32:05 点击:1418 所属专题:化学反应原理 易忽略知识点
[化学反应原理综合] 《化学反应原理》易忽略知识点 作者:化学自习室 来源:未知 日期:2019-05-16 15:32:05 点击:1418 所属专题:化学反应原理 易忽略知识点
绪言 1 P 3 一种分子要转变为另一种分子,首先应减弱或破坏分子原子间的化学键 2 P 3 右图中:E 1 是反应的活化能,E 2 是活化分子能量 变成生成物分子付出的能量,能量差 E 2 -E 1 是 反应热 3 P 4 活化能的作用在于促进反应物活化,从而启动 反应或改变反应速率 化学反应...
 [化学反应原理综合] 必修二易忽略知识点 作者:化学自习室 来源:未知 日期:2019-05-16 15:27:37 点击:1165 所属专题:必修二 易忽略知识点
[化学反应原理综合] 必修二易忽略知识点 作者:化学自习室 来源:未知 日期:2019-05-16 15:27:37 点击:1165 所属专题:必修二 易忽略知识点
16 P16 磷蒸气与氢气能反应 17 P17 金属性与非金属性无严格的分界线,分界线附近元素既有一定金属性又有非 金属性 1 P4 原子序数=核电荷数=质子数=核外电子数 2 P5 周期表有 18 个纵行,第 8、9、10 三个纵行叫做第 VIII 族 3 P5 最外层电子数为 8 的元素,化合价为 0,...
 [教育热点] “3+3”高考模式解读 作者:关平 来源:未知 日期:2017-09-22 16:46:01 点击:2120 所属专题:高考模式
[教育热点] “3+3”高考模式解读 作者:关平 来源:未知 日期:2017-09-22 16:46:01 点击:2120 所属专题:高考模式
9月起,北京、天津等第二批高考综合改革试点省(市、区)将进入高考综合改革实施阶段,新一届高一学生将会在3年后采用“3+3”的高考模式。 “3+3”模式中,普通高校招生录取的总成绩由统一高考的语文、数学、外语3个科目和考生自主选择的普通高中学业水平考试3个科目成绩组...
 [化学反应原理综合] 《化学反应原理》重要知识点记忆口诀 作者:关平 来源:未知 日期:2017-09-21 15:41:42 点击:1633 所属专题:化学反应原理
[化学反应原理综合] 《化学反应原理》重要知识点记忆口诀 作者:关平 来源:未知 日期:2017-09-21 15:41:42 点击:1633 所属专题:化学反应原理
1.化学反应热概念 化学反应伴能变,成键放出断需要。 左能高常是放热,置氢中和和燃烧。 炭水铵碱分解类,吸热自然右能高。 2.燃料燃烧知识理解 能源紧张,不久用光。 接触充分,空气足量。 节能减排,新能跟上。 高效清洁,来日方长。 3.化学反应速率概念理解 化学反应有快...
 [化学反应原理综合] 溶液中离子平衡之思维导图 作者:张超鹏 来源:未知 日期:2016-12-19 17:36:05 点击:5901 所属专题:电解质溶液
[化学反应原理综合] 溶液中离子平衡之思维导图 作者:张超鹏 来源:未知 日期:2016-12-19 17:36:05 点击:5901 所属专题:电解质溶液
...
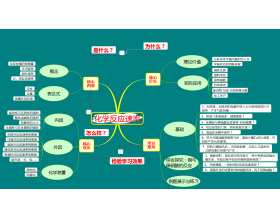 [化学反应原理综合] 化学反应速率之思维导图(复习提纲) 作者:刘小丹 来源:未知 日期:2016-12-19 17:49:54 点击:7813 所属专题:化学反应速率
[化学反应原理综合] 化学反应速率之思维导图(复习提纲) 作者:刘小丹 来源:未知 日期:2016-12-19 17:49:54 点击:7813 所属专题:化学反应速率
...
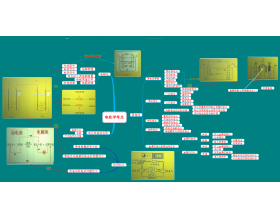 [化学反应原理综合] 电化学之思维导图 作者:毛远明 来源:未知 日期:2016-12-19 17:50:38 点击:6777 所属专题:电化学
[化学反应原理综合] 电化学之思维导图 作者:毛远明 来源:未知 日期:2016-12-19 17:50:38 点击:6777 所属专题:电化学
...
 [化学反应原理综合] 《化学反应原理》中的误区剖析 作者:王金玉 来源:未知 日期:2016-05-12 19:23:30 点击:978 所属专题:化学反应原理
[化学反应原理综合] 《化学反应原理》中的误区剖析 作者:王金玉 来源:未知 日期:2016-05-12 19:23:30 点击:978 所属专题:化学反应原理
第二页...
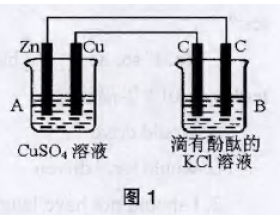 [注解与辨疑k] 电化学中值得思考的问题集 作者:黄叶 来源:未知 日期:2016-03-13 18:38:25 点击:1855 所属专题:电化学问题
[注解与辨疑k] 电化学中值得思考的问题集 作者:黄叶 来源:未知 日期:2016-03-13 18:38:25 点击:1855 所属专题:电化学问题
原电池和电解池是高中有关电化学知识的两 个基本装置,深人了解两种装置的形成条件,判断 依据和内部微粒的运动是解决各种电化学问题的基础,但在实际的教学过程中笔者也发现了一些值得思考的问题,与各位同行交流讨论。 一、非氧化还原反应不能设计成原电池? 非氧化还...
 [化学反应原理综合] 《化学反应原理》简要概括 作者:罗翊轩 来源:未知 日期:2015-12-27 16:43:42 点击:1006 所属专题:化学反应原理
[化学反应原理综合] 《化学反应原理》简要概括 作者:罗翊轩 来源:未知 日期:2015-12-27 16:43:42 点击:1006 所属专题:化学反应原理
一、知识主题 1.能量变化:反应热,热化学方程式,盖斯定律;原电池原理,电解原理。 2.反应快慢:有效碰撞理论,影响因素,平均反应速率。 3.化学平衡:平衡态的形成与特点,平衡的移动,平衡常数。 4.反应方向:放热和熵增有利于反应自发。 5.电解质溶液:电离理论,...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
在笔者的教学工作中,常常能听到一部分学生反馈自己基础比较...
一、氧化还原反应 (一)回扣要点知识 (二)辨析易混易错问...
1、 掌握一图(原子结构示意图)、五式(分子式、结构式、结构简...
1. 熔化状态下能导电的物质一定是电解质。 不一定,如金属单质...
一、原子结构与性质 (1)原子均由质子数、中子数和核外电子组成...
高中化学教材中,有一个平衡理论体系,包括 溶解平衡、化学平...
1、明矾净水的原理 规范解答:明矾溶于水电离出的Al 3+ 发生水...
(一)关于元素周期律(表)的6大误区 常见误区 出错原因 误认为最...