
|
ѧϰСר�� |

|
ѧϰСר�� |
 [ע�������j] ���ָʾ���ı�ɫԭ�� ����:���� ��Դ: ���ڣ�2007-09-29 08:55:21 �����17325 ����ר�⣺���ָʾ��
[ע�������j] ���ָʾ���ı�ɫԭ�� ����:���� ��Դ: ���ڣ�2007-09-29 08:55:21 �����17325 ����ר�⣺���ָʾ��
ʯ��ͷ�̪�������ָʾ����������һ�������л��ᡣ����Һ�������Һ����Եı仯��ָʾ���ķ��ӽṹ�����仯����ʾ����ͬ����ɫ�� ʯ��(��Ҫ�ɷ���HL��ʾ)��ˮ��Һ���ܷ������µ��룺 ��������Һ���ɫ�ķ����Ǵ��ڵ���Ҫ��ʽ����Һ�Ժ�ɫ���ڼ�����Һ�������...
 [ע�������j] ��Щ���ʲ��ܻ�ʩ ����:����ӱ ��Դ: ���ڣ�2007-09-20 12:54:50 �����8289 ����ר�⣺����
[ע�������j] ��Щ���ʲ��ܻ�ʩ ����:����ӱ ��Դ: ���ڣ�2007-09-20 12:54:50 �����8289 ����ר�⣺����
��Щ����Ӧ����ʩ�ã����ܻ�ϣ�����ή�ͷ�Ч������ʧЧ�� ������Ʋ������ľ�ҡ�ʯ�ҵ���ʯ�ҵȼ��Է��ϻ����������ƺ��������ᣬ�����Է�Ӧ�����������Է��Ϻ����ʽ϶࣬�������ʩ�ã���������Ӧ�����ͷ�Ч���ֻ�ʹ�ƹ̶����أ��������ܾ��ˡ���ۡ���...
 [ע�������j] ����� ����:������ ��Դ: ���ڣ�2007-09-11 13:58:15 �����7966 ����ר�⣺�����
[ע�������j] ����� ����:������ ��Դ: ���ڣ�2007-09-11 13:58:15 �����7966 ����ר�⣺�����
���ᡢ��������������ˮ��Һ�д��ڵ���ƽ�⡣���磺 ���ﵽ����ƽ��ʱ�����������Һ�������Ũ�ȱ���һ�������ô�ʱ����Ũ�ȵĸߵͺ���������ʵ����ǿ�������ڵĵ���Ⱦ��Ƕ��������������ǿ������Ҫ��� 1 ��ȷ�������ȵĸ��� �������������Һ��ﵽ����...
 [ע�������j] pH��ͬ�����Ϻ�pH������? ����:�¹��� ��Դ: ���ڣ�2016-02-02 19:36:04 �����7247 ����ר�⣺ph����
[ע�������j] pH��ͬ�����Ϻ�pH������? ����:�¹��� ��Դ: ���ڣ�2016-02-02 19:36:04 �����7247 ����ר�⣺ph����
��Ŀ ����pH=3��HCl��pH=3��CH 3 COOH��������ʱ��������Һ��pH�ǣ� �� A. 3 B. 4 C.С��3 D.����3 һ�������Դ �˽̰滯ѧ��������������ѡ�ޣ��ڶ���p78ѡ�����2�⣺���������У�����10mLHCl��Һʱ����pH����ı�ĵ��ǣ� �� A. 20mLͬһŨ�ȵ�HCl��Һ B. 20...
 [ע�������j] ˮ��Һ��Ϊ�β�����̼������ ����:���� ��Դ: ���ڣ�2007-07-21 02:32:57 �����9029 ����ר�⣺̼���� ˫ˮ�ⷴӦ
[ע�������j] ˮ��Һ��Ϊ�β�����̼������ ����:���� ��Դ: ���ڣ�2007-07-21 02:32:57 �����9029 ����ר�⣺̼���� ˫ˮ�ⷴӦ
�ҹ����и���ѧ��ѧ�̿����е��ᡢ������ܽ��Ա�����̼����(��)������ˮ�ij���ˮ�в����ڡ���������Fe(H 2 O) 6 3+ ��Fe 3+ �ĵ�ɶ࣬�뾶С����ɵ�ƽ����뾶֮��ֵ��(Z 2 /r=3515c 2 m -1 1028)���������ļ�������ǿ����Fe(H 2 O) 6 3+ �У�Fe 3+ ����λ�ļ���H...
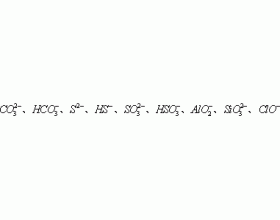 [ע�������j] ��η�����������Һ��ˮ����� ����:������ ��Դ: ���ڣ�2016-02-02 21:48:42 �����5790 ����ר�⣺˫ˮ�ⷴӦ
[ע�������j] ��η�����������Һ��ˮ����� ����:������ ��Դ: ���ڣ�2016-02-02 21:48:42 �����5790 ����ר�⣺˫ˮ�ⷴӦ
һ����˵����������ˮ�����Һ�������෴�����Ի���ԣ�ʱ��Ӧ��ˮ����ٽ��ĽǶȿ��ǣ����ⲻ��һ�Ŷ��ۣ����������Ӧ������������ܽ����£� һ . ��Ҫ������ˮ������ 1. ����ˮ�������෴���Σ�Ӧ�����ε�ˮ�� �����������ˮ�����Һ�����ԣ������������ˮ��...
 [ע�������j] ���ڡ����������ҺԽϡ������̶�Խ�ļ��ֽ��ͷ��� ����:�¹��� ��Դ: ���ڣ�2007-05-14 14:32:18 �����11554 ����ר�⣺��Һϡ�� ����� ����ƽ��
[ע�������j] ���ڡ����������ҺԽϡ������̶�Խ�ļ��ֽ��ͷ��� ����:�¹��� ��Դ: ���ڣ�2007-05-14 14:32:18 �����11554 ����ר�⣺��Һϡ�� ����� ����ƽ��
1 ������Ч��ײ���۽��� �������������������£���һ��Ũ�ȵ����������Һ�м�ˮ������ˮ���������࣬ʹ��������ʵ��������֮��ľ����������Ӽ����ײ��ϳɷ��ӵĻ����С����λʱ�������Ӽ����Ч��ײ�������١����⣬������ʷ��������ܵ����Է��ӵ����ã�...
 [ע�������j] ���λ�ϲ�����ˮ������� ����:�쿵 ��Դ: ���ڣ�2016-02-02 21:51:56 �����2456 ����ר�⣺˫ˮ�ⷴӦ
[ע�������j] ���λ�ϲ�����ˮ������� ����:�쿵 ��Դ: ���ڣ�2016-02-02 21:51:56 �����2456 ����ר�⣺˫ˮ�ⷴӦ
�� 1 ����������Һ���ʣ����Ի���ԣ���ͬʱ��������ʽ�����Ӵ��ڣ������ܷ�����Ӧ����������ʱ������ˮ�⡣�� Pb(NO 3 ) 2 �� CuSO 4 �� Na 2 CO 3 �� BaS �� ZnCl 2 �� AgNO 3 ��������������ˮ�����ƣ������ڸ��ֽⷴӦ���Ƹ��ʲ�����ˮ�⡣ �� 2 �������ηֱ�...
 [ע�������j] ̼����������ͭ��Һ��Ӧ ����:��ʤ ��Դ: ���ڣ�2016-02-02 21:50:46 �����5087 ����ר�⣺̼���� ����ͭ ˫ˮ�ⷴӦ
[ע�������j] ̼����������ͭ��Һ��Ӧ ����:��ʤ ��Դ: ���ڣ�2016-02-02 21:50:46 �����5087 ����ר�⣺̼���� ����ͭ ˫ˮ�ⷴӦ
2Cu 2+ + 2CO 3 2- + H 2 O ==== Cu 2 ��OH�� 2 CO 3 �������� + CO 2 �����壩...
 [ע�������j] ��þ�������Һ��Ӧ����ʶ���� ����:��� ��Դ: ���ڣ�2016-02-02 21:54:47 �����9834 ����ר�⣺þ ��� ����ˮ�����
[ע�������j] ��þ�������Һ��Ӧ����ʶ���� ����:��� ��Դ: ���ڣ�2016-02-02 21:54:47 �����9834 ����ר�⣺þ ��� ����ˮ�����
����þ�����������߾��ǽϻ��õĽ��������䱾�������е�����������������ȫ��������ˮ�����û���Ӧ�ų�������EAl 3+ /Al=-2.375V��EMg 2+ /Mg=-1.67V��EH 2 O/H 2 =-0.414V��������ʵ�ϣ���ͨ�������£�þ��������ˮ��Ӧ����ԭ������Ϊ��þ����ˮ��Ӧ��������...
 ��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ�
��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ� ��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء�
��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء���ѧ�����ʡ� �̲���������ʵ�飬һ���� AgI ת��Ϊ Ag 2 S��һ���� Mg(OH) 2 ת��Ϊ ...
25 �� ʱ�� K a1 (H 2 S)=1.1 �� 10 -7 �� K a2 (H 2 S)=1.3 �� 10 -13 . ���ߵȽ���...
����ת���dz����ܽ�ƽ���Ӧ��֮һ�� �����ܶȻ��ϴ�ij���תΪ�ܶȻ���С�ij�������...
1.ʵ�� �����£���0.100 0 mol��L ��1 NaOH��Һ�ζ�20.00 mL 0.100 0 mol��L ��1 CH 3...
������֣�pH=5��ϡ�����ˮ��ϡ1000����ϡ�ͺ���Һ��pH=����ͨ������˵���� ���⣺��...
��Ԫ�����Ƿֲ�����ģ����Ե�һ������Ϊ�����������볣�����٣������ܴ� ��...
���ɽ������ж�������������Ϊ�����d���ӿ��Բ��ֻ���ȫ������ɼ��������������...
�ʣ�Ϊʲôǿ���ڱ������п��ԱȽϳ�������ǿ���� ��Ҫ�ش�������⣬���ǵûص����...