
|
学习小专题 |

|
学习小专题 |
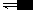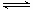 [注解与辨疑i] 有气体参加(或生成)的平衡体系中, 再充入气体对平衡的影响分析 作者:化学自习室 来源:未知 日期:2019-06-26 10:00:58 点击:2425 所属专题:惰性气体影响
[注解与辨疑i] 有气体参加(或生成)的平衡体系中, 再充入气体对平衡的影响分析 作者:化学自习室 来源:未知 日期:2019-06-26 10:00:58 点击:2425 所属专题:惰性气体影响
1.加入与反应相关的气体 (1)在容积恒定的密闭容器中,反应已达平衡,此时只要充入反应体系中任何一种气体,也就是改变反应体系中任何一种气体的浓度, 平衡都会发生移动.平衡移动的方向应从浓度对平衡的影响来判断,而不应从压强的影响去判断. 例如:2SO 2 (g)+O 2 (g) 2SO...
 [注解与辨疑i] 等体积反应,化学平衡发生移动时压强是否一定不变? 作者:化学自习室 来源:未知 日期:2019-06-26 09:57:51 点击:1797 所属专题:平衡移动量变
[注解与辨疑i] 等体积反应,化学平衡发生移动时压强是否一定不变? 作者:化学自习室 来源:未知 日期:2019-06-26 09:57:51 点击:1797 所属专题:平衡移动量变
通常情况下压强对化学平衡的影响是指反应在体系内外可进行能量传递的容器中进行的,在这一前提下的等体反应,压强保持恒定时,不能作为判断化学平衡的标志,化学平衡发生移动时压强也保持恒定. 但如果反应是在一个体积不变的绝热容器中的等体反应,压强保持恒定时,可作为判断化学...
 [注解与辨疑i] 平均相对分子质量或压强不变,可逆反应是否平衡状态? 作者:化学自习室 来源:未知 日期:2019-06-26 09:54:34 点击:2342 所属专题:平衡状态 平均分子量
[注解与辨疑i] 平均相对分子质量或压强不变,可逆反应是否平衡状态? 作者:化学自习室 来源:未知 日期:2019-06-26 09:54:34 点击:2342 所属专题:平衡状态 平均分子量
一定条件下的可逆反应,当平均相对分子质量或压强不再变化时,该反应是否已经达到平衡状态,要根据具体反应进行具体分析. 现以反应mA(g)+nB(g) pC(g)+qD(g)(己知该反应的正反应为放热反应)为例,分析如下: (1)平均相对分子质量 ①若m+n≠ p+q:混合气体的平均相对分子质量发生变...
 [注解与辨疑i] 巧用吉布斯自由能化解判断化学反应的方向的疑难问题 作者:化学自习室 来源:未知 日期:2019-06-12 10:24:02 点击:7377 所属专题:反应方向
[注解与辨疑i] 巧用吉布斯自由能化解判断化学反应的方向的疑难问题 作者:化学自习室 来源:未知 日期:2019-06-12 10:24:02 点击:7377 所属专题:反应方向
一、从实践提出问题 化学反应体系趋于高能态向低能态转化。对于放热反应来说。是从高能向低能转变。故是一种自发进行的趋势。所以一般放热反应具有自发性.即Δ H <0自发倾向大,Δ H >0非自发倾向大。 虽然几乎所有的焓变小于零的放热反应都是自发的。但是有不少的焓变大...
 [注解与辨疑i] 平衡等效,则转化率、物质的量、物质的量分数如何比较? 作者:化学自习室 来源:未知 日期:2019-05-11 18:11:23 点击:3861 所属专题:等效平衡 转化率
[注解与辨疑i] 平衡等效,则转化率、物质的量、物质的量分数如何比较? 作者:化学自习室 来源:未知 日期:2019-05-11 18:11:23 点击:3861 所属专题:等效平衡 转化率
三类等效平衡的比较: 等效类型 I II III 条件 恒温、恒容 恒温、恒容 恒温、恒压 起始投料特征 换算为方程式同一半边物质后,其 “ 量 ” 相同 换算为方程式同一边物质后,其 “ 量 ” 符合同一比例 换算为方程式同一边物质后,其 “ 量 ” 符合同一比例 对反应的要求 任何...
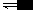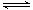 [注解与辨疑i] 充入气体化学平衡移动方向和转化率或百分数变化的问题 作者:化学自习室 来源:未知 日期:2019-05-11 18:10:45 点击:8543 所属专题:转化率 惰性气体影响
[注解与辨疑i] 充入气体化学平衡移动方向和转化率或百分数变化的问题 作者:化学自习室 来源:未知 日期:2019-05-11 18:10:45 点击:8543 所属专题:转化率 惰性气体影响
(一)充入气体化学平衡移动方向的问题 1、充入惰性气体情况 1.1恒温恒容下,达到平衡后再充入惰性气体(或不参与反应的气体)时,反应体系内压强虽然增大,但各反应气体的分压没有变,浓度没有改变,所以正反应速率没有改变,故平衡不移动。 1.2恒温恒压下,达到平衡后...
 [注解与辨疑i] 转化率与体积分数分析 作者:化学自习室 来源:未知 日期:2018-11-23 15:18:11 点击:2195 所属专题:转化率 体积分数
[注解与辨疑i] 转化率与体积分数分析 作者:化学自习室 来源:未知 日期:2018-11-23 15:18:11 点击:2195 所属专题:转化率 体积分数
在mA(g)+nB(g)pC(g)+qD(g)中,从反应物开始反应,达到平衡时: 1.反应物投入比的影响 (1)n(A) : n(B)=m : n时: α(A) = α(B),φ(A) : φ(B) =m :n ,φ(C)、φ(D) 最大 ; (2)n(A) : n(B)>m : n时: α(A) < α(B),φ(A) : φ(B) >m :n ,φ(C)、...
 [注解与辨疑i] 充入A,A的转化率真的减小吗? 作者:陈达 来源:未知 日期:2018-10-06 09:48:26 点击:1528 所属专题:转化率
[注解与辨疑i] 充入A,A的转化率真的减小吗? 作者:陈达 来源:未知 日期:2018-10-06 09:48:26 点击:1528 所属专题:转化率
下面以一计算结果分析, N 2 (g)+ 3H 2 (g) 2NH 3 (g), 某温度下,平衡常数K=5.7×10 -4 ,假设体积恒容为1 L,求得不同投料时转化率如下: 投料 容器 体积 转化率 N 2 (mol) H 2 (mol) N 2 (%) H 2 (%) 1 3 1 L 5.54 5.54 1 4 1 L 8.30 6.23 1 8 1 L 21.2 7.94 1 15...
 [注解与辨疑i] 勒沙特列原理应用中的易错点剖析 作者:关平 来源:未知 日期:2017-10-09 16:16:55 点击:1378 所属专题:勒沙特列原理盲区
[注解与辨疑i] 勒沙特列原理应用中的易错点剖析 作者:关平 来源:未知 日期:2017-10-09 16:16:55 点击:1378 所属专题:勒沙特列原理盲区
...
 [注解与辨疑i] 催化剂的系列问题集答疑 作者:关平 来源:未知 日期:2017-09-19 21:13:33 点击:920 所属专题:催化剂
[注解与辨疑i] 催化剂的系列问题集答疑 作者:关平 来源:未知 日期:2017-09-19 21:13:33 点击:920 所属专题:催化剂
1 、 化 学 反 应 没 有 催 化 剂 就 不 能 发 生 吗 催 化 剂 不 是 化 学 反 应 的 必 要 条 件 , 它 只 改 变 化 学 反 应 的 速 率 , 而 不 能 决 定 能 否 发 生 化 学 反 应 。 如 没 有 催 化 剂 , 将 过 氧 化 氢 加 热 也 能 反 应 放 出 氧 气 。 (马上点...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。在化学平衡的学习中,压强对气体平衡的影响与水溶液中“越稀越电离、越稀越水解”的规...
在化学动力学研究中,基元反应是理解反应机理的 “最小单元”,而反应速率方程则是描...
在多重平衡体系中,各物质在达到平衡状态时的浓度。多重平衡体系是指一个化学反应体系...
催化反应的核心始于吸附机理――分子通过物理吸附(范德华力)或化学吸附(化学键重组...
武汉市九月调考试题 解析 一般来说,有几个 过渡态就有几个基元反应。 那么吸附或脱附...
在化学热力学中,吉布斯自由能变(ΔG)是判断反应自发性的核心判据,其核心规律 “Δ...
核心思想: 多、快、好、省, 四大关键条件的分析与调控 1. 温度 (Temperature) ・ 热...
在化学反应动力学与热力学研究中,多平衡系统是一类普遍存在的复杂反应体系。明确其定...