
|
学习小专题 |

|
学习小专题 |
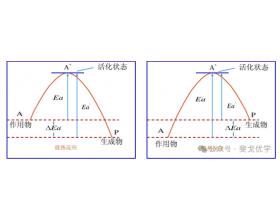 [注解与辨疑h] 化学反应原理中热力学与动力学的区别和联系是什么? 作者:化学自习室 来源:未知 日期:2025-01-10 09:27:47 点击:782 所属专题:热力学
[注解与辨疑h] 化学反应原理中热力学与动力学的区别和联系是什么? 作者:化学自习室 来源:未知 日期:2025-01-10 09:27:47 点击:782 所属专题:热力学
化学反应热力学和动力学的区别与联系如下: 一、热力学和动力学区别 1. 研究对象 热力学 主要研究化学反应中的能量变化,包括反应热、焓变、熵变、自由能变等,以及反应的方向和限度,判断反应能否自发进行及进行的程度,关注反应的始态和终态,不涉及反应过程. 动力学 ...
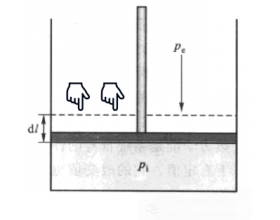 [注解与辨疑h] 焓变△H就是反应热吗? 作者:化学自习室 来源:未知 日期:2024-09-21 17:48:07 点击:306 所属专题:焓变 反应热
[注解与辨疑h] 焓变△H就是反应热吗? 作者:化学自习室 来源:未知 日期:2024-09-21 17:48:07 点击:306 所属专题:焓变 反应热
能量多种多样,通常来说,体系的总能量包括整体运动的动能、外力场中的位能、热力学能。如果假定体系是静止的且无特殊外力场存在,此时体系就只需要考虑热力学能,即内能U。 热力学能是指体系内分子运动的平动能、转动能、振动能、电子及核的能量,以及分子与分子相互作...
 [注解与辨疑h] 有关化学反应与热能中的易错点 作者:化学自习室 来源:未知 日期:2024-04-23 10:55:53 点击:212 所属专题:化学反应与热能
[注解与辨疑h] 有关化学反应与热能中的易错点 作者:化学自习室 来源:未知 日期:2024-04-23 10:55:53 点击:212 所属专题:化学反应与热能
1.放热反应不一定在常温下就能反应,吸热反应在常温下也可能发生反应,如NH 4 Cl(s)与Ba(OH) 2 ・8H 2 O的反应就是吸热反应,在常温下就能反应。 2.不能根据反应条件判断反应是放热还是吸热,需要加热才能进行的反应不一定是吸热反应,不需要加热就能进行的反应也不一定是放...
 [注解与辨疑h] 关于化学能,几点释疑 作者:王笃年 来源:未知 日期:2024-03-26 11:20:06 点击:204 所属专题:化学能
[注解与辨疑h] 关于化学能,几点释疑 作者:王笃年 来源:未知 日期:2024-03-26 11:20:06 点击:204 所属专题:化学能
1.焓是什么?与什么因素有关?物质的具体焓值是否可测? 焓(符号H)是一个很难说清楚其含义的化学量,它是在讨论恒压体系发生变化的过程中,为说明系统热效应的本质含义而引入的关于物质状态的一个函数(恒容过程则不需要用Δ H 表达,恒容过程的热效应就是体系内能变化值):...
 [注解与辨疑h] 加热或高温的反应一定吸热吗? 作者:刘凯 来源:未知 日期:2023-02-22 18:31:37 点击:399 所属专题:吸热反应
[注解与辨疑h] 加热或高温的反应一定吸热吗? 作者:刘凯 来源:未知 日期:2023-02-22 18:31:37 点击:399 所属专题:吸热反应
...
 [注解与辨疑h] 中和热与燃烧热概念辨析 作者:化学自习室 来源:未知 日期:2022-07-30 17:14:22 点击:2733 所属专题:中和热 燃烧热
[注解与辨疑h] 中和热与燃烧热概念辨析 作者:化学自习室 来源:未知 日期:2022-07-30 17:14:22 点击:2733 所属专题:中和热 燃烧热
反应热 当化学反应在一定温度下进行时,反应所释放或吸收的热量称为该反应此温度下的热效应,简称反应热。任何化学反应都有反应热。燃烧热和中和热是反应热的种类之一。 01 中和热 (1)定义 在稀溶液中,酸跟碱发生中和反应,生成 1mol 液态水所放出的热量叫作中和热。...
 [注解与辨疑h] 高中化学之反应进度解读 作者:化学自习室 来源:未知 日期:2022-01-03 11:26:59 点击:2756 所属专题:反应进度
[注解与辨疑h] 高中化学之反应进度解读 作者:化学自习室 来源:未知 日期:2022-01-03 11:26:59 点击:2756 所属专题:反应进度
高中热化学中的反应进度: 化学反应的焓变:化学反应过程中所释放或吸收的能量,都可以热量(或转换成相应的热量)来表示,称为焓变(Δ H ),单位:kJ/mol或kJmol-1。 燃烧热:在101KPa时,1mol 物质完全燃烧生成稳定的氧化物时所放出的热量,叫做该物质的燃烧热。燃烧热...
 [注解与辨疑h] 关于化学反应与热能的几个重要概念 作者:化学自习室 来源:未知 日期:2021-11-12 10:48:28 点击:811 所属专题:化学反应与热能
[注解与辨疑h] 关于化学反应与热能的几个重要概念 作者:化学自习室 来源:未知 日期:2021-11-12 10:48:28 点击:811 所属专题:化学反应与热能
1、焓是什么?与什么因素有关?物质的具体焓值是否可测? 焓(符号H)是一个很难说清楚其含义的化学量,它是在讨论恒压体系发生变化的过程中,为说明系统热效应的本质含义而引入的关于物质状态的一个函数(恒容过程则不需要用Δ H 表达,恒容过程的热效应就是体系热力学能变化...
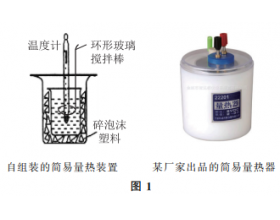 [注解与辨疑h] 关于中和热测定实验的问题讨论 作者:王笃年 来源:未知 日期:2021-11-02 14:14:53 点击:2310 所属专题:中和热测定
[注解与辨疑h] 关于中和热测定实验的问题讨论 作者:王笃年 来源:未知 日期:2021-11-02 14:14:53 点击:2310 所属专题:中和热测定
中学化学里一般使用简易量热器(图1)粗略地测定强酸、强碱发生中和反应时的热效应,关于教科书给出的药品(种类、浓度、体积)选择、实验操作要点,学生存有一些疑问。 1、计算中和热过程中,采取了那么多的近似,如认为混合溶液的密度为1g・cm -3 、溶液的比热容直接使用水的...
 [注解与辨疑h] 如何理解反应热与焓变的单位? 作者:化学自习室 来源:未知 日期:2021-09-13 14:41:38 点击:890 所属专题:反应热 焓变 反应进度
[注解与辨疑h] 如何理解反应热与焓变的单位? 作者:化学自习室 来源:未知 日期:2021-09-13 14:41:38 点击:890 所属专题:反应热 焓变 反应进度
在依据化学课程标准编写的中学化学教材中,通常都会有下列热化学方 程式: 2H 2 (g) + O 2 (g) =2H 2 O(1) Δ H =-571. 1 kJ mol -1 H 2 (g)++O 2 (g)= H 2 O(1) Δ H =-285. 8 kJ mol -1 在化学教学中,学生们常常会产生下列困惑:在热化学方程式中,Δ H 的单位...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。化学反应热力学和动力学的区别与联系如下: 一、热力学和动力学区别 1. 研究对象 热力...
一、概念梳理 中和热是指在稀溶液中,酸与碱发生中和反应生成1 mol 水时的反 应热.在2...
1.焓是什么?与什么因素有关?物质的具体焓值是否可测? 焓(符号H)是一个很难说清楚其...
...
第一阶段:离子反应发生的条件是要有沉淀、气体、水生成; 第二阶段:离子反应发生的...
反应热 当化学反应在一定温度下进行时,反应所释放或吸收的热量称为该反应此温度下的...
高中热化学中的反应进度: 化学反应的焓变:化学反应过程中所释放或吸收的能量,都可...
1、焓是什么?与什么因素有关?物质的具体焓值是否可测? 焓(符号H)是一个很难说清楚...