
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
AgCl是一种难溶于水的白色沉淀,每100g H2O中可以溶解1.35×10-4g AgCl,因此常利用Cl-与Ag+生成AgCl沉淀反应去检出Ag+或Cl-。AgCl既不溶于强酸,也不溶于强碱,却易溶于氨水,这是因为Ag+和NH3可以形成可溶性的[Ag(NH3)2]+:
AgCl+2NH3·H2O ![]() [Ag(NH3)2]++Cl-+2H2O
[Ag(NH3)2]++Cl-+2H2O
[Ag(NH3)2]+叫银氨络离子或配离子,其中Ag+和NH3用配位键相结合,这类化合物叫配位化合物,简称配合物,也叫络合物。周期表里d区和f区金属元素都容易形成配合物,特别是金属和有机分子形成的配位化合物,普遍存在于各种体系中。生物化学、催化、分析化学等领域都在广泛研究各类配位化合物的合成、结构和性质。配位化合物有何特征?配位键与共价键有何异同?
配位化合物是一类比较复杂的分子间化合物,其中含有一个复杂离子,它是一个稳定的结构单元,可以存在于晶体中,也可以存在于溶液中,可以是正离子,也可以是负离子。例如:
CuSO4+4NH3![]() [Cu(NH3)4]SO4
[Cu(NH3)4]SO4![]() [Cu(NH3)4]2++SO42-
[Cu(NH3)4]2++SO42-
3NaF+AlF3![]() Na3[AlF6]
Na3[AlF6] ![]() 3Na++[AlF6]3-
3Na++[AlF6]3-
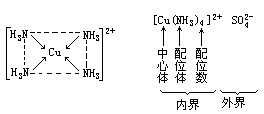
在[Cu(NH3)4]2+中的4个NH3分子位于同一平面上,以正四边形的方位与Cu2+结合,其中Cu2+位于四边形的中心位置,叫中心体;NH3分子位于四边形的顶角,叫配位体;有4个NH3与Cu2+相配,因此Cu2+的配位数为4;整个离子叫内界,用方括号括在一起;SO42-则为外界。
Cu2+和NH3之间的结合力与共价键略有不同,叫配位键,现以此为例说明配位键的本质。基态Cu的外层电子结构是3d104s1,失电子成Cu2+后为3d9,其中有1个3d电子被激发到4p轨道之后,能量相近的1个3d,1个4s和2个4p轨道杂化形成4个能量相等的dsp2杂化轨道,这是4个空轨道。
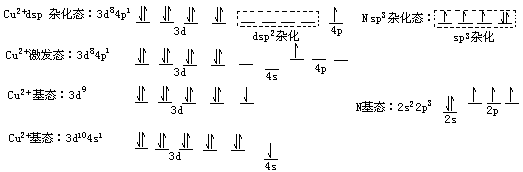
NH3分子中N原子的4个sp3杂化轨道上有3个未成对电子,可以和3个H形成N-H键,此外还有一对未成键的孤对电子,它们恰好与Cu2+的dsp2杂化空轨道相结合形成配位键。Cu与N之间也共用了一对电子,但这对电子是由N提供的,而Cu则提供了空轨道,我们用N→Cu表示,箭头指向具有空轨道的原子,以便与共价键的短线区别。总之,一个原子有杂化空轨道,另一个原子有孤对电子,两者可结合,借这类结合形成的化学键称为配位键。
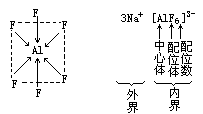
[AlF6]3-中的情况也差不多。Al是中心体,F-是配位体,配位数为6,内界带负电荷,配离子为负3价,外界是3个Na+。[AlF6]3-为正八面体结构,Al位于八面体中心,6个F-位于八面体的顶点,这6个F→Al配位键是等长的,其中4个F-位于同一平面正四边形的顶角,另外2个分别位于四边形的上方与下方,这6个F-形成的八面犹如一个网兜将Al3+装在八面体的中心。这类化合物形象地也叫络合物,“络”字的含义就是指网络或网袋的意思。
d区元素和f区元素有足够的d轨道和能量相近的s轨道、p轨道进行杂化,提供若干空轨道;多种负离子或中性分子(可以是简单的无机分子,也可以是很复杂的的有机分子)中有未成键的孤对电子,这两类原子容易以配位键相结合形成配位化合物。这类化合物品种繁多,结构复杂,用途广泛,是现代无机化学的重要研究领域。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
...
孤对电子,英文名:unshared pair electrons;lone pair electrons分子中除...
今天整理完整版氢键核心笔记,概念、形成、分类、性质影响一...
提到化学,我们最先想到的往往是化学键断裂与重组的化学反应...
一、概念与本质类易错点 •易错1:混淆氢键与化学键——氢键...
高中化学物质结构板块里,配位键和配位化合物一直是高频考点...