
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
【导读】HN₃是弱酸,酸性强于醋酸,极不稳定并且危险。
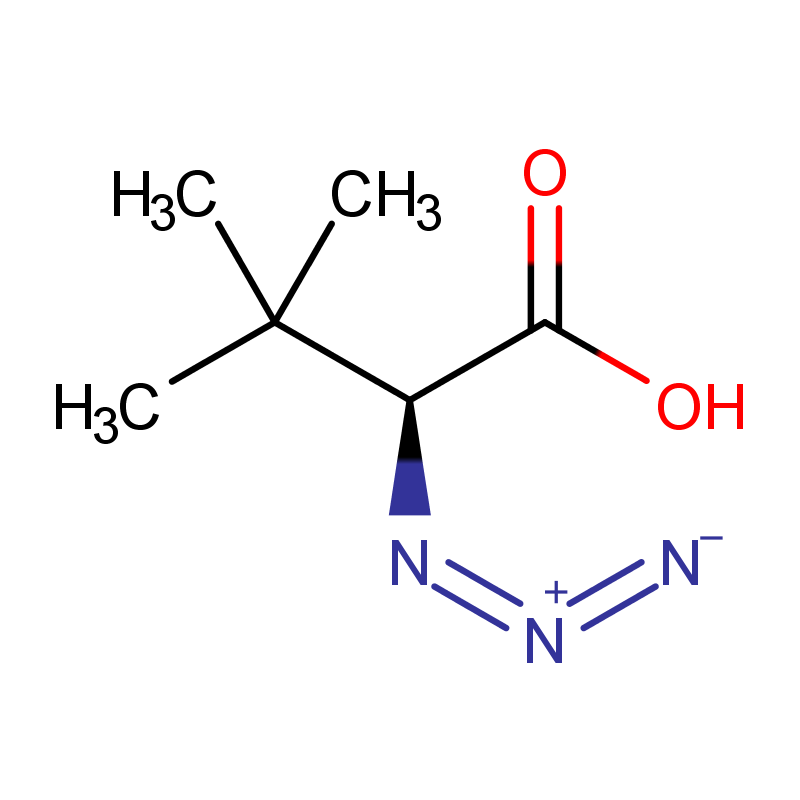
结构:
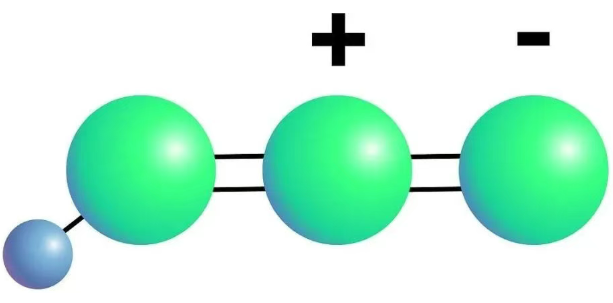
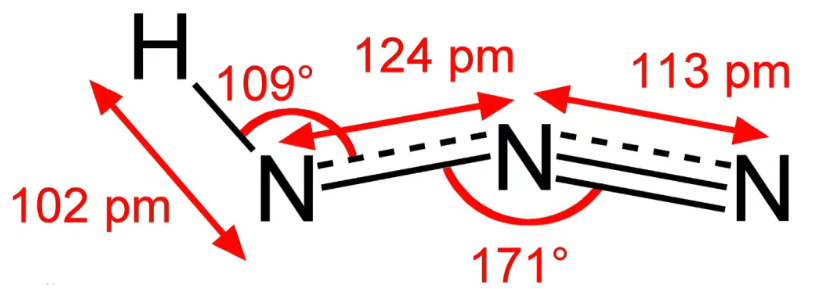
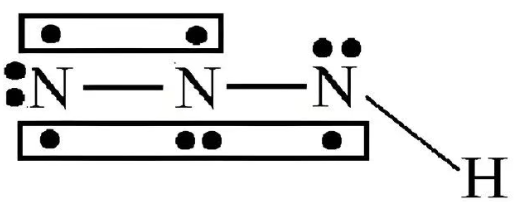

性质
氢叠氮酸为无色有刺激味的液体,沸点308.8K,熔点193K。它是易爆物质,只要受到撞击就立即爆炸而分解。
2HN3![]() 3N2+H2 ΔRHθ=-593.6kJ·mol-1
3N2+H2 ΔRHθ=-593.6kJ·mol-1
因为HN3的挥发性高,可用稀H2SO4与NaN3作用制备HN3:
NaN3+H2SO4![]() NaHSO4+HN3
NaHSO4+HN3
NaN3可从下面反应得到:
3NaNH2+NaNO3![]() NaN3+3NaOH + NH3
NaN3+3NaOH + NH3
HN3的水溶液为一元弱酸(K=1.9×10-5),它与碱或活泼金属作用生成叠氮化物。
HN3+NaOH![]() NaN3+H2O
NaN3+H2O
2HN3+Zn![]() Zn(N3)2+H2
Zn(N3)2+H2
HN3中N的氧化态为-1/3,所以它既显氧化性又显还原性。HN3的水溶液会发生歧化分解。
HN3+H2O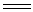 NH2OH + N2
NH2OH + N2
活泼金属如碱金属和钡等的叠氮化物,加热时不爆炸,分解为氮和金属。
2NaN3(s)![]() 2Na(l) + 3N2(g)
2Na(l) + 3N2(g)
加热LiN3则转变为氮化物。象Ag、Cu、Pb、Hg等的叠氮化物加热就发生爆炸,基于这一性质,Pb(N3)2和Hg(N3)2可做为雷管的起爆剂。
性质补充
HN₃的电离与酸性:
HN₃⇌H⁺+N₃⁻(pKa=4.6~4.7,25℃)
与金属反应:
Zn+2HN₃=Zn(N₃)₂+H₂↑(缓慢释放氢气)
与碱中和:
HN₃+NaOH=NaN₃+H₂O(生成盐和水)
氧化性:可被强还原剂(如HI)还原:
HN₃+2HI=NH₃+N₂+I₂
酸性强弱对比:
醋酸(CH₃COOH) pKa=4.76
氢氰酸(HCN) pKa=9.2
酸性强度:HN₃>CH₃COOH>HCN
制备方式(酸化叠氮盐):
NaN₃+H₂SO₄=HN₃+NaHSO₄(需低温操作)
物理性质:无色液体,沸点仅37℃,刺激性气味(类似硝酸);易挥发,20℃时蒸气压高达520mmHg。
致命缺陷:对震动、热、光极度敏感,室温下可能自发爆炸。2HN₃=3N₂+H₂这个反应的同时释放大量热(爆炸速度超5000m/s)。
叠氮酸钠(NaN₃)属于盐吗?

NaN₃是典型的离子化合物(盐类)。
组成结构:由钠阳离子(Na⁺)和叠氮酸根阴离子(N₃⁻)通过离子键结合,符合盐的定义(金属离子+酸根离子)。
物理性质:白色结晶固体,易溶于水(溶解度约40g/100mL,20℃),水溶液呈弱碱性(因N₃⁻水解:N₃⁻+H₂O⇌HN₃+OH⁻,pH≈8.5)。
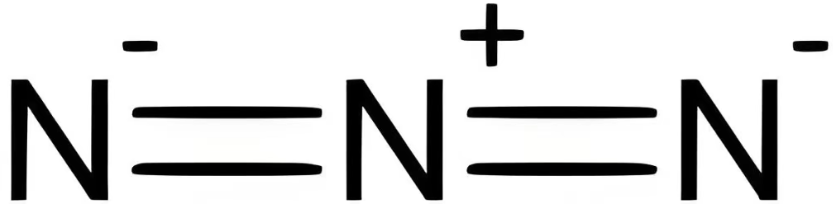
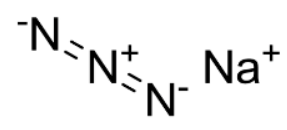
化学性质:
①受热分解:2NaN₃=2Na+3N₂↑(用于汽车安全气囊)
②与酸反应:NaN₃+HCl=HN₃+NaCl(生成叠氮酸,剧毒)
③常见用途:化工合成、安全气囊产气剂、防腐剂(需严格控制剂量)
④NaN₃是剧毒:(LD₅₀≈27mg/kg,大鼠口服),且与重金属(如Pb²⁺、Cu²⁺)接触可能生成爆炸性叠氮化物!

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
一、认识双氧水:从分子结构说起 化学名称:过氧化氢(Hydro...
一、总方法:接触法 整个工业制硫酸分为三个阶段、三个设备、...
1.硫代硫酸钠(Na 2 S 2 O 3 ): Na 2 S 2 O 3 ·5H 2 O俗名海波或大苏打,...
...
磷作为周期表第 ⅤA 族核心元素,兼具 “生命不可替代性”(构...
硫酸盐 俗名 颜色 用途 2CaSO 4 H 2 O 熟石膏 白色 CaSO 4 2H 2 O 生石膏...