
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、方法介绍
2Al+6HCl===2AlCl3+3H2↑
2Al+2NaOH+2H2O===2NaAlO2+3H2↑
(1)等质量的铝与足量的盐酸、氢氧化钠溶液分别反应:
①产生H2的物质的量相等。
②消耗H+、OH-的物质的量之比为n(H+)∶n(OH-)=3∶1。
(2)足量的铝分别与等物质的量的HCl和NaOH反应:
①消耗Al的物质的量之比为1∶3。
②生成H2的物质的量之比为1∶3。
(3)一定量的铝分别与一定量的盐酸、氢氧化钠溶液反应:
若产生氢气的体积比为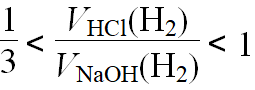 ,则必定
,则必定
①铝与盐酸反应时,铝过量而HCl不足。
②铝与氢氧化钠溶液反应时,铝不足而NaOH过量。
二、应用
甲、乙两烧杯中各盛有100mL3mol·L-1的盐酸和NaOH溶液,向两烧杯中分别加入等质量的铝粉,反应结束后,测得生成的气体体积比为V(甲)∶V(乙)=1∶2,则加入铝粉的质量为________(填字母)。
A.5.4g B.3.6g C.2.7g D.1.8g
解析:其反应原理分别为2Al+6HCl===2AlCl3+3H2↑,2Al+2NaOH+2H2O===2NaAlO2+3H2↑。可见当参加反应的HCl和NaOH的物质的量一样多时,产生H2的体积比是1∶3,而题设条件体积比为1∶2,说明此题投入的铝粉对盐酸来说是过量的,而对于NaOH来说是不足的。
2Al+6HCl=== 2AlCl3 + 3H2↑
6mol 3mol
3mol·L-1×0.1L 0.15mol
则Al与NaOH反应生成的H2为0.15mol×2=0.3mol。
2Al+2NaOH+2H2O===2NaAlO2+3H2↑
2×27g 3mol
5.4g 0.3mol
即投入的铝粉为5.4g。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
化学计算是化学学习中的重点,也是难点。中学化学常见的计算...
Fe 3+ 有较强的氧化性,可以把铁粉氧化成 Fe 2+ : 2Fe 3+ +Fe=3Fe 2...
在涉及金属铝及其化合物的计算中,有一类重要的计算,就是铝...
1、何为过量? 如某反应中两种反应物的量都已给出,则应先通过...
铁与稀硝酸的反应与反应物的量有关,原因在于金属铁有变价。...
一、问题的提出 将amolFe 3+ 、bmolCu 2+ 、cmolFe和dmolCu混合于同一反...