
|
学习小专题 |
 为何二氟化碘离子离子的空间构型为直线形,键角为90°,120°?
日期:2025-08-07 11:09:55
点击:564
好评:0
为何二氟化碘离子离子的空间构型为直线形,键角为90°,120°?
日期:2025-08-07 11:09:55
点击:564
好评:0
分析: 依据价层电子对数计算公式分析, 可得价层电子对数=5=[2+3],故有2个配位原子F,形成2对成键电子对( 键),剩余3对孤电子对,其分子的空间构型可能如下三种情况; 依据孤对电子对不参加成键,只受到一个核的吸引,电子云比成键电子对更“肥大”,故电子对间斥力...
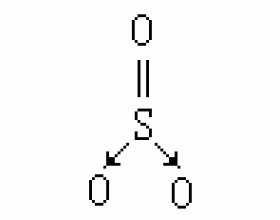 分子结构规律——最大对称原理
日期:2022-12-08 16:45:16
点击:44937
好评:2
分子结构规律——最大对称原理
日期:2022-12-08 16:45:16
点击:44937
好评:2
化合物中的中心原子周围的电子对之间总是尽可能最大角度地对称分布,因为共用电子之间的角度越大,对称性越高,它们之间的同性排斥力就必然越小,这样分子就必然越稳定。这个规律不妨叫做最大对称原理。 只有当中心原子周围的电子对(或共价键)相同时,它们才可能最大...
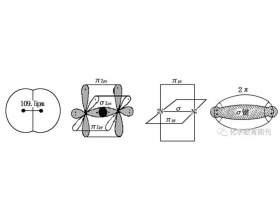 氮及其化合物的分子空间结构分析
日期:2022-07-29 10:23:13
点击:32033
好评:1
氮及其化合物的分子空间结构分析
日期:2022-07-29 10:23:13
点击:32033
好评:1
氮原子的价电子结构为2s22p3,电负性仅次于氟与氧,能与其他元素形成较强的化学键,存在多种价态,高中生很难正确把握氮及其化合物的结构,笔者对此进行理论分析和结构总结,以期有助于师生的正确理解。 根据中心原子成键时杂化方式的不同,本文将氮及其化合物分成四大...
 分子(离子)的几何构型的判断方法
日期:2022-07-29 10:22:15
点击:40670
好评:0
分子(离子)的几何构型的判断方法
日期:2022-07-29 10:22:15
点击:40670
好评:0
1、确定中心原子价层电子数。它可由下式计算得到: 价层电子对数=(中心原子价电子数+ 配位原子提供电子数-离子所带电荷数)/2 上式中配位原子提供电子数的计算方法是:氢和卤素原子均提供1个价电子;氧和硫原子提供电子为零。因为氧和硫价电子数为6,它与中心原子成键...
 分子立体结构的判断方法详解
日期:2022-07-29 10:20:04
点击:21951
好评:0
分子立体结构的判断方法详解
日期:2022-07-29 10:20:04
点击:21951
好评:0
一、价层电子对互斥模型( VSEPRmodels ) 把分子分成两大类:一类是中心原子上的价电子都用于形成共价键。如 CO 2 、 CH 2 O 、 CH 4 等分子中的 C 原子。它们的立体结构可用中心原子周围的原子数来预测,概括如下: 另一类是中心原子上有孤对电子(未用于形成共价键的...
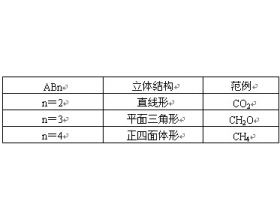 有关分子空间结构的判断方法
日期:2022-07-29 10:19:08
点击:41702
好评:0
有关分子空间结构的判断方法
日期:2022-07-29 10:19:08
点击:41702
好评:0
(一)价层电子对互斥模型(VSEPRmodels) 把分子分成两大类:一类是中心原子上的价电子都用于形成共价键。如CO 2 、CH 2 O、CH 4 等分子中的C原子。它们的立体结构可用中心原子周围的原子数来预测,概括如下: 另一类是中心原子上有 孤对电子 ( 未用于形成共价键的电...
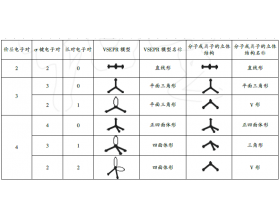 如何通过分子式直接推断分子的立体结构
日期:2022-07-29 10:16:53
点击:5961
好评:0
如何通过分子式直接推断分子的立体结构
日期:2022-07-29 10:16:53
点击:5961
好评:0
教材在介绍分子立体结构模型时先给出了分子的分子式和结构式后介绍了有关分子的立体结 构,所以有些学生在学习这部分内容时常常会从结构式着手推分子立体结构,其实这只是一部分同学学习过程中的一个误区。应用价层电子对互斥理论推测ABn型分子的立体结构模型时,只要 ...
 判断分子空间结构的方法
日期:2022-07-29 10:13:51
点击:138110
好评:12
判断分子空间结构的方法
日期:2022-07-29 10:13:51
点击:138110
好评:12
分子的立体构型是指分子中的原子在空间的排布,由键长和键角共同决定。 在高中阶段,判断分子的空间构型,常用的方 法有 3 种。 — 、 价层电子对互斥模型 ( VSEPR) 早在 1940 年,希吉维克和坡维尔在总结实验事实的基础上提出了一种简单的理论模型,用以预测简单分子...
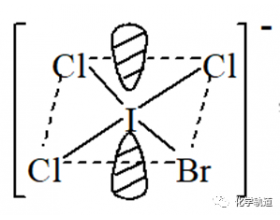 一个多卤离子的空间结构
日期:2022-07-29 10:12:55
点击:1456
好评:0
一个多卤离子的空间结构
日期:2022-07-29 10:12:55
点击:1456
好评:0
题目: 根据VSEPR理论,对于IBrCl3-: (1)计算其中心原子的价层电子对数; (2)画出几何构型; (3)指出孤电子对数; (4)给出分子构型的名称; (5)对分子结构中键角可能偏离理想构型的情况给予简单说明。 解析: 中心原子:I 配位原子(共4个):1个Br-,3个Cl-...
 动画演示:分析氨分子和铵离子的空间结构
日期:2022-07-29 10:12:09
点击:414
好评:0
动画演示:分析氨分子和铵离子的空间结构
日期:2022-07-29 10:12:09
点击:414
好评:0
...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。