
|
ѧϰСר�� |
 ����������ܱȽ�
���ڣ�2023-09-04 14:50:53
�����2058
������0
����������ܱȽ�
���ڣ�2023-09-04 14:50:53
�����2058
������0
���ܣ������й��ۼ��ļ��ܣ�ʹ1mol ij���ۼ��������������(���ʣ�kJ/mol)�� ��˵���Ӽ�(�ͽ�����)�ļ��ܣ���Ϊ���Ӽ�û�б����ԣ�������������������о�����������Զ����������Ҳ��������ͬ�����Ӽ仹�г������������Ӿ���Ļ�ѧ��������������������Ӽ�ļ�����ȡ��...
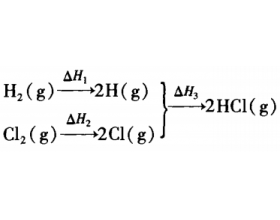 ��ѧ��Ӧ���ʉ�����ܹ�ϵ����
���ڣ�2022-07-23 17:13:54
�����4440
������0
��ѧ��Ӧ���ʉ�����ܹ�ϵ����
���ڣ�2022-07-23 17:13:54
�����4440
������0
��ѧ��Ӧ���ұ����¿α�Ҫ�����յ�һ������ ���������ܵĹ�ϵ���С�������Ϊ��Ӧ��ʵ���� ��ɷ�Ӧ��ĸ��ֻ�ѧ�����ƻ������������ĸ� �ֻ�ѧ�����γɡ��ڴ˹����У���Ȼ�����������ı� �� ,�������ʽΪ�����ķų������ա����������ı仯����ӳ��������������...
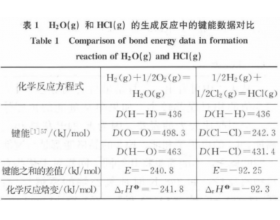 ���ڼ������ܡ����ܡ���Ӧ�ʱ��̽��
���ڣ�2022-07-21 09:16:20
�����3068
������0
���ڼ������ܡ����ܡ���Ӧ�ʱ��̽��
���ڣ�2022-07-21 09:16:20
�����3068
������0
�������ܡ����ܡ���Ӧ�ʱ��dz����Ļ�ѧ���ͨ�������Ĵ�ʡ�μӡ�����ƻ����Ľ�ʦ���֣��������ʦ������3������ײ�����������Ҫ����֮һ�Ƕ�����ʦ��Ϊ���������������ȫ��ͬ�������������������ͬһ������⣬���ڼ��ܺͷ�Ӧ�ʱ�Ĺ�ϵ��������ʦ��Ϊ����ѧ��Ӧ...
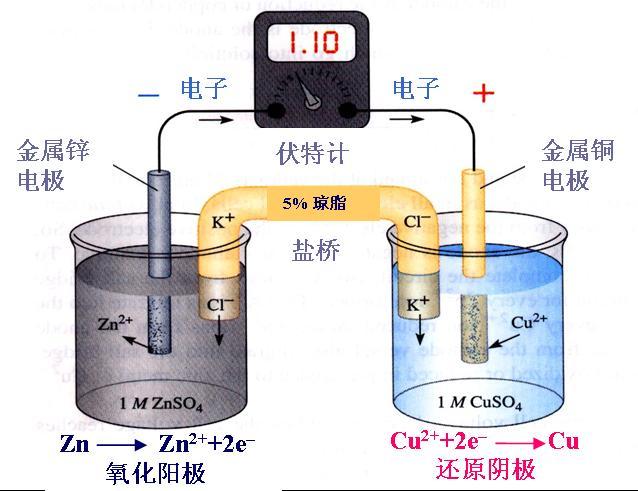 ������ѧ�����ܱ�
���ڣ�2022-04-18 08:11:00
�����12098
������0
������ѧ�����ܱ�
���ڣ�2022-04-18 08:11:00
�����12098
������0
��ѧ��(Chemical bond) ���� (Bond length) /(10-12m) ���� (Bond energy) /(kJ/mol) ��ѧ��(Chemical bond) ���� (Bond length) /(10-12m) ���� (Bond energy) /(kJ/mol) B��F - 644 N��H 101 389 B��O - 515 N��N 145 159 Br��Br 229 193 N�TN 125 456 C��B 156 393 N��N...
 �����˳��ѧ�ܡ���ѧ�����ȶ����������仯�Ĺ�ϵ��
���ڣ�2021-01-18 10:09:31
�����1030
������0
�����˳��ѧ�ܡ���ѧ�����ȶ����������仯�Ĺ�ϵ��
���ڣ�2021-01-18 10:09:31
�����1030
������0
1����ѧ��Ӧ��������ʲô�� ��ѧ��Ӧ�������������������ɡ���ѧ��Ӧ�����˷�Ӧ������������ʵ�������ʵ�ת���� 2����ѧ��Ӧ�ı�����ʲô�� ��ѧ��Ӧ�Ĺ��̰�����Ӧ���л�ѧ���Ķ��Ѻ��������л�ѧ�����γɡ����ڡ���ѧ��Ӧ�����˷�Ӧ������������ʵ������...
 ΪʲôN��N���ܴ���N��N���ܵ�3����
���ڣ�2019-11-06 10:39:44
�����5078
������0
ΪʲôN��N���ܴ���N��N���ܵ�3����
���ڣ�2019-11-06 10:39:44
�����5078
������0
��1 ����˫������������ ��ѧ�� ����/pm ����/kJ��mol ��1 ��ѧ�� ����/pm ����/kJ��mol ��1 ��ѧ�� ����/pm ����/kJ��mol ��1 C��C 154 347.7 N��N 145 193 O��O 148 142 C=C 153 615 N=N 125 418 O=O 120 497.3 C��C 120 812 N��N 110 946 C��O 143 315 N��O 146 176 ...
 ΪʲôN��H������С��C��H�����ܣ�
���ڣ�2019-11-06 10:39:06
�����12166
������0
ΪʲôN��H������С��C��H�����ܣ�
���ڣ�2019-11-06 10:39:06
�����12166
������0
��1���ַǽ���Ԫ��ԭ������ԭ���γɵĹ��ۼ���������� ��ѧ�� C��H N��H O��H ����/pm 109 101 96 ����/KJ��mol ��1 413.4 390.8 462.8 ͨ����3���֣�N��H�����������ܾ�С��C��H���������������̬�⻯���ȶ���NH 3 ��CH 4 ��Ҫ���͡�ΪʲôN��H������С��C��H����...
 ����������Խ�ߣ����ܾ�Խ����?
���ڣ�2019-06-26 11:11:24
�����7256
������4
����������Խ�ߣ����ܾ�Խ����?
���ڣ�2019-06-26 11:11:24
�����7256
������4
���������������ʵ�����(������ѧ��)���������ڸ�����ʽ�������ܺͣ��������Ӷ��ܡ��������ܡ������ڵ��ӵĶ��ܺ����ܣ�ԭ�Ӻ��ܵȵȣ�������ʶ��������ڷ�����������ʽ�����ܵľ���ֵ����ȷ������������ָ�ڳ�����(25�� ) ��̬��ѧ���ֽ����̬ԭ�������յ�������������...
 dz�����������Ĺ�ϵ
���ڣ�2019-06-05 09:41:26
�����8108
������0
dz�����������Ĺ�ϵ
���ڣ�2019-06-05 09:41:26
�����8108
������0
�˽̰桶ѡ��3���ڶ��µ�һ�ڹ��ڼ�������������������ģ���������̬��̬ԭ���γ�1 mol ��ѧ���ͷŵ�����������������γɹ��ۼ�������ԭ��֮��ĺ˼�ࡣ����Խ�̣���������Խ�������ۼ�Խ�ȶ�����Ŀǰͨ�������Ե��о��ͼ��㷢�֣��������л������еĻ�ѧ������...
 ������ѧ���ļ��������
���ڣ�2013-05-07 08:58:49
�����37336
������0
������ѧ���ļ��������
���ڣ�2013-05-07 08:58:49
�����37336
������0
�±������л�ѧ���ļ��������ֵ���ڴ����������Ǻ��иû�ѧ���ĸ��ֲ�ͬ�����еļ����ͼ���ֵ��ƽ��ֵ�����м�����ָ��������� 25��Ͽ�1Ħ���ü����������� ������ѧ���ļ�������� Bond Lengths and Bond Energies of C...
 ��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ�
��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ� ��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء�
��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء�