
|
学习小专题 |
 消暑凉袋中的化学原理
日期:2022-08-01 17:34:52
点击:5363
好评:0
消暑凉袋中的化学原理
日期:2022-08-01 17:34:52
点击:5363
好评:0
夏天到的时候,我们通常可以看到超市里有一种凉袋出售。在炎炎的夏日中抱在怀里,垫在椅子上,或者睡觉的时候当枕头,无疑给炎炎的夏日带来一丝凉意。当我们把凉袋拿到手中时,感觉胶袋里面好像是装了水,那么,胶袋里面装的到底是不是水呢?根据生活常识,很多人都会...
 化学作坊:如何制作化学冰袋
日期:2022-08-01 17:33:32
点击:14428
好评:0
化学作坊:如何制作化学冰袋
日期:2022-08-01 17:33:32
点击:14428
好评:0
随着夏季的到来,食品的储存离不开冰箱,外出旅游、郊游时,想致冷饮料和食品更是没有好的办法。但是如果家中没有冰箱,而且又想在外出旅游、郊游的时候拥有冷的食品,怎么办?教你一个具有经济价值的办法,那就是用化学的方法“冰袋”,以最简单、廉价、安全的方法,取...
 四种基本反应类型与放热反应和吸热反应的关系
日期:2016-01-31 21:30:10
点击:47263
好评:1
四种基本反应类型与放热反应和吸热反应的关系
日期:2016-01-31 21:30:10
点击:47263
好评:1
一、化合反应中的放热反应和吸热反应 绝大多数的化合反应是放热反应,少数化合反应是吸热反应。 1、化合反应中常见的放热反应: (1)氢化物的生成反应是放热反应的实例 ①氢气与氟气黑暗处就爆炸放热:H2+F2=2HF ②氢气在氯气中燃烧放热:H2+Cl2...
 趣味实验:化学能就在“身边”
日期:2016-01-31 21:14:17
点击:21001
好评:0
趣味实验:化学能就在“身边”
日期:2016-01-31 21:14:17
点击:21001
好评:0
家住城郊或者农村的同学可能都注意到这样的现象:建筑工人将红薯、鸡蛋埋入生石灰中,然后浇水,石灰堆上会顿时冒出大量浓烈而滚烫的热汽;不一会儿取出红薯、鸡蛋一尝——早熟透了!还有呢,在炎热的夏天里,你赤着脚往水田里抛洒碳铵( NH 4 HCO 3 )或肥田粉 [ (NH 4...
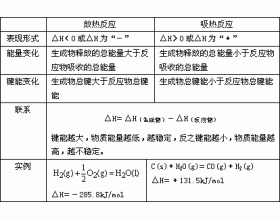 化学反应放热或吸热的判断
日期:2016-01-31 20:26:07
点击:9717
好评:0
化学反应放热或吸热的判断
日期:2016-01-31 20:26:07
点击:9717
好评:0
1、根据具体化学反应实例判断 (1)常见的放热反应:所有可燃物的燃烧、所有金属与酸的反应、所有中和反应、绝大多数化合反应、少数分解反应、多数置换反应、铝热反应、某些复分解反应。典型反应: (2)常见的吸热反应:极个别的化合反应(CO 2 和C的反应)、绝大多数...
 常见的放热反应和吸热反应的总结
日期:2015-12-11 20:55:31
点击:23526
好评:1
常见的放热反应和吸热反应的总结
日期:2015-12-11 20:55:31
点击:23526
好评:1
1.放热反应 ①活泼金属置换水或酸中氢的反应,如: 2Na+2H2O=2NaOH+H2 2Al+6HCl=2AlCl3+3H2 ②酸碱中和反应。如: NaOH+HCl=NaCl+H2O 2KOH+H2SO4=K2SO4+2H2O ③含碳燃料燃烧的反应,如: 2CO+O2 2CO2 CH3CH2OH+3O2 2CO2+3H2O ④易爆物质的爆炸反应。 ⑤多数的化合反应...
 放热反应和吸热反应与四种基本反应类型的关系以及判断
日期:2015-12-11 20:38:25
点击:37664
好评:0
放热反应和吸热反应与四种基本反应类型的关系以及判断
日期:2015-12-11 20:38:25
点击:37664
好评:0
一、四种基本反应类型与放热反应和吸热反应的关系 (一)、化合反应中的放热反应和吸热反应 绝大多数的化合反应是放热反应,少数化合反应是吸热反应。 1 、化合反应中常见的放热反应: ( 1 )氢化物的生成反应是放热反应的实例 ①氢气与氟气黑暗处就爆炸放热: H 2 +F ...
 四个简单的吸热反应实验
日期:2015-12-11 20:25:41
点击:17587
好评:0
四个简单的吸热反应实验
日期:2015-12-11 20:25:41
点击:17587
好评:0
吸热反应实验是一个新的很重要的实验,也是一个疑难实验。通过我们的研究,现介绍四个简单的吸热反应实验。可以作为教师的演示实验也可以作为学生的探究实验。 1、氯化铵与氢氧化钡晶体[Ba(OH) 2 8H 2 O]反应 1.1 实验步骤和现象 在小烧杯里加入20g已研磨成粉末的氢氧化...
 放热和吸热的经验规则
日期:2015-12-11 19:46:43
点击:1385
好评:0
放热和吸热的经验规则
日期:2015-12-11 19:46:43
点击:1385
好评:0
一般情况下,解离的反应是吸热的,如分解、离解(电离)、水解、电解等,反之,合的反应放热,如化合、结合(离子结合成气体、沉淀、弱电解质)等。 作为氧化还原反应,氧化性还原性强的物质之间反应生成氧化性还原性弱的物质都是放热的,反之是吸热的。...
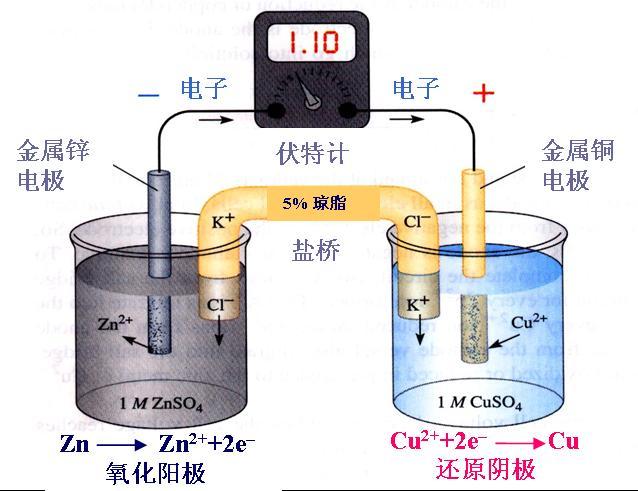 碳酸氢钠与强酸反应为啥吸热?
日期:2015-02-03 09:13:51
点击:2226
好评:0
碳酸氢钠与强酸反应为啥吸热?
日期:2015-02-03 09:13:51
点击:2226
好评:0
NaHCO 3 (s)+H + =Na + +H 2 O(l)+CO 2 (g),用焓变来判别; 根据公式:△rHm=∑(△fHm)产物-∑(△fHm)反应物 △rHm,298=[(-239.66)+(-285.83)+(-393.51)]-[(-947.7)+0]=28.7 KJ/mol (△rHm﹥0),所以此反应为吸热反应。...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。