
|
ѧϰСר�� |

|
ѧϰСר�� |
 [̽������չ5] Ũ�ȷֱ�Ϊ0.1mol/L��̼������Һ��̼��������Һ��˭����ǿ�� ����:�¿��� ��Դ:δ֪ ���ڣ�2017-04-06 20:57:57 �����1333 ����ר�⣺̼���� ̼������01 ����ˮ�����
[̽������չ5] Ũ�ȷֱ�Ϊ0.1mol/L��̼������Һ��̼��������Һ��˭����ǿ�� ����:�¿��� ��Դ:δ֪ ���ڣ�2017-04-06 20:57:57 �����1333 ����ר�⣺̼���� ̼������01 ����ˮ�����
...
 [ע�������j] �Ե���ƽ�ⳣ������̼��������ӵ����ӹ������� ����:����ƽ ��Դ:δ֪ ���ڣ�2017-03-03 09:06:09 �����2373 ����ר�⣺����ƽ�ⳣ�� ̼������01 ���ӹ���
[ע�������j] �Ե���ƽ�ⳣ������̼��������ӵ����ӹ������� ����:����ƽ ��Դ:δ֪ ���ڣ�2017-03-03 09:06:09 �����2373 ����ר�⣺����ƽ�ⳣ�� ̼������01 ���ӹ���
...
 [̽������չ5] ̼��������Һ��ֵ�ù�ע�ļ������� ����:��ǫ ��Դ:δ֪ ���ڣ�2017-03-02 10:23:16 �����772 ����ר�⣺̼������01
[̽������չ5] ̼��������Һ��ֵ�ù�ע�ļ������� ����:��ǫ ��Դ:δ֪ ���ڣ�2017-03-02 10:23:16 �����772 ����ר�⣺̼������01
...
 [ע�������j] �����������������ڶ���ͭ�������� ����:��Ϧ ��Դ:δ֪ ���ڣ�2019-06-11 16:31:48 �����2138 ����ר�⣺������ ����ת��
[ע�������j] �����������������ڶ���ͭ�������� ����:��Ϧ ��Դ:δ֪ ���ڣ�2019-06-11 16:31:48 �����2138 ����ר�⣺������ ����ת��
...
 [ע�������j] ����ƽ������еķ���Ũ����ƽ��Ũ�� ����:�º� ��Դ:δ֪ ���ڣ�2017-03-02 10:04:10 �����1978 ����ר�⣺���ʵ���Ũ�� ����ƽ��
[ע�������j] ����ƽ������еķ���Ũ����ƽ��Ũ�� ����:�º� ��Դ:δ֪ ���ڣ�2017-03-02 10:04:10 �����1978 ����ר�⣺���ʵ���Ũ�� ����ƽ��
...
 [ע�������j] ������ǿ�ᾭ������ ����:���� ��Դ:δ֪ ���ڣ�2016-12-28 10:51:48 �����2774 ����ר�⣺ǿ��������
[ע�������j] ������ǿ�ᾭ������ ����:���� ��Դ:δ֪ ���ڣ�2016-12-28 10:51:48 �����2774 ����ר�⣺ǿ��������
1�������������� 1.����ʽ��CuSO 4 ��H 2 S== CuS �� H 2 SO 4 2.ƽ�ⳣ��K=7.143��10 14 3.��Ȼ�ܷ�����Ӧ��ԭ��Ҳ�ܼ�Cu���ӵĴ��ڣ��ٽ���������ĵ��룬�õ�ǿ��(����) 2�������������� 1.��֪���볣��K(CHCOOH)=1.76��10 ��5 ��K(HNO 2 )=4.6��10 ��4 2.����ʽ...
 [ע�������j] �ķ��������������ˮ�ⷴӦ ����:���ڷ� ��Դ:δ֪ ���ڣ�2016-11-04 16:32:05 �����5678 ����ר�⣺�ķ����� ����ˮ�ⷴӦ
[ע�������j] �ķ��������������ˮ�ⷴӦ ����:���ڷ� ��Դ:δ֪ ���ڣ�2016-11-04 16:32:05 �����5678 ����ר�⣺�ķ����� ����ˮ�ⷴӦ
�ܺͣ�3SiF 4 ��3H 2 O��H 2 SiO 3 ��2H 2 SiF 6 ˮ�⡢����ܹ��棬�ܿ��档 �ܺ� 2AlF 3 ��3H 2 O= Al(OH) 3 ��H 3 AlF 6 �ķ�������HF���ΪH 2 SiF 6 ����NaF���Ϊ Na 2 SiF 6 ����������HF���ΪH 3 AlF 6 ����NaF���Ϊ Na 3 AlF 6 дһд�� 1��Al(OH) 3 ��Al 2 O 3...
 [ע�������j] ����ˮ��ѧϰ�еļ������� ����:���� ��Դ:δ֪ ���ڣ�2016-05-12 19:17:28 �����961 ����ר�⣺����ˮ��
[ע�������j] ����ˮ��ѧϰ�еļ������� ����:���� ��Դ:δ֪ ���ڣ�2016-05-12 19:17:28 �����961 ����ר�⣺����ˮ��
...
 [ע�������j] �߳�����к͵ζ������� ����:���� ��Դ:δ֪ ���ڣ�2016-05-12 19:14:56 �����773 ����ר�⣺�к͵ζ�
[ע�������j] �߳�����к͵ζ������� ����:���� ��Դ:δ֪ ���ڣ�2016-05-12 19:14:56 �����773 ����ר�⣺�к͵ζ�
...
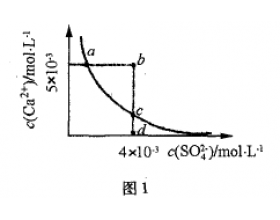 [ע�������j] �߳��ܽ�ƽ��ļ������� ����:����һ ��Դ:δ֪ ���ڣ�2016-05-12 19:01:12 �����3070 ����ר�⣺�ܽ�ƽ��
[ע�������j] �߳��ܽ�ƽ��ļ������� ����:����һ ��Դ:δ֪ ���ڣ�2016-05-12 19:01:12 �����3070 ����ר�⣺�ܽ�ƽ��
��ѧ��ѧ�ij����ܽ�ƽ����ָ:��һ���¶��£����ܵ� ������Һ�У����ܽ���������������ʱ�������˹������� Һ������֮��Ķ�̬ƽ��.�������漰�ܽ�ȡ�Ksp�������� ת������������������.���ڽ̲��ϵ����ݽ���������� �࣬ʹ�úܶ�ѧ�����ⷽ�������ʶ������.����...
 ��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ�
��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ� ��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء�
��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء��ʣ�Ϊʲôǿ���ڱ������п��ԱȽϳ�������ǿ���� ��Ҫ�ش�������⣬���ǵûص����...
����0.01mol ZnS����1.0L �����У�������������Ũ�ȣ� �����֪�� K sp (Zns)=2.0��...
ˮ�����ӻ����� K w ��һ���¶ȵĺ���������֮�����ֻ���¶��йأ�ֻҪ�¶Ȳ��䣬��...
�����������ˮ��ʱ���Ƚ���������Ӻͷ����ӣ����������Ҫ���������� �����Ӻͷ�...
...
HI 10 11 HBr 10 9 HCl 10 7 HClO 4 10 7 HClO 3 10 3 H 2 SO 4 10 2 HNO 3 20 H 3 O ...
һ�� ǿ��������ʸ����ϵ��Ĵ����� ǿ�������ˮ��Һ��ȫ�����룬���벻���棬������...
�������ָʾ����ɫ��pH��Χ���ټ���3.1~4.4���ڼ���4.4~6.2�۷�̪8.2~10������0....