
|
学习小专题 |

|
学习小专题 |
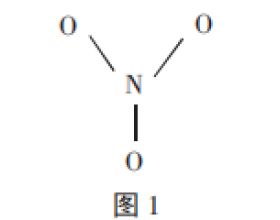 [方法与规律e] 路易斯结构式的书写 作者:庞晓峰 来源:未知 日期:2020-03-19 10:28:00 点击:23985 所属专题:路易斯结构式
[方法与规律e] 路易斯结构式的书写 作者:庞晓峰 来源:未知 日期:2020-03-19 10:28:00 点击:23985 所属专题:路易斯结构式
一、路易斯理论的介绍 1916年,美国化学家路易斯通过对实验现象的归纳总结,提出分子中的原子之间可以通过共享电子对,使分子中的每个原子具有稳定的稀有气体电子结构(除了He为1P外,其他稀有气体的价电子构型均为 n s 2 n p 6 ) ,这样形成的分子成为共价分子,原子之间通...
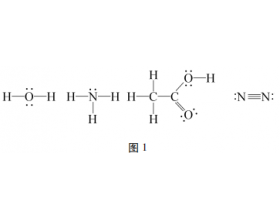 [方法与规律e] 例析路易斯结构式的书写 作者:蒋泓 来源:未知 日期:2020-03-19 10:20:48 点击:22411 所属专题:路易斯结构式
[方法与规律e] 例析路易斯结构式的书写 作者:蒋泓 来源:未知 日期:2020-03-19 10:20:48 点击:22411 所属专题:路易斯结构式
路易斯结构式源于路易斯结构理论,又称为八隅体理论。该理论的基本要点如下:一个共价 化合物(或共价分子)能够稳定存在,是由于电子对的共享使每个原子能够形成一种稳定的稀有气体电子构型。在书写路易斯结构式时,两原子间以短线相连,孤对电子用小黑点表示。 对于简单的分...
 [方法与规律e] 运用均摊法计算化合物分子间氢键的数目 作者:化学自习室 来源:未知 日期:2020-02-26 10:16:14 点击:7723 所属专题:均摊法 氢键02
[方法与规律e] 运用均摊法计算化合物分子间氢键的数目 作者:化学自习室 来源:未知 日期:2020-02-26 10:16:14 点击:7723 所属专题:均摊法 氢键02
我们知道,氢键像共价键一样也是存在方向性和饱和性的。什么是方向性和饱和性呢?每个原子所能形成共价键的数目取决于该原子中的单电子数目,这就是共价键的饱和性。成键时,两原子轨道重叠愈多,两核间电子云愈密集,形成的共价键愈牢固,这称为原子轨道最大重叠原理,...
 [方法与规律e] 键角NF3小于NH3, 则键角PF3也小于PH3吗? 作者:化学自习室 来源:未知 日期:2020-02-16 13:48:40 点击:4427 所属专题:键角
[方法与规律e] 键角NF3小于NH3, 则键角PF3也小于PH3吗? 作者:化学自习室 来源:未知 日期:2020-02-16 13:48:40 点击:4427 所属专题:键角
看到一道高中化学选修3物构习题,要求比较PF 3 、PH 3 的键角并解释,习题答案是键角PF 3 <PH 3 ,原因是PF 3 中,F电负性大,吸引电子能力强,使成键电子对远离P原子,成键电子对之间的斥力减弱,故PF 3 键角变...
 [方法与规律e] 大π键的书写及认识 作者:化学自习室 来源:未知 日期:2020-01-30 12:14:10 点击:8017 所属专题:大Π键
[方法与规律e] 大π键的书写及认识 作者:化学自习室 来源:未知 日期:2020-01-30 12:14:10 点击:8017 所属专题:大Π键
...
 [方法与规律e] 大π键的形成与分析 作者:化学自习室 来源:未知 日期:2020-01-30 10:46:04 点击:7728 所属专题:大π键
[方法与规律e] 大π键的形成与分析 作者:化学自习室 来源:未知 日期:2020-01-30 10:46:04 点击:7728 所属专题:大π键
...
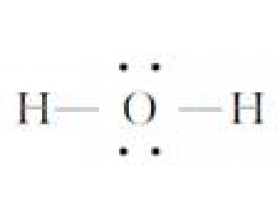 [方法与规律e] 多原子粒子中的中心原子价层电子对数计算方法及其应用 作者:化学自习室 来源:未知 日期:2020-01-02 07:09:38 点击:21191 所属专题:价层电子对数计算
[方法与规律e] 多原子粒子中的中心原子价层电子对数计算方法及其应用 作者:化学自习室 来源:未知 日期:2020-01-02 07:09:38 点击:21191 所属专题:价层电子对数计算
多原子粒子(分子或离子)中的中心原子价层电子对数的计算至关重要,它决定着价层电子对互斥理论模型(VSEPR模型)及中心原子杂化类型,同时还决定着粒子的立体构型。 一、根据多原子粒子的价电子构型计算中心原子价层电子对数 1.多原子分子中的中心原子价层电子对数计算 (1)先...
 [方法与规律e] 等电子体及其应用 作者:化学自习室 来源:未知 日期:2020-01-01 14:39:47 点击:7024 所属专题:等电子体
[方法与规律e] 等电子体及其应用 作者:化学自习室 来源:未知 日期:2020-01-01 14:39:47 点击:7024 所属专题:等电子体
一、 “等电子体”推导的一般方法 等电子体概念的核心内容是结构微粒的“两个相等”(原子数相等和价电子总数相等)。现将一些等电子体整理出来(见下表)。 等电子体类型 等电子体 2原子10价电子 N 2 、CO、CN - 、NO + 、C 2 2- 、O 2 2+ 3原子16价电子 CO 2 、CS 2 、N 2...
 [方法与规律e] 原子轨道杂化类型判断的几种方法 作者:化学自习室 来源:未知 日期:2020-01-01 11:24:02 点击:45014 所属专题:杂化类型判断
[方法与规律e] 原子轨道杂化类型判断的几种方法 作者:化学自习室 来源:未知 日期:2020-01-01 11:24:02 点击:45014 所属专题:杂化类型判断
1.依据微粒的空间构型 杂化轨道是为了解释多原子分子或复杂离子的空间构型而提出的,因而根据分子的空间构型可以逆推出中心原子的杂化类型, 。中学阶段主要涉及sp类型的杂化,其杂化方式及对应的空间构型、键角如下: 杂化轨道类型 杂化轨道空间构型 键角 sp 直线形 180°...
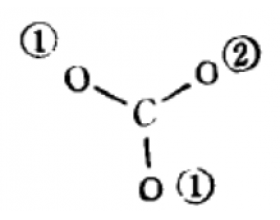 [方法与规律e] 有关书写大π键表达式的一点经验 作者:化学自习室 来源:未知 日期:2019-05-28 08:13:11 点击:7799 所属专题:大π键
[方法与规律e] 有关书写大π键表达式的一点经验 作者:化学自习室 来源:未知 日期:2019-05-28 08:13:11 点击:7799 所属专题:大π键
HMO法认为形成离域大π键的条件为: (l)形成离域大π键的原子均在同一平面上; (2)p电子数必须小于p轨道数的两倍。怎 样正确写出某个离域大π键的π m n 表达式呢?下面谈谈自己的一点休会。 步骤: (l)判断该分子有无形成大π键的可能,并确定n值; (2)将有关原子间以短线相连; (...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。1.σ键与π键 σ键:原子轨道沿着轨道对称轴的方向“头碰头”重叠形成的共价键。 π键...
配位化合物的空间构型: 二配位:直线型;四配位:正四面体型或平面正方形;六配位(无...
1、当中心离子(或原子)与多基配体配合时,配位数可以等同于配位原子的数目,但不是配...
一、 知识储备 1、 手性 手性 ( chirality ) 一词指一个物体不能与其镜像相重合 。 ...
人的左手和右手互为实物和镜像关系,彼此不能重合。手的这种特征在其他物质中也广泛存...
对于ABn型分子, 其中:①a表示中心原子的价电子数; 对主族元素:a=最外层电子数; ...
固态氨的障构比冰的复杂.每一个氮原子周围有6个最邻近 的氮原子,它们之间的距离为3.3...
分子的立体结构是指其原子在空间的排布,可以用现代实验手段测定。例如,通过分子或离...