
|
学习小专题 |

|
学习小专题 |
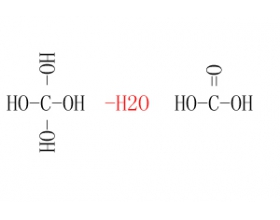 [注解与辨疑a] 元素最高价氧化物对应水化物的写法 作者:张红 来源:未知 日期:2014-12-06 19:05:00 点击:63793 所属专题:最高价氧化物水化物
[注解与辨疑a] 元素最高价氧化物对应水化物的写法 作者:张红 来源:未知 日期:2014-12-06 19:05:00 点击:63793 所属专题:最高价氧化物水化物
元素最高价氧化物对应的水化物,这一概念出现在高中化学必修2元素周期律那章,用于判断元素金属性和非金属性强弱。元素最高价氧化物对应水化物碱性越强,则金属性越强;元素最高价氧化物对应水化物酸性越强,则非金属性越强。 有些同学对于元素最高价氧化物对应的水化物...
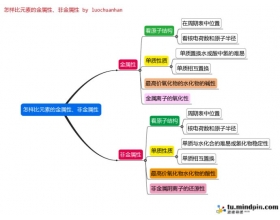 [注解与辨疑a] 怎样比较金属性、非金属性的强弱之思维导图 作者:张安荣 来源:未知 日期:2016-01-22 18:53:51 点击:1910 所属专题:金属性 非金属性
[注解与辨疑a] 怎样比较金属性、非金属性的强弱之思维导图 作者:张安荣 来源:未知 日期:2016-01-22 18:53:51 点击:1910 所属专题:金属性 非金属性
...
 [注解与辨疑a] 金属性和金属活动性概念比较 作者:邵磊 来源:未知 日期:2014-09-24 09:34:38 点击:1453 所属专题:金属性 金属活动性
[注解与辨疑a] 金属性和金属活动性概念比较 作者:邵磊 来源:未知 日期:2014-09-24 09:34:38 点击:1453 所属专题:金属性 金属活动性
元素的金属性指的是元素原子的性质,是元素的气态原子失去电子变成气态阳离子倾向的大...
 [注解与辨疑a] 物质结构(必修)易错判断 作者:许雁祥 来源:未知 日期:2016-01-22 19:01:12 点击:743 所属专题:物质结构必修 是非判断
[注解与辨疑a] 物质结构(必修)易错判断 作者:许雁祥 来源:未知 日期:2016-01-22 19:01:12 点击:743 所属专题:物质结构必修 是非判断
( )1. 16 O 2 与 18 O 2 互为同位素,它们的性质基本相同。 ( )2. 第三周期元素的简单离子半径随原手序数的递增依次减...
 [注解与辨疑a] 氢的同位素的介绍 作者:舒次恩 来源:未知 日期:2021-05-07 08:51:54 点击:20452 所属专题:同位素
[注解与辨疑a] 氢的同位素的介绍 作者:舒次恩 来源:未知 日期:2021-05-07 08:51:54 点击:20452 所属专题:同位素
首先,我们来看看同位素的定义。同位素的定义如下:具有相同质子数和不同中子数的原子互称为同位素。 氢有三种同位素,即氕(读音:piē)、氘 (读音:dāo)、氚 (读音:chuān)。 氕〈读音〉piē,原子质量为1的普通的轻氢同位素。元素符号为 1 H,通常称为氢,它是氢的...
 [注解与辨疑a] 物质结构(必修)6类29条误区归纳 作者:赵宝 来源:未知 日期:2016-01-08 15:09:35 点击:3846 所属专题:物质结构必修
[注解与辨疑a] 物质结构(必修)6类29条误区归纳 作者:赵宝 来源:未知 日期:2016-01-08 15:09:35 点击:3846 所属专题:物质结构必修
1 、原子结构 ( 1 )所有元素的原子核都由质子和中子构成。 正例: 12 C 、 13 C 、 14 C 三原子质子数相同都是 6 ,中子数不同,分别为 6 、 7 、 8 。 反例 1 :只有氕( H )原子中没有中子,中子数为 0 。 ( 2 )所有原子的中子数都大于质子数。 正例 1 : C 、 C...
 [注解与辨疑a] 常用36元素的一些性质和用途 作者:周四 来源:未知 日期:2021-12-29 09:18:09 点击:7655 所属专题:短周期元素
[注解与辨疑a] 常用36元素的一些性质和用途 作者:周四 来源:未知 日期:2021-12-29 09:18:09 点击:7655 所属专题:短周期元素
氢( H ) 主要性质和用 熔点为 -259.1 ℃ ,沸点为 -252.9 ℃ ,密度为 0.08988g/L(10 ℃ ) 。无色无臭气体,不溶于水,能在空气中燃烧,与空气形成爆炸混合物。工业上用于制造氨、环已烷、甲醇等。 氦 (He) 主要性质和用途 熔点为 -272.2 ℃ (加压),沸点为- 268.9...
 [注解与辨疑a] 元素金属性及非金属性的比较方法 作者:章金莲 来源:未知 日期:2013-11-13 17:18:36 点击:12082 所属专题:金属性 非金属性
[注解与辨疑a] 元素金属性及非金属性的比较方法 作者:章金莲 来源:未知 日期:2013-11-13 17:18:36 点击:12082 所属专题:金属性 非金属性
一、元素金属性的比较方法 1 、用失去电子的难易比较:金属原子失去电子越容易,金属元素的金属性就越强;金属原子失去电子越不容易,金属元素的金属性就越弱。 例如:钠比镁更容易失去电子,钠金属性比镁强。 2 、用与水反应产生氢气的能力比较:金属越容易和水反应产生氢...
 [注解与辨疑a] 原子序数与化学式关系归纳 作者:陈爱玉 来源:未知 日期:2016-01-24 17:06:23 点击:2916 所属专题:原子序数 化学式
[注解与辨疑a] 原子序数与化学式关系归纳 作者:陈爱玉 来源:未知 日期:2016-01-24 17:06:23 点击:2916 所属专题:原子序数 化学式
原子序数与化学式的联系依靠化合价关联在一起,而化合价又主要取决于最外层电子数。原子序数决定了原子的核外电子排布,决定了最外层电子数,决定了在周期表的周期和族,也就决定了元素的化合价。原子序数就就主要通过主族序数和化学式关联在一起。 例如:AB 2 型的化合...
 [注解与辨疑a] 常见的含氧酸及其含氧酸盐的化学式 作者:李萱 来源:未知 日期:2014-01-11 17:34:16 点击:6052 所属专题:含氧酸 分子式
[注解与辨疑a] 常见的含氧酸及其含氧酸盐的化学式 作者:李萱 来源:未知 日期:2014-01-11 17:34:16 点击:6052 所属专题:含氧酸 分子式
1 、突破含氧酸及其含氧酸盐的化学式关键还是把握元素的化合价,一般来说,元素有什么样的化合价,就有什么样的含氧酸,也就有什么样的含氧酸盐。 Be H 2 BeO 2 、 Na 2 BeO 2 B HBO 2 、 H 3 BO 3 、 H 2 B 4 O 7 、 NaBO 2 、 Na 3 BO 3 、 Na 2 B 4 O 7 、 Al H 3 Al...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。一、研究历史 自然界中物质常见的存在形式有气态、液态和固态,决定物质状态的主要原...
...
【导读】键长和键能的关系在化学中通常表现为反比规律:键长越短,键能越大,但受原子...
人教版高中化学必修第一册2019年6月第1版2024年7月第8次印刷P 10 3 讲解卤素单质与氢...
冰在0℃开始融化。这是本家都熟悉的事儿。 然而,世界上竟有热冰它在3.8℃方才融化! ...
1. 为什么 HF 分子间氢键比 H 2 O 分子间氢键强,而 HF 的沸点却比 H 2 O 的低? 由于...
1、为什么氧、氟没有最高正价?(朱朝宇) 氟是非金属性最强的元素,理论上没有哪种物...
1.如何理解分子间作用力的本质也是静电作用? 首先,在极性分子与极性分子之间,存在...