
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
芬顿反应是以英国化学家H.J.H. 芬顿命名的无机化学反应,核心是在酸性条件下,由二价铁离子 (Fe²⁺)催化过氧化氢 (H₂O₂)分解,产生具有强氧化能力的羟基自由基 (・OH),从而实现对有机物的高效降解。
羟基自由基(·OH),由于它有一个没有配对的电子,故此是一种活性比活氧更强的氧化剂,作为中间态物质仅能存在1毫秒。
它的氧化性有多强呢?那是相当的强!
氟气(3.06eV)>羟自由基(2.85eV)>臭氧(2.07eV)>氯气(1.36eV)>氧气(1.23eV)
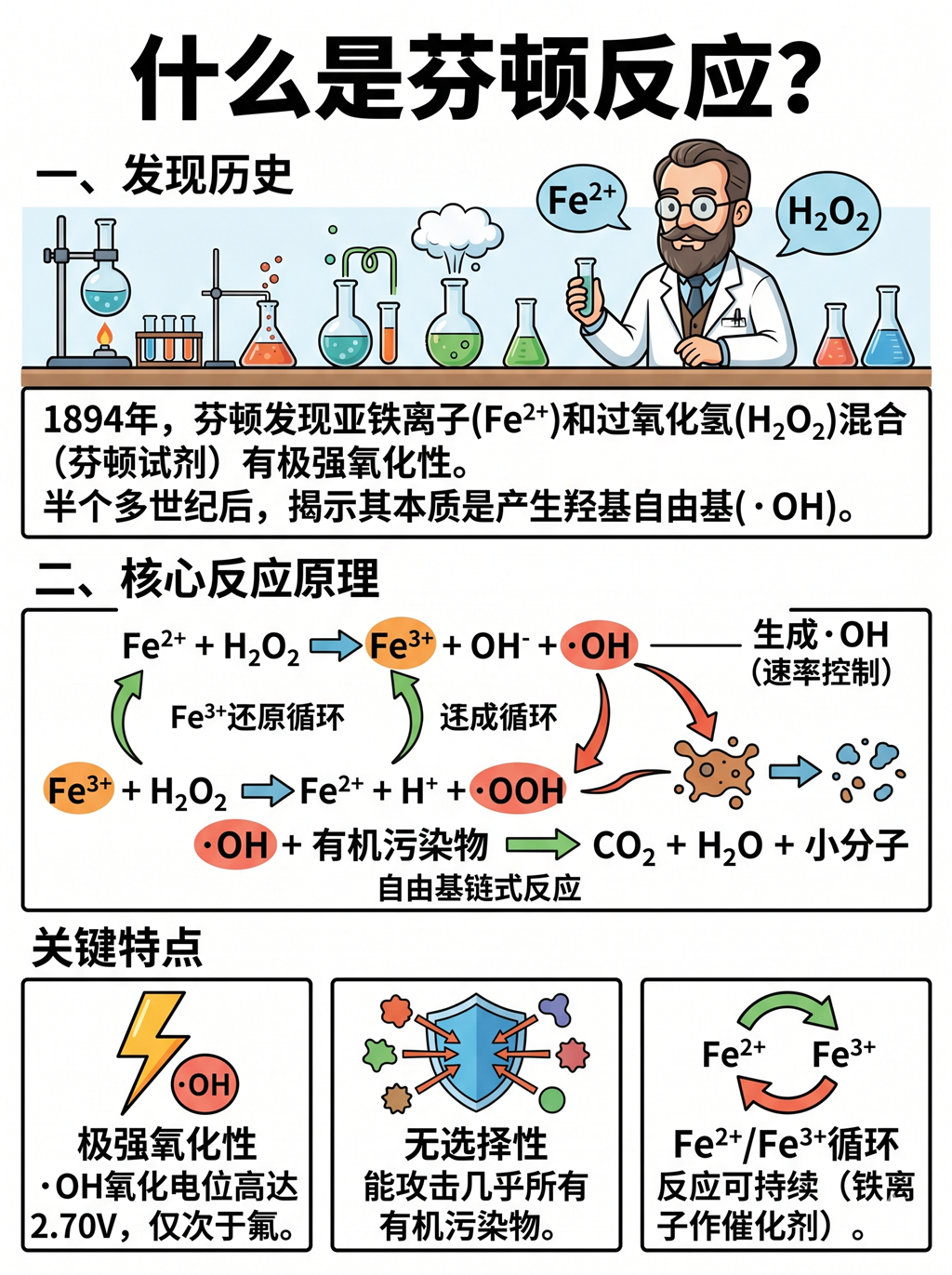
一、发现历史
1894 年,芬顿发现过氧化氢与二价铁离子的混合溶液(后称芬顿试剂)具有极强氧化性,能将多种有机化合物(羧酸、醇、酯等)氧化为无机态。
半个多世纪后,科学家才揭示其本质 —— 反应中产生了羟基自由基,这是导致其强氧化性的关键。
二、核心反应原理
芬顿反应是一个自由基链式反应,包含以下关键步骤:
初级反应(羟基自由基生成)
Fe²⁺ + H₂O₂ → Fe³⁺ + OH⁻ +・OH (速率控制步骤)
次级反应(Fe³⁺还原与循环)
Fe³⁺ + H₂O₂ → Fe²⁺ + H⁺ +・OOH (过氧羟基自由基)
自由基链式反应
・OH + 有机物 → 有机自由基 + H₂O
有机自由基 + O₂ → 过氧自由基 → 进一步氧化 → CO₂ + H₂O + 小分子有机物
关键特点:
羟基自由基氧化电位高达2.70V,仅次于氟,是极强的氧化剂
自由基反应无选择性,能攻击几乎所有有机污染物分子
Fe²⁺/Fe³⁺循环使反应可持续进行,铁离子起到催化作用
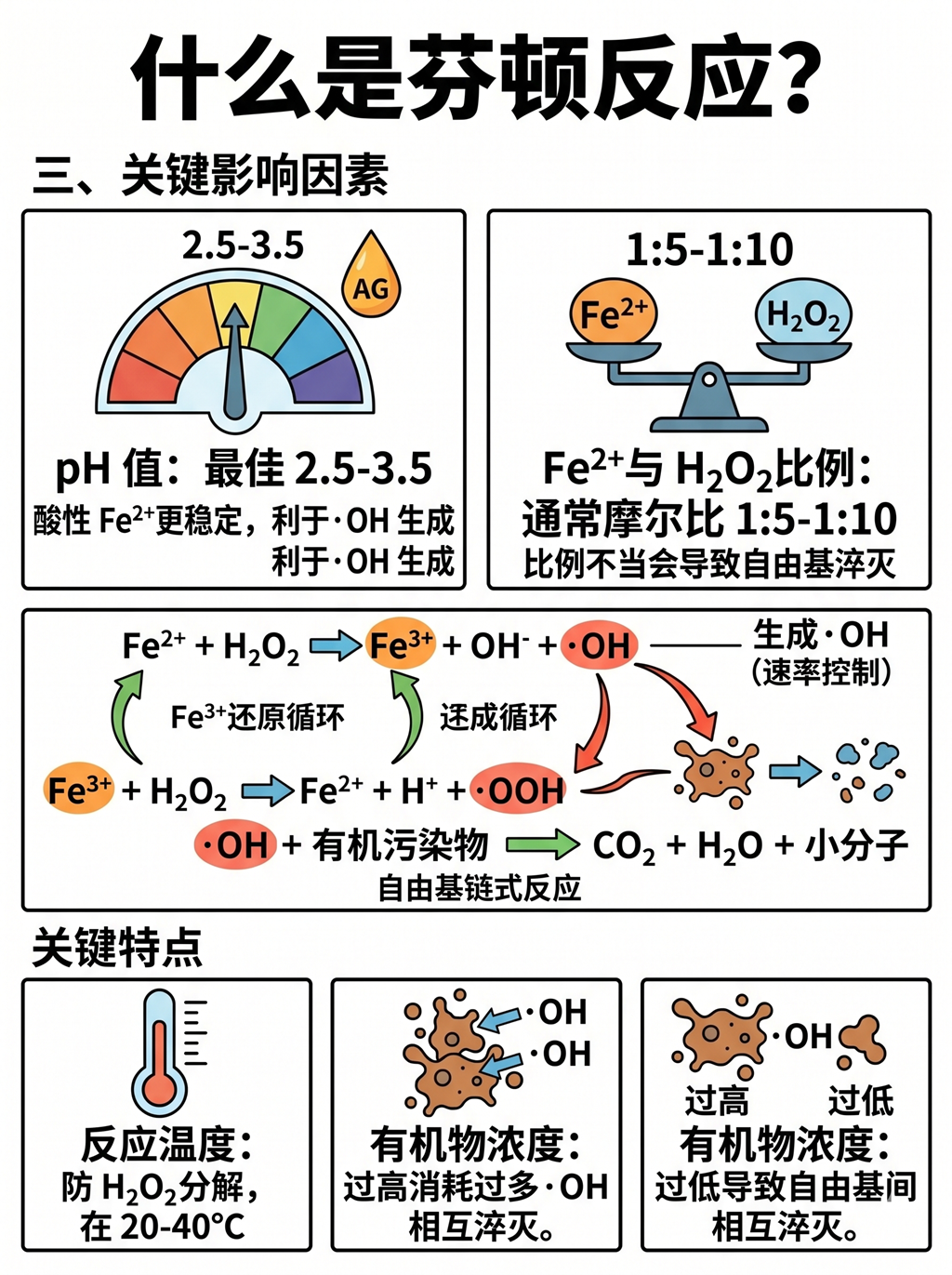
三、关键影响因素
pH 值:最佳范围为2.5-3.5,酸性条件下 Fe²⁺更稳定,且有利于・OH 生成
Fe²⁺与 H₂O₂比例:通常摩尔比为1:5-1:10,比例不当会导致自由基淬灭或利用率低
反应温度:温度升高可加速反应,但过高会导致 H₂O₂分解过快,一般控制在20-40℃
有机物浓度:过高会消耗过多・OH,过低则可能导致自由基间相互淬灭
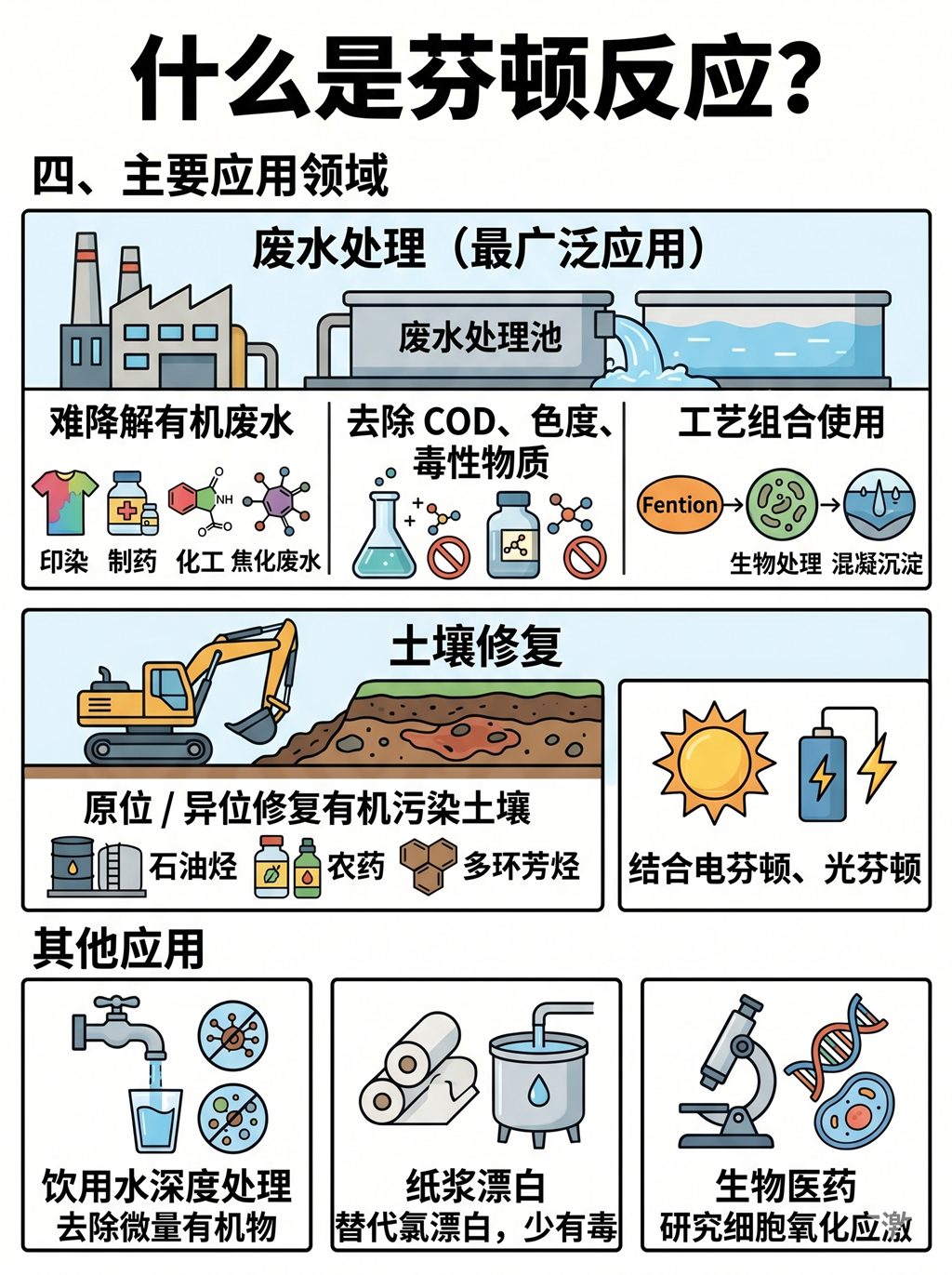
四、主要应用领域
废水处理(最广泛应用)
处理难降解有机废水:印染、制药、化工、焦化废水等
去除 COD、色度、毒性物质,提高废水可生化性
可与生物处理、混凝沉淀等工艺组合使用
土壤修复
原位 / 异位修复有机污染土壤,如石油烃、农药、多环芳烃等污染
可与电芬顿、光芬顿等技术结合,提高修复效率
其他应用
饮用水深度处理:去除微量有机污染物和消毒副产物前驱体
纸浆漂白:替代传统氯漂白,减少有毒物质生成
生物医药:研究细胞氧化应激、疾病机制及抗氧化剂筛选。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
芬顿反应是以英国化学家H.J.H. 芬顿命名的无机化学反应,核心是...
【导读】判断有机胺类碱性强弱的依据是“结构决定性质”。在...
苯酚是高中有机化学中结构决定性质的典型代表,其所有实验现...
...
氢键效应对有机酸酸性的影响主要体现在稳定其共轭碱,从而增...
一、根据元素电负性判断 电负性较大的原子或原子团通常表现为...