
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
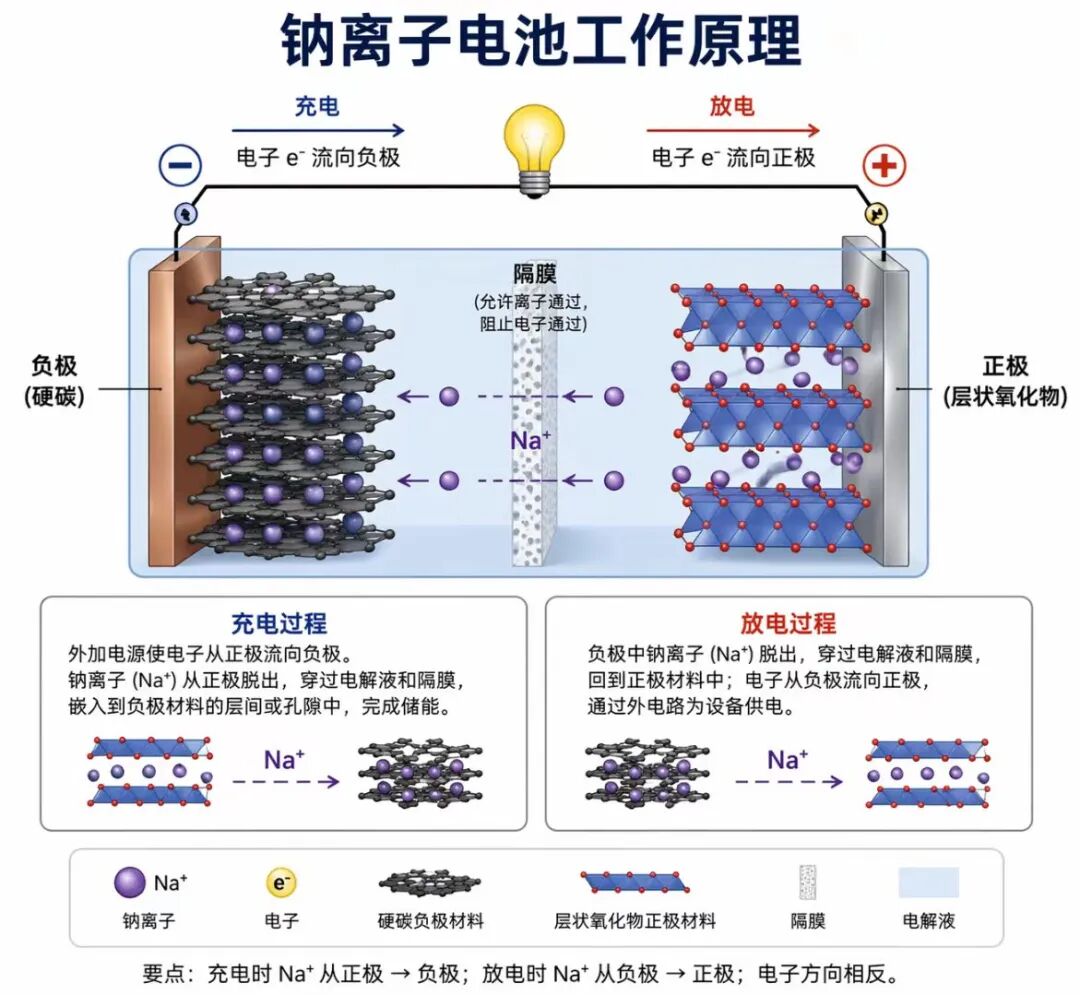
这张图清晰拆解了钠离子电池的核心工作逻辑,我们可以从核心结构、充电过程、放电过程三个维度,把它的原理彻底讲透。
一、核心结构:四大关键部件各司其职
钠离子电池的基础架构和锂电池类似,但用“钠离子”替代了锂离子作为载流子,核心部件分工明确:
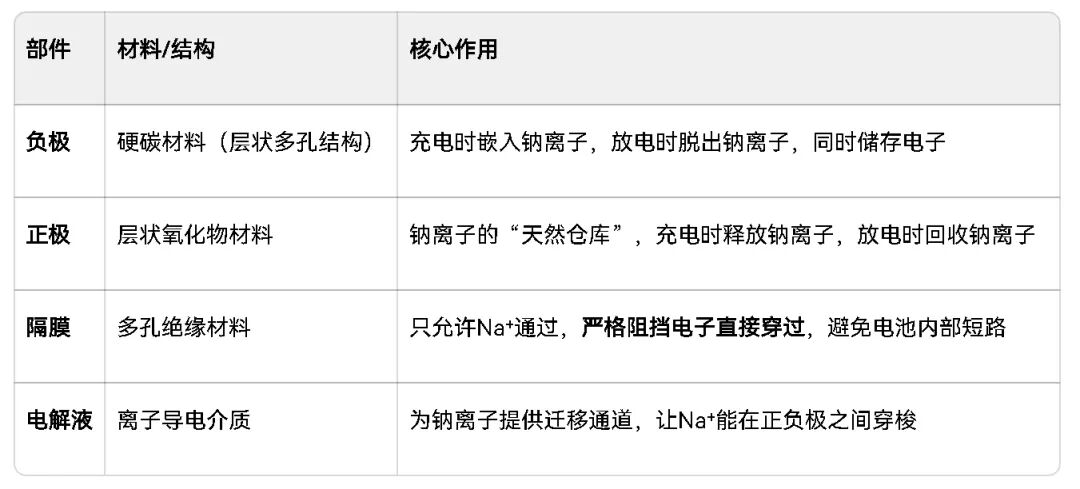
二、充电过程:把钠离子“送进”负极,把电能存起来
充电时,电池相当于一个“储能装置”,在外加电源的驱动下,离子和电子的移动方向完全可控:
1. 电子的路径:外加电源的作用下,电子(e⁻)从正极通过外电路,定向流向负极并被储存起来。
2. 钠离子的路径:为了维持电荷平衡,正极层状氧化物材料中的钠离子(Na⁺)会脱出,穿过电解液和隔膜,嵌入到负极硬碳材料的层间或孔隙中。
3. 最终结果:钠离子被“锁”在负极,电子也同步储存在负极,电能转化为化学能,电池完成储能。
三、放电过程:把钠离子“送回”正极,把化学能变成电能
放电时,电池成为“供电装置”,离子和电子自发反向移动,为外部设备供电:
1. 电子的路径:负极的电子(e⁻)通过外电路,流向正极,在流动过程中经过灯泡(负载),为设备供电。
2. 钠离子的路径:为了维持电荷平衡,储存在负极的钠离子(Na⁺)会脱出,再次穿过电解液和隔膜,回到正极层状氧化物材料中。
3. 最终结果:钠离子回到正极,电子和钠离子在正极“汇合”,储存在电池里的化学能,就转化成了设备能用的电能。
四、核心规律总结:钠离子和电子的“反向奔赴”
这张图的核心要点,也是钠离子电池的底层逻辑:
- 钠离子(Na⁺)的移动方向:充电时从正极→负极;放电时从负极→正极。
- 电子(e⁻)的移动方向:充电时从正极→负极;放电时从负极→正极。
- 电子和钠离子永远“不同路”:电子只能走外电路,钠离子只能走电解液+隔膜,二者必须在正极完成“电荷平衡”,电池才能持续工作。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
这张图清晰拆解了钠离子电池的核心工作逻辑,我们可以从核心...
...
锂离子蓄电池,负极材料是石墨,负极的充电反应为: xLi + +...
...
锂离子电池是二次可充放电电池,核心工作逻辑是锂离子的嵌脱...
在高考化学电化学模块中,带离子交换膜的电化学装置是绝对高...