
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
有机物中共价键的极性影响有机反应中化学键的断裂与形成,影响有机化合物分子中化学键的极性有:诱导效应、共轭效应、超共轭效应和场效应(本文不作介绍)。
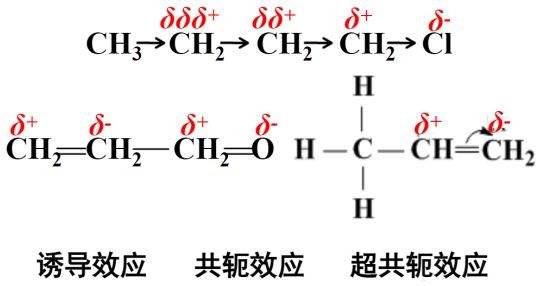
一、诱导效应
原子和基团的极性不同而引起成键电子云沿原子链向某一个方向移动的效应。特点:电子云沿原子链传导,诱导效应随距离增加而减弱。
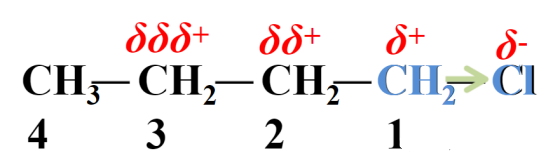
例1、比较甲酸、乙酸和丙酸酸性强弱。
羧酸 | PKa |
丙酸(C2H5COOH) | 4.88 |
乙酸(CH3COOH) | 4.76 |
甲酸(HCOOH) | 3.75 |
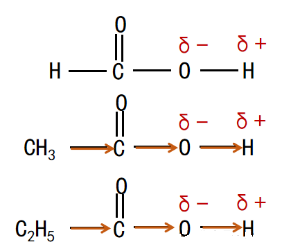
CH3和-C2H5为给电子基团(推电子基团),诱导效应使-OH中的共用电子对偏离O原子,羟基极性变小,酸性变弱。烃基越大,给电子诱导效应越明显。
给电子诱导效应:(CH3)3C- >(CH3)2CH->CH3CH2->CH3->H-
-CH3和-C2H5为给电子基团,带负电荷的基团具有给电子诱导效应
例2:比较Na与H2O和C2H5-OH反应的剧烈程度
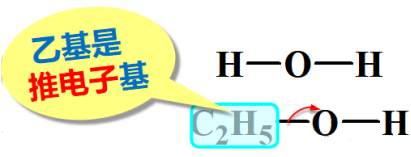
水与钠反应更剧烈,由于烷基是推电子基团,使醇分子中的O-H键的极性小于水分子中的氢氧键的极性,相较于水,乙醇分子中的O-H键不容易断裂。
例3、比较乙酸、氯乙酸、二氯乙酸和三氯乙酸酸性强弱
羧酸 | PKa |
乙酸(CH3COOH) | 4.76 |
氯乙酸(CH2ClCOOH) | 2.86 |
二氯乙酸(CHCl2COOH) | 1.29 |
三氯乙酸(CCl3COOH) | 0.65 |
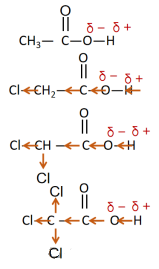
氯的电负性较大,吸电子基团诱导效应使-OH中的共用电子对偏离O原子,导致氯乙酸中的羟基的极性最大,更易电离出氢离子,酸性增强。
吸电子诱导效应:-NO2>-CN>-F>-Cl>-C≡CH>-OCH3>-OH>-C6H5>-CH=CH2>-H
(与C相连的原子电负性大,吸电子诱导效应明显;与碳原子直接连接的基团不饱和度大,吸电子诱导效应明显;带正电荷的基团具有吸电子诱导效应,带负电荷的基团具有给电子诱导效应)
例4:苯酚具有一定的酸性
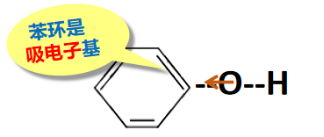
苯环吸电子基团,诱导效应使-OH中的共用电子对偏离O原子,导致羟基的极性最大,相对易电离出氢离子,酸性增强。
二、共轭效应
共轭体系中原子相互影响使体系的π电子(或P电子)分布发生变化的电子效应。
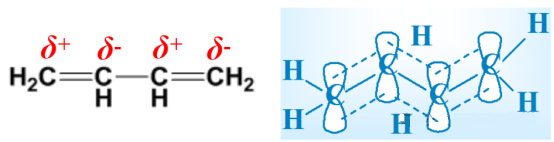
吸电子共轭效应:共轭体系上的基团能减小体系π电子密度
如:-NO2 -CN -COOH -CHO -COR
给电子共轭效应:共轭体系上的基团能增大体系π电子密度
-NH2 -OH -OR -OOCr -NHCOR
基团是否为供电子基团是由诱导效应和共轭效应(超共轭效应)共同决定的。
推电子诱导效应(+I)和推电子共轭效应(+C)的结果是基团表现为推电子,如:氧负离子(-O)、烷基(-R)
吸电子诱导效应(-I)小于推电子共轭效应(+C)的结果是基团表现为推电子,如:二烷基氨基(-NR2)、烷基氨基(-NHR)、氨基(-NH2)、羟基(-OH)、烷氧基(-OR)、酰胺基(-NHCOR)、酰氧基(-OOR)
下表给出醛基、氨基和氯原子的诱导效应、共轭效应与总的电子效应
结构简式 | 诱导效应 | 共轭效应 | 总的电子效应 |
CH2=CCH=CH-CHO | 吸电子 | 吸电子 | 吸电子 |
CH2=CCH=CH-NH2 | 吸电子 | 给电子 | 给电子 |
CH2=CCH=CH-Cl | 吸电子 | 给电子 | 吸电子 |
1.解释有机化合物的酸碱性
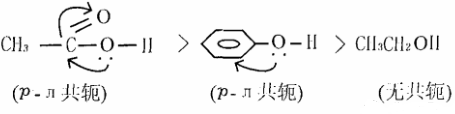
在羧酸和苯酚分子中,-OH中的氧原子上一对未共用的电子对占据的P轨道可以和C=O双键π键或苯环中的大π键形成共轭体系,增大0-H键的极性,促使H容易以H+的形式脱去,而且形成羧酸负离子或酚氧负离子后,共扼效应增强,体系更趋稳定,因此使羧酸或苯酚显酸性;而醇一般为中性,其原因就是醇中无p一π大共轭体系。
2.解释有机反应速率
苯环上的硝基对氯苯水解速率的影响。
| 反应物 | 反应条件 | 产物 |
氯苯+碱OH- | NaHCO3溶液中煮沸数天 | 无反应 |
邻硝基氯苯+碱OH- | NaHCO3溶液中加热到130度 | 邻硝基苯酚 |
2,4-二硝基氯苯+碱OH- | NaHCO3溶液中加热到100度 | 2,4-二硝基苯酚 |
2,4,6-三硝基氯苯+碱OH- | NaHCO3溶液中加热到30度 | 2,4,6-三硝基苯酚 |
﹣NO2是很强的吸电子基团,其中的N = O中π键可以和苯环中的大π键形成π-π共轭体系,硝基具有强的共轭效应,-NO2的加入,使苯环上电子云密度降低,亲核试剂OH-就容易进攻,而且﹣NO2处于邻对位时,这种共轭效应能够得到有效传递,-NO2数越多,整个吸电子共轭效应越强,化学反应速率越快。
3.预测有机反应产物
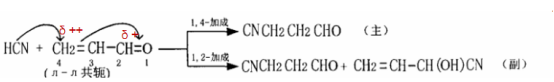
C=O是吸电子基团,C=O与C=C形成π-π共轭体系,其结果是4号C上的正电荷比2号C上多,由此预测CN-主要加在4号C上,即该反应主要按1,4-加成方向进行。
三.σ-π超共轭
超共轭效应都是向π键给电子的
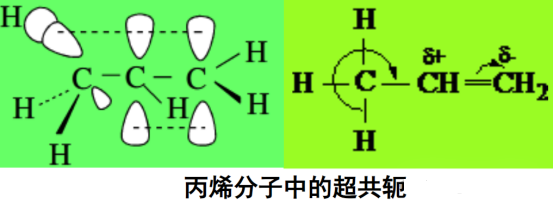
丙烯分子中的甲基可绕C—Cσ键旋转,旋转到某一角度时,甲基中的C-Hσ键与C=C的π键在同一平面内,C-Hσ键轴与π键P轨道近似平行,形成σ-π共轭体系,称为σ-π超共轭体系。
其结果是甲基上C-H的电子向π键离域,该C-H键的极性变强,H原子更容易被取代。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
疑问1:王后雄《重难点手册》选修5《有机化学基...
表1.二甲苯异构体的熔沸点比较 提出问题 1.沸点:邻二甲苯>间...
在高中化学中,能用来比较熔沸点的方法不少,比如氢键、相对...
【导读】有机物中“支链越多,熔沸点越低”的规律,更准确地...
...
高中化学选择性必修3《有机化学基础》里,卤代烃的物理性质一...