
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
所谓密堆积原理是指由无方向性的金属键、离子键和范德华力等结合的晶体中,原子、离子和分子等微粒总是趋向于相互配位数高,堆积密度大,能充分利用空间,因而体系稳定的那些结构。金属原子的电子云分布基本上是球对称的,可以把同一种金属晶体看成是由半径相等的圆球构成,因此金属晶体的结构可用等径圆球的密堆积模型来研究。常见的堆积形式有:A1、A2、A3和A4等。

A1(立方最密堆积,ccp,记为 A1型)和A3(六方最密堆积,hcp,记为A3型)堆积是等径球的密置层以两种不同方式堆积而成的最密堆积。
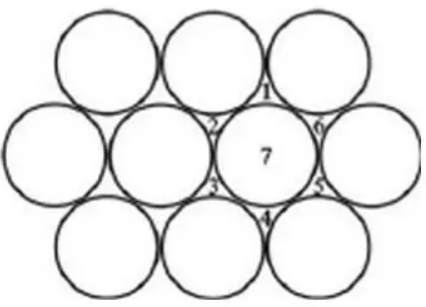
如图所示,每个球与6个球紧密接触,形成6个三角形空隙,其中1、3、5三角形空隙的底边在下、顶点在上,2、4、6三角形空隙的底边在上、顶点在下。
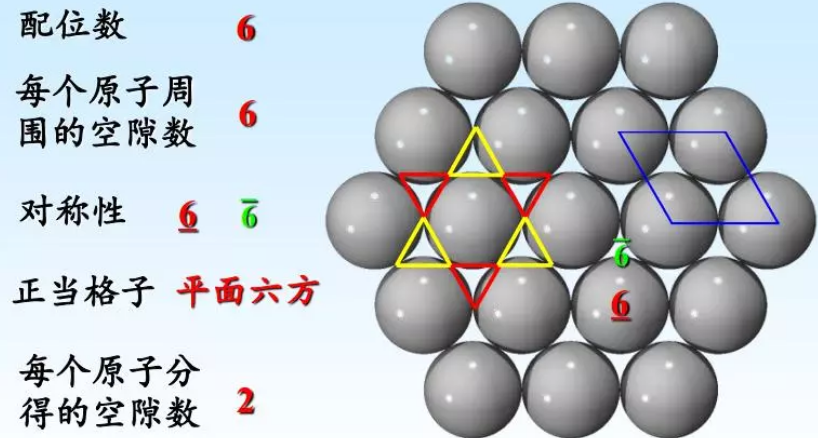
在堆积第二层等径球时,这个密置层中圆球的凸出部位正好处于第一密置层的凹陷部位,也就是一个球同时与第一密置层的三个球接触,它可以占据1、3、5空隙,也可占据2、4、6空隙,但不会两者都占,也不会混合占据。如果占据1、3、5空隙,第一密置层中的1、3、5三角形空隙转化成密置双层中的底面在下、顶点在上的正四面体空隙T+,见图(a)。而2、4、6三角形空隙转化成正八面体空隙O,见图(c)。注意在7位还有一个底面在上、顶点在下的正四面体空隙T-,见图(b)。
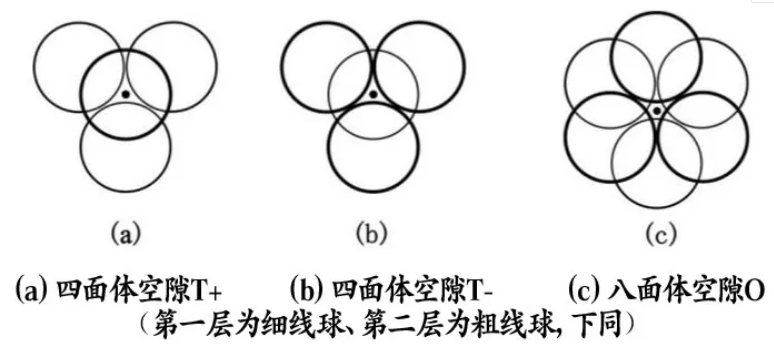
两个密置层间形成的空隙种类及分布下图所示。
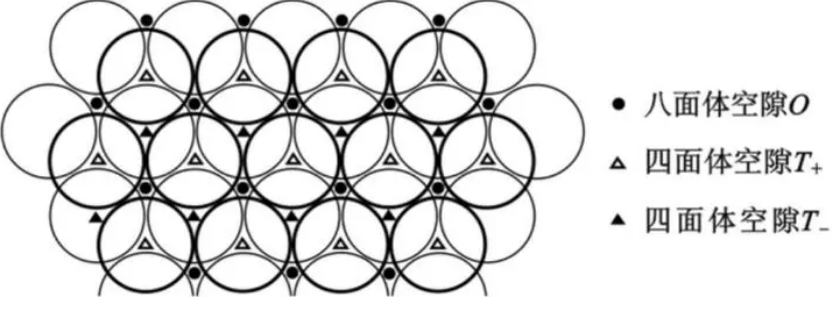
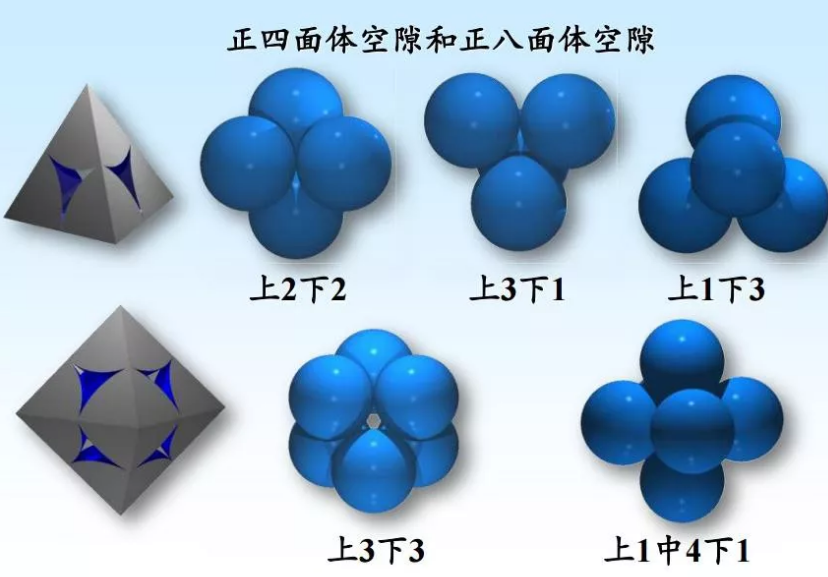
在这两种堆积方式中,任何四个相切的球围成一个正四面体空隙;另外,相切的三个球如果与另一密置层相切的三个球空隙对应,它们六个球将围成一个正八面体空隙。
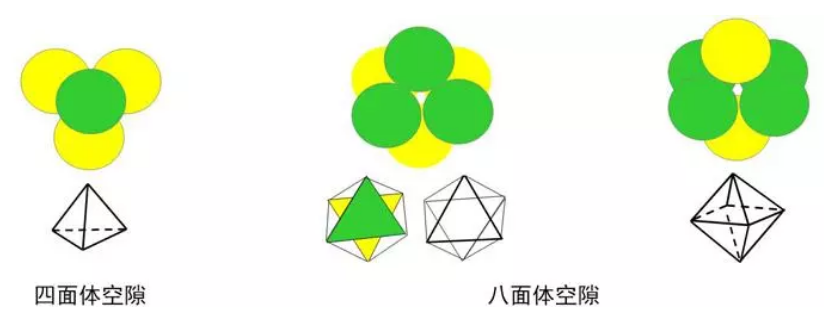
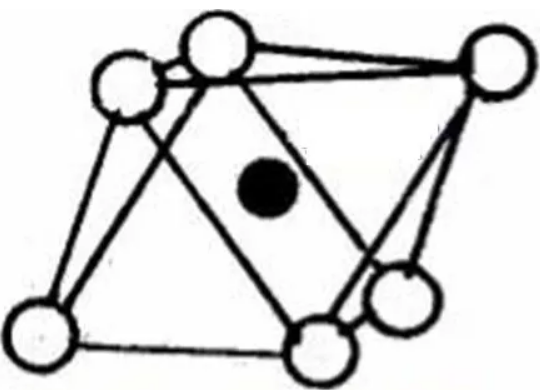
也就是说,围成正八面体空隙的这六个球可以分为相邻的两层,每层的正三角形中心的连线垂直于正三角形所在的密置层,参看下图,黑色代表的不是球而是正八面体的中心。
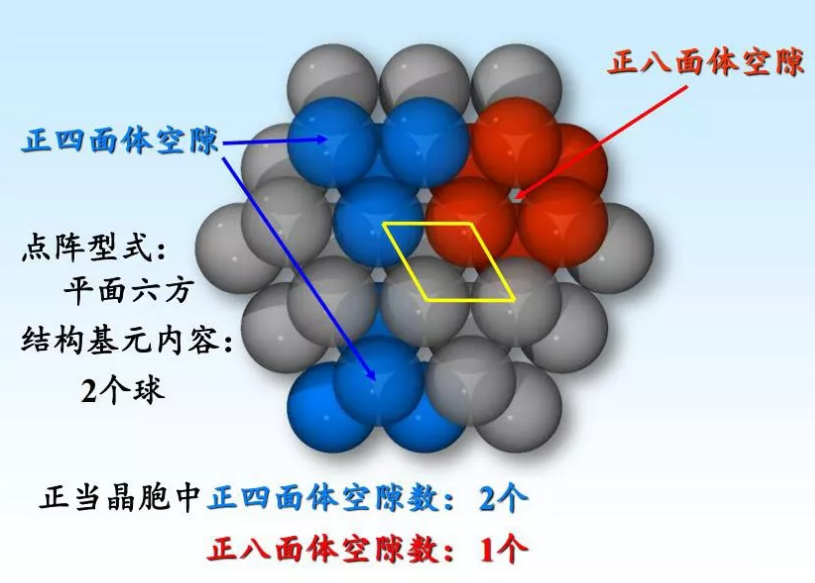
在这两种最密堆积方式中,每个球与同一密置层的六个球相切,同时与上一层的三个球和下一层的三个球相切,即每个球与周围十二个球相切(配位数为12)。中心这个球与周围的球围出八个正四面体空隙,平均分摊到每个正四面体空隙的是八分之一个球。这样,每个正四面体空隙分摊到的球数是四个八分之一,即半个。中心这个球周围还围出六个八面体空隙,它平均分摊到每个正八面体空隙的是六分之一个球。这样,每个正八面体空隙分摊到的球数是六个六分之一,即一个。总之,这两种最密堆积中,球数 : 正八面体空隙数 : 正四面体空隙数 = 1:1:2 。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
一、四大晶体类型,过渡晶体和混合晶体: 固体分为晶体和非晶...
1、从2009年江苏高考最后一问谈起 试题在1个Cu 2 O晶胞中(如图1所...
在晶体结构中,阳离子周围的阴离子总配位数,等于阴离子周围...
配位数之比(阳离子配位数:阴离子配位数)等于化学式角码反比...
一、金刚石结构 二、二氧化硅 三、氯化钠 插入投票 投票: 高...
第二页...