
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
浓硫酸是一种氧化性相当强的氧化剂,尤其是在加热时,绝 大多数金属都能和浓硫酸反应;而稀硫酸只能与金属活动性顺序中位于氢前面的金属反应,这种差别的原因是什么呢?
我们知道,浓硫酸中,硫酸是以分子状态存在,或者说多数 是以分子状态存在。硫酸的分子结构是不对称的,4个S—O键的长度都不一样。
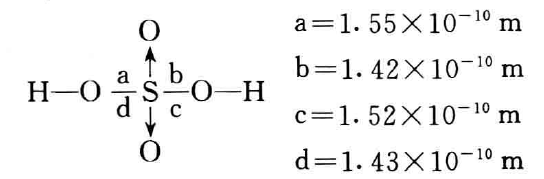
这是因为在硫酸分子中,氢原子很小,有很强的极化能力,使 硫酸根中的氧原子与硫原子的结合力减弱,从而破坏了硫酸根的 空间结构,减弱了它的稳定性,这就使硫原子很容易接受外来电 子,所以浓硫酸具有很强的氧化性。加热浓硫酸时,使硫酸分子 的内能增大,增大了分子原子间的相对振动的振幅,从而使硫酸根的结构更容易破裂,所以热的浓硫酸的氧化性更强。
稀硫酸几乎完全电离成H+和SO42-,而电离成的SO42-是对 称的正四面体结构,4个氧原子与硫原子之间的键长完全一样,都 是1.44×10-10m,故比较稳定,因而稀硫酸中的硫原子没有氧化 性,起氧化作用的是H2SO4电离出的H+。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
将一过程设计成原电池,方法和步骤如下: (1)将此过程分解...
...
电化学中的电极,是一个由电子导体(如金属)和 离子导体(如...
催化剂的催化能力一般叫做催化活性。各种催化剂都具有一定的...
从原始人用的天火到今天熟食用的煤气火以及科威特的油田大火...
在原电池中,理论上,是在负极上发生氧化反应,在正极上发生...