
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、问题的提出
在稀释弱电解质浓溶液时,一般为什么开始时溶液的导电性逐渐增强,以后又逐渐减弱?为了帮助同学们正确理解和回答这个问题,我们设计了下述实验。
二、实验步骤及数据
1、试剂:冰醋酸(CH3COOH含量≥99.0%,密度1.05g/mL)、蒸馏水。
2、仪器:电流计、直流稳压电源、100mL烧杯、石墨电极。
3、装置图及实验步骤
①按下图装置先测出电流通过冰醋酸、蒸馏水时的电流强度。
②再用同样的方法测出电流通过不同浓度的醋酸溶液时的电流强度。
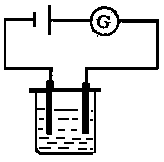

(注意:整个实验过程中,实验操作条件保持不变。石墨电极要求清洁、干燥。)
4、实验数据记录
电流通过冰醋酸(浓度为17.33mol/L)和蒸馏水时的电流强度分别为15μA和86μA,电流通过其他浓度的醋酸溶液时的电流强度如上表。
5、绘制醋酸浓度和电流强度的曲线图,以醋酸浓度C为横座标,以电流计读数I,用mA表示)为纵座标,作出I—C曲线图。
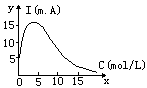
三、结论和解释
1、冰醋酸的导电性比蒸馏水的还弱得多(它几乎不导电),这是因为冰醋酸(本实验是在20℃时做的,此时冰醋酸系液态)含水极少,它几乎不发生电离之故。
2、加水稀释冰醋酸,直至浓度为2mol/L左右时,在这个浓度范围内(17.33至2mol/L),随着溶液的稀释,醋酸的电离度逐渐增大,自由移动离子的浓度也增大(溶液体积虽然增大,但它处于矛盾的次要方面),所以溶液的导电性逐渐增强。
3、当浓度在2mol/L以下再加水稀释时,虽然醋酸的电离度仍在逐渐增大,但这一过程中溶液体积的增大已成为矛盾的主要方面,致使溶液自由移动离子的浓度逐渐减小,因此溶液的导电性逐渐减弱。
4、对于其他易溶于水的弱电解质溶液的导电性与溶液浓度的关系也能得出相似的结论(如氨水等)。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
在化学研究与教学实践中,醋酸钠溶液作为强碱弱酸盐的典型代...
1.减小偶然误差 (1)终点判断的主观性:不同人对颜色变化的敏...
一、何谓热冰 冷却的醋酸钠过饱和溶液,暂时处于亚稳态。当受...
问题:测溶液pH能否使用胶头滴管? 讨论1:用胶头滴管吸取溶液...
pH值是什么? pH值,也称氢离子浓度指数、酸碱值,是溶液中氢...
中和滴定 水液洗器切分明, 查漏赶气再调零。 待测液中加试剂...