
|
学习小专题 |
 探究硝酸溶解碘化银的条件
日期:2022-11-29 15:04:18
点击:1834
好评:0
探究硝酸溶解碘化银的条件
日期:2022-11-29 15:04:18
点击:1834
好评:0
在中学化学 ,检验溶液中是否存在 I- ,其方法是取 少量试液于试管中,并向其中滴加 AgNO 3 (aq), 有黄色 沉淀产生后,再滴加稀 HNO 3 ,如果黄色沉淀不溶解,则 证明溶液中存在「。但当我们认识到「具有强还原 性 ,HNO 3 具有强氧化性,两者之间易发生氧化还原反应 8H*+2...
 巧记硝酸性质口诀
日期:2022-08-06 17:14:08
点击:4625
好评:1
巧记硝酸性质口诀
日期:2022-08-06 17:14:08
点击:4625
好评:1
用口诀记忆那些较繁杂,易混淆的知识是一个好办法。例如高中一年级化学教材中关于硝酸的性质,就可以编成如下口诀: 硝酸金属铜,反应不放氢(1); 稀硝三八无(2),浓硝一四棕(3); 铝铁能钝化(4),光热不稳定(5); 一硝三盐王,能把金铂溶(6)。 这个口诀基本概括了硝酸...
 氨 硫酸 硝酸知识要点
日期:2017-08-08 19:35:33
点击:5262
好评:0
氨 硫酸 硝酸知识要点
日期:2017-08-08 19:35:33
点击:5262
好评:0
一、氮的固定 氮气转化为氮的化合物称为氮的固定。分自然固氮和人工固氮 二、氨 1、氨的组成 分子式:NH 3 , 相对分子质量:17 摩尔质量:17g/mol 2、氨的物理性质 [实验4-8]氨的喷泉实验 实验内容 实验现象 解释与结论 教材实验4-8 形成红色喷泉 氨气易溶于水,少量...
 化学小论文:神奇的硝酸
日期:2016-01-21 15:54:24
点击:1571
好评:0
化学小论文:神奇的硝酸
日期:2016-01-21 15:54:24
点击:1571
好评:0
你知道三大强酸吗?对,它们是盐酸(HCl)硫酸(H 2 SO 4 )、硝酸这三种由非金属形成的无机酸。相信前两者对于大家来说一定不会陌生,因为在初中的《自然科学》中我们就和它们打地交道了。今天,我要向大家介绍的便是酸大家放族的重要一员―硝酸(HNO 3 )。 细心的同学也许...
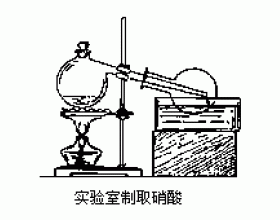 实验室制取硝酸
日期:2016-01-21 15:11:30
点击:9076
好评:1
实验室制取硝酸
日期:2016-01-21 15:11:30
点击:9076
好评:1
[原理] NaNO 3 +H 2 SO 4 (浓)=NaHSO 4 +HNO 3 ↑ [用品] 曲颈甑、圆底烧瓶、水槽、酒精灯、铁架台、石棉网 、 固体硝酸钠、浓硫酸 [操作] 在曲颈甑内装入20g硝酸钠和20mL浓硫酸,先用小火加热,然后再逐渐升高温度,即可看见接受器的圆底烧瓶中,有硝酸蒸气冷凝而成...
 硝酸的计算
日期:2016-01-21 15:08:04
点击:16594
好评:1
硝酸的计算
日期:2016-01-21 15:08:04
点击:16594
好评:1
与硝酸有关的计算由于涉及到原子守恒、得失电子守恒,所以在题目中较为常见,在实际问题中硝酸有关的计算主要可归纳为以下几种情况: 1、依据得失电子守恒的计算 例1:1.92 g铜投入到一定量浓硝酸中,铜完全溶解,生成气体颜色越来越淡,将收集到的气体与一定体积的氧气...
 硝酸的氧化性规律小结
日期:2016-01-19 23:58:01
点击:4772
好评:0
硝酸的氧化性规律小结
日期:2016-01-19 23:58:01
点击:4772
好评:0
硝酸在中学化学中有着举足轻重的作用,它除了具有强酸的性质外,实际上在有关试题中更多的是关注它的氧化性。本文就硝酸的氧化性作一小结,以期加深对硝酸氧化性的认识和理解。 一、硝酸氧化性的具体体现 Fe(NO 3 ) 3...
 如何理解浓、稀硝酸氧化性的强弱?
日期:2016-01-19 22:10:58
点击:7654
好评:0
如何理解浓、稀硝酸氧化性的强弱?
日期:2016-01-19 22:10:58
点击:7654
好评:0
有人说,浓HNO3与Cu反应产生NO2,稀HNO3与Cu反应产生NO,则稀HNO3氧化性更强,这种说法对吗? 有人从硝酸与铜反应时浓硝酸被还原为NO2,稀硝酸被还原为NO这一事实出发,认为稀硝酸被还原程度比浓硝酸大,稀硝酸的氧化性应该比浓硝酸强。其实,这是对物质氧化性强弱标准...
 硝酸的氧化性易错点剖析
日期:2014-06-11 14:59:19
点击:737
好评:0
硝酸的氧化性易错点剖析
日期:2014-06-11 14:59:19
点击:737
好评:0
1、一定量的浓硝酸与足量的铜片反应时,还原产物开始是二氧化氮,随着反应的进行,硝酸的浓度变小,后来会生成一氧化氮。 [例题]38.4 Mg 铜跟适量的浓硝酸反应,铜全部反应后,共收集到 22.4 mL 气体(标准状况下)。反应消耗的 HNO 3 的物质的量可能是( )。 A、1.0×10 -3...
 课件学习:硝酸
日期:2012-05-22 17:36:45
点击:299
好评:2
课件学习:硝酸
日期:2012-05-22 17:36:45
点击:299
好评:2
...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。