
|
ѧϰСר�� |

|
ѧϰСר�� |
 [���������9] ����Ũ�����ϡ�����13�ַ��� ����:��Ⱥ ��Դ:δ֪ ���ڣ�2021-01-19 15:07:09 �����12503 ����ר�⣺���ʼ���04 Ũ����
[���������9] ����Ũ�����ϡ�����13�ַ��� ����:��Ⱥ ��Դ:δ֪ ���ڣ�2021-01-19 15:07:09 �����12503 ����ר�⣺���ʼ���04 Ũ����
1�����ط���Ũ�����ϡ�����ܶȴ�98%��Ũ�����ܶ�Ϊ1.84g/mL�������ص���Ũ���ᡣ 2��ճ�ȷ���Ũ������ճ����Һ�壬��ϡ������ӽ���ˮ��ճ�ȣ����Խ��Լ�ƿ����ҡ������ 3���е㷨�������Ǹ߷е���ᣬ98%��Ũ����е�Ϊ338�棬�ʿ�ȡ�������Թ��м��ȣ��ȷ������д�...
 [���������9] ����ļ��� ����:��Ǭ�� ��Դ:δ֪ ���ڣ�2016-01-21 15:08:04 �����16547 ����ר�⣺����
[���������9] ����ļ��� ����:��Ǭ�� ��Դ:δ֪ ���ڣ�2016-01-21 15:08:04 �����16547 ����ר�⣺����
�������йصļ��������漰��ԭ���غ㡢��ʧ�����غ㣬��������Ŀ�н�Ϊ��������ʵ�������������йصļ�����Ҫ�ɹ���Ϊ���¼�������� 1�����ݵ�ʧ�����غ�ļ��� ��1��1.92 gͭͶ�뵽һ����Ũ�����У�ͭ��ȫ�ܽ⣬����������ɫԽ��Խ�������ռ�����������һ�����������...
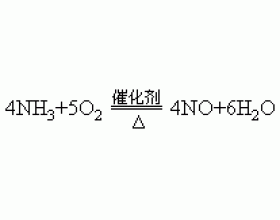 [���������9] ���ڰ�������������ļ������ ����:���� ��Դ:δ֪ ���ڣ�2012-05-15 14:41:29 �����4990 ����ר�⣺���Ṥҵ ��ϵʽ��
[���������9] ���ڰ�������������ļ������ ����:���� ��Դ:δ֪ ���ڣ�2012-05-15 14:41:29 �����4990 ����ר�⣺���Ṥҵ ��ϵʽ��
���������������ԭ���� 2NO+O 2 = 2NO 2 3NO 2 +H 2 O= 2HNO 3 + NO ����������ʽ��������������Ĺ�ϵʽ�ƺ�Ӧ��3NH 3 ��2HNO 3 ����ҵ������NOҪ����ѭ���������������ѭ����������ȫ��ת��Ϊ���ᣬ���ϵʽӦΪ��NH 3 ��HNO 3 ��...
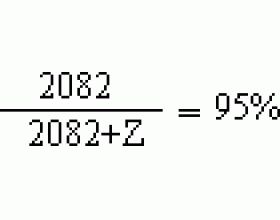 [���������9] ��������ϡ�ͼ��� ����:������ ��Դ:δ֪ ���ڣ�2016-01-21 14:30:59 �����9924 ����ר�⣺Ũ���� ��Һϡ��
[���������9] ��������ϡ�ͼ��� ����:������ ��Դ:δ֪ ���ڣ�2016-01-21 14:30:59 �����9924 ����ר�⣺Ũ���� ��Һϡ��
[ �� ] ���� 1L �� SO 3 Ϊ 30% �ķ������ᣨ�ܶ�Ϊ 1.95g/cm 3 ����Ҫ����ϡ�ͳ�Ϊ 95% ��Ũ���ᡣ����Ҫ�����м���ˮ������� [ ���� ] ѧ���ԡ��� SO 3 Ϊ 30% �ķ������ᡱ�����岻̫��ȷ��ͬʱ��ˮ���ܶ�Ϊ 1g/cm 3 ��Ҳ�������������� 1L �е�λ�� L �����ܶ��е�...
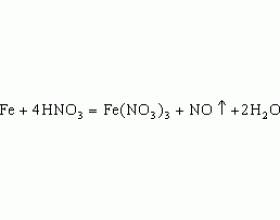 [���������9] ����ϡ���ᷴӦ���� ����:��� ��Դ:δ֪ ���ڣ�2021-04-19 14:41:44 �����29577 ����ר�⣺��������
[���������9] ����ϡ���ᷴӦ���� ����:��� ��Դ:δ֪ ���ڣ�2021-04-19 14:41:44 �����29577 ����ר�⣺��������
����ϡ����ķ�Ӧ�뷴Ӧ������йأ�ԭ�����ڽ������б�ۡ���������Ƚϸ��ӣ����ɽ������£� һ. ֪ʶ���� �漰�Ļ�ѧ��Ӧ����ʽ�� ��1�� ��2�� �������ʾ���£� ����ϡ���ᷴӦ������Թ���Ϊ�� 1. ��������� �� ������ʣ�ࣻ 2. ��������� �� ������ʣ�ࣻ 3. ��...
 [���������9] �ȵ����ʣ�����һ���й�N2H4����Ϣ������ ����:������ ��Դ:δ֪ ���ڣ�2020-03-05 18:51:26 �����19309 ����ר�⣺���� ��
[���������9] �ȵ����ʣ�����һ���й�N2H4����Ϣ������ ����:������ ��Դ:δ֪ ���ڣ�2020-03-05 18:51:26 �����19309 ����ר�⣺���� ��
��Ŀ 1 ���������������ش� 1~3 �⣺ �� N 2 H 4 �� ��Ϊ�»������� N 2 H 4 �� NH 3 �Ĺ�ϵ�� H 2 O 2 �� H 2 O �Ĺ�ϵ����֪ N 2 H 4 �ܷ������з�Ӧ�� N 2 H 4 + H 2 O N 2 H 5 + + OH -- N 2 H 5 + + H 2 O N 2 H 6 2+ + OH -- N 2 H 4 + H 3 O + N 2 H 5 + + H 2 O...
 [���������9] NO2��NO��O2�����������ˮ�ļ��� ����:�°��� ��Դ:δ֪ ���ڣ�2016-01-21 13:46:12 �����26385 ����ר�⣺��������
[���������9] NO2��NO��O2�����������ˮ�ļ��� ����:�°��� ��Դ:δ֪ ���ڣ�2016-01-21 13:46:12 �����26385 ����ר�⣺��������
�������ɣ� NO 2 �� NO �� O 2 �������к����ֻ����ֵĻ��������ˮ�й��������ɣ������ijɷݵ��жϿ��������з���ʽ�� �� 3NO 2 +H 2 O==2HNO 3 +NO �� ��2 NO+O 2 ==2NO 2 �� ��4 NO 2 +O 2 +2H 2 O==4HNO 3 �� ��ʽ���ɢ� �w 2+ �ڵõ��� ��4 NO+3O 2 +2H 2 O==4HN...
 [���������9] ����ϡ�����Ũ���� ����:�Ű� ��Դ:δ֪ ���ڣ�2016-01-21 13:56:51 �����7749 ����ר�⣺���ʼ���04 ϡ���� Ũ����
[���������9] ����ϡ�����Ũ���� ����:�Ű� ��Դ:δ֪ ���ڣ�2016-01-21 13:56:51 �����7749 ����ר�⣺���ʼ���04 ϡ���� Ũ����
1�����ط���Ũ�����ϡ�����ܶȴ�98%��Ũ�����ܶ�Ϊ1.84g/mL�������ص���Ũ���ᡣ 2��ճ�ȷ���Ũ������ճ����Һ�壬��ϡ������ӽ���ˮ��ճ�ȣ����Խ��Լ�ƿ����ҡ�����£��Ϳɿ����ĸ���Ũ���ᣬҺ�����ʱ��ȡ�������Թ����� 3���е㷨�������Ǹ߷е���ᣬ98%...
 [���������9] �����仯����������� ����:���� ��Դ:δ֪ ���ڣ�2016-01-21 13:59:29 �����8534 ����ר�⣺�����仯����
[���������9] �����仯����������� ����:���� ��Դ:δ֪ ���ڣ�2016-01-21 13:59:29 �����8534 ����ר�⣺�����仯����
1����Ԫ�ص縺�Խϴǽ����Խ�ǿ���������µ����Ļ�ѧ���ʲ����á���Ϊ�������е����������ܴ��Ե�ʡ� 2����IIA��Ԫ�ص���ֻ��Be����N 2 ��Ӧ�� 3����������������г�N 2 O 3 ��N 2 O 5 �ֱ�Ϊ�������������⣬������������ 4��ͨ����NO 2 ��������Ϊ����NO 2 ��N ...
 [���������9] ���仯�����һ�������� ����:��� ��Դ:δ֪ ���ڣ�2016-01-21 13:59:57 �����10646 ����ר�⣺���仯����
[���������9] ���仯�����һ�������� ����:��� ��Դ:δ֪ ���ڣ�2016-01-21 13:59:57 �����10646 ����ר�⣺���仯����
1��һ����ͽ�����Ӧ���������ף�������������ȴ�ڳ����·�Ӧ���������ܡ� 2Ag��S==Ag 2 S��Hg��S==HgS�� 2���������ۺ���۵Ļ���������Al 2 S 3 ��������ͨ����Һ�еĸ��ֽⷴӦ�Ʊ�Al 2 S 3 ����Ϊ2Al 3+ +3S 2 - +6H 2 O==2Al(OH) 3 ��+3H 2 S���� 3�����������...
 ��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ�
��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ� ��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء�
��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء�һ������ ����ɫ���ܽ��Թ���: ���� (Ag 2 S) ���Һ�ɫ��������ˮ������Ũ����...
���� 1�� ��ij100ml�Ļ��Һ�У�����������������Ũ�ȷֱ���0.4mol/L,0.1mol/L,���...
ͭ������ķ�Ӧ�����������ǿ������������ , Ũ�����ڷ�Ӧ��������ϡ , ��ɲ���...
������Mg��Cu��ɵ�2.64�˻����Ͷ������ϡ������ǡ�÷�Ӧ,������ȫ�ܽ�ʱ�ռ��Ļ�ԭ...
�����������ǿ�����ԣ���������˳����г�Pt��Au��������н�����Ӧ������Ũ����...
������������NO��NO 2 ��N 2 O 4 �ȣ���ֻ��NO 2 ��ֱ����ˮ������Ӧ��3NO 2 +H 2 O==...
����ϡ����ķ�Ӧ�뷴Ӧ������йأ�ԭ�����ڽ������б�ۡ���������Ƚϸ��ӣ����ɽ�...
ͭ������ķ�Ӧ�����������ǿ������������,Ũ�����ڷ�Ӧ��������ϡ,��ɲ������...