
|
学习小专题 |

|
学习小专题 |
 [注解与辨疑i] 有固体参与的等效平衡问题讨论 作者:董啸 来源:未知 日期:2012-07-22 15:43:29 点击:11223 所属专题:等效平衡
[注解与辨疑i] 有固体参与的等效平衡问题讨论 作者:董啸 来源:未知 日期:2012-07-22 15:43:29 点击:11223 所属专题:等效平衡
最近高三学生在练习过程中遇到下列一题: 在一个 1L 的密闭容器中,加入2molA和1molB,发生下列可逆反应: 2A (g)+B(g)→ 3C (g)+D(s)达到平衡时,C的浓度为1.2mol/L,维持容器的体积和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度还是1.2mol/L的是( ) A.1molA+...
 [注解与辨疑i] 自发反应和非自发反应 作者:江已舒 来源:未知 日期:2013-04-16 10:54:09 点击:23369 所属专题:自发反应
[注解与辨疑i] 自发反应和非自发反应 作者:江已舒 来源:未知 日期:2013-04-16 10:54:09 点击:23369 所属专题:自发反应
人们在研究化学反应时发现,有的反应如钢铁在空气中生锈,氧化钙跟水生成消石灰等在常温时就能自发地进行。有的反应,如氢气在氧气中燃烧,碳燃烧,铁粉跟硫粉的反应等虽然需要点燃或加热,但反应一旦发生,就能自发地进行下去。化学上把这一类反应称为自发反应。 另有...
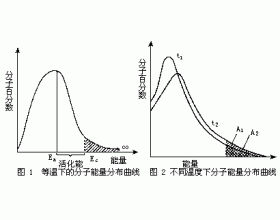 [注解与辨疑i] 化学反应的活化能 作者:张楠 来源:未知 日期:2016-02-01 12:13:27 点击:12485 所属专题:活化能 活化分子 有效碰撞
[注解与辨疑i] 化学反应的活化能 作者:张楠 来源:未知 日期:2016-02-01 12:13:27 点击:12485 所属专题:活化能 活化分子 有效碰撞
实验证明,只有发生碰撞的分子的能量等于或超过某一定的能量Ec(可称为临界能)时,才可能发生有效碰撞。具有能量大于或等于Ec的分子称为活化分子。 在一定温度下,将具有一定能量的分子百分数对分子能量作图,如图1所示。从图1可以看出,原则上来说,反应物分子的能量可...
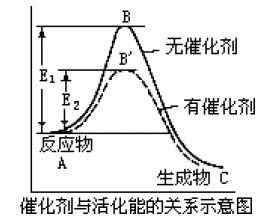 [注解与辨疑i] 催化剂对化学反应速率影响的原因是什么? 作者:郝军 来源:未知 日期:2020-03-09 12:53:11 点击:22293 所属专题:催化剂 影响反应速率因素
[注解与辨疑i] 催化剂对化学反应速率影响的原因是什么? 作者:郝军 来源:未知 日期:2020-03-09 12:53:11 点击:22293 所属专题:催化剂 影响反应速率因素
催化剂加快反应速率的原因与温度对反应速率的影响是根本不同的。催化剂可以改变反应的路线,降低反应的活化能,使反应物分子中活化分子的百分数增大,反应速率加快。(如图) 催化作用可分为均相催化和非均相催化两种。如果催化剂和反应物同处于气态或液态,即为均相催化...
 [注解与辨疑i] 怎样用活化分子和活化能的概念理解浓度、温度等外界条件对反应速 作者:李从山 来源:未知 日期:2017-04-25 16:41:02 点击:13132 所属专题:活化能 活化分子 化学反应速率 有效碰撞
[注解与辨疑i] 怎样用活化分子和活化能的概念理解浓度、温度等外界条件对反应速 作者:李从山 来源:未知 日期:2017-04-25 16:41:02 点击:13132 所属专题:活化能 活化分子 化学反应速率 有效碰撞
化学反应产生的先决条件,是反应物分子之间必须相互接触,然后才能互相作用,否则就不可能引起反应。不过反应物分子之间,并不是每一次碰撞都能产生反应的。以气体间的反应来说,我们知道,气体分子是以极大的速率向各个方向运动着,分子之间不断地相互碰撞,倘若每一次...
 [注解与辨疑i] 怎样分析浓度压强对化学平衡移动的影响? 作者:吴键 来源:未知 日期:2015-12-11 21:55:46 点击:5593 所属专题:浓度 压强 平衡移动
[注解与辨疑i] 怎样分析浓度压强对化学平衡移动的影响? 作者:吴键 来源:未知 日期:2015-12-11 21:55:46 点击:5593 所属专题:浓度 压强 平衡移动
1.在容积一定的密闭容器中,气体反应已达平衡,此时只要改变反应中的任何一种气体的浓度,平衡就会发生移动。移动方向应从浓度对平衡的影响考虑,而不应从压强考虑。 2.在容积一定的密闭容器中,气体反应已达平衡,若 同等程度地改变反应中各气体的浓度 ,可视为压强...
 [注解与辨疑i] 怎样理解压强对化学平衡的影响? 作者:陈恒 来源:未知 日期:2015-12-11 21:55:05 点击:13894 所属专题:压强 平衡移动
[注解与辨疑i] 怎样理解压强对化学平衡的影响? 作者:陈恒 来源:未知 日期:2015-12-11 21:55:05 点击:13894 所属专题:压强 平衡移动
对于有气体参加且反应前后气体体积发生改变的可逆反应,若在其它条件不变时,增大压强会使平衡向气体体积缩小的方向移动。 对于气体体积在反应前后不改变的反应(如H 2 +I 2 (气) 2HI),改变压强时,只影响反应速率,但对平衡无影响。 在理解压强对化学平衡的影响时,要...
 [注解与辨疑i] 增大某一反应物的浓度时生成物在混合物中的百分含量不一定增大 作者:程新 来源:未知 日期:2012-05-15 15:47:08 点击:9625 所属专题:平衡移动 浓度 百分含量
[注解与辨疑i] 增大某一反应物的浓度时生成物在混合物中的百分含量不一定增大 作者:程新 来源:未知 日期:2012-05-15 15:47:08 点击:9625 所属专题:平衡移动 浓度 百分含量
在平衡体系中增大某一反应物的浓度会使平衡向正反应方向移动。但生成物在平衡混合物中的百分含量并不一定增大。因为增大反应物的浓度,必须会使平衡时反应混合物的总物质的量增加。因此生成物在平衡混合物中的百分含量是否增大通过计算作出回答。 例:对于反应CO+H 2 O(气)...
 [注解与辨疑i] 合成氨工业条件的选择 作者:陈爱玉 来源:未知 日期:2012-05-15 15:43:06 点击:4984 所属专题:合成氨
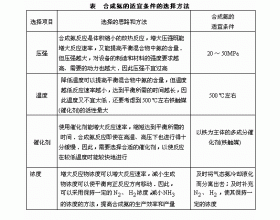
[注解与辨疑i] 合成氨工业条件的选择 作者:陈爱玉 来源:未知 日期:2012-05-15 15:43:06 点击:4984 所属专题:合成氨
工业上合成氨,既要使反应进行得快,又要使平衡混合物中氨的含量高,还要考虑生产中的动力、材料、设备等因素,以取得最佳效益.因此,必须根据化学反应速率和化学平衡原理的有关知识,对合成氨的条件进行选择.表为合成氨的适宜条件及其选择思路和方法....
 [注解与辨疑i] 走出勒沙特列原理的误区 作者:傅芳 来源:未知 日期:2016-05-12 10:34:50 点击:16269 所属专题:勒沙特列原理盲区
[注解与辨疑i] 走出勒沙特列原理的误区 作者:傅芳 来源:未知 日期:2016-05-12 10:34:50 点击:16269 所属专题:勒沙特列原理盲区
浓度、压强、温度对化学平衡的影响可以概括为平衡移动原理,又称之为勒夏特列原理:如果改变影响平衡的一个条件(如浓度、压强、温度等)平衡就向减弱这种改变的方向移动。该原理是判断平衡移动方向的重要依据,适用于所有的动态平衡,如:化学平衡、电离平衡、溶解平衡...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
在讨论惰性气体对化学反应平衡的影响之前,首先需要明确:这...
一、外界条件对反应速率的影响:别只看压强! 很多同学在判断...
在化学反应中,驱动力指的是推动反应进行的内在因素,它决定...
一.核心概念辨析 中间体:寿命长于分子振动的瞬态物种,多步...
活化分子百分数和活化分子数,理解它对掌握化学反应速率至关...
化学反应的焓变越大,代表这个反应受温度变化的影响越大吗?...
在化学热力学和分析化学中,我们常常听到这样的说法:“如果...
...