
|
学习小专题 |
 活化分子百分数和活化分子数
日期:2026-01-30 19:38:11
点击:612
好评:0
活化分子百分数和活化分子数
日期:2026-01-30 19:38:11
点击:612
好评:0
活化分子百分数和活化分子数,理解它对掌握化学反应速率至关重要。 简单来说: ·活化分子百分数:指的是在所有分子中,具有足够能量(即能量高于活化能)、能够发生有效碰撞的分子所...
 怎样用活化分子和活化能的概念理解浓度、温度等外界条件对反应速
日期:2017-04-25 16:41:02
点击:13101
好评:0
怎样用活化分子和活化能的概念理解浓度、温度等外界条件对反应速
日期:2017-04-25 16:41:02
点击:13101
好评:0
化学反应产生的先决条件,是反应物分子之间必须相互接触,然后才能互相作用,否则就不可能引起反应。不过反应物分子之间,并不是每一次碰撞都能产生反应的。以气体间的反应来说,我们知道,气体分子是以极大的速率向各个方向运动着,分子之间不断地相互碰撞,倘若每一次...
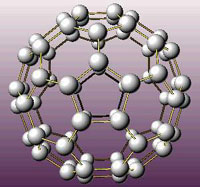 动画演示:活化分子
日期:2016-04-19 13:47:50
点击:495
好评:0
动画演示:活化分子
日期:2016-04-19 13:47:50
点击:495
好评:0
...
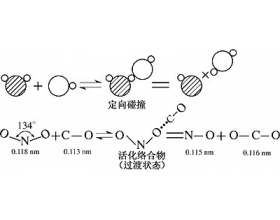 为什么活化分子的碰撞不一定都发生有效碰撞
日期:2016-03-17 14:39:49
点击:11319
好评:0
为什么活化分子的碰撞不一定都发生有效碰撞
日期:2016-03-17 14:39:49
点击:11319
好评:0
反应物分子之间发生有效碰撞,必须同时满足两个条件,一是反应物分子的能量必须达到某一临界数值,二是反应物分子必须按一定的方向互相碰撞。前者是能量因素,后者是空间因素。现以反应NO 2 +CO=NO+CO 2 为例来说明。 当NO 2 和CO分子彼此靠近时,它们分子中的价电子云...
 化学反应的活化能
日期:2016-02-01 12:13:27
点击:12467
好评:-2
化学反应的活化能
日期:2016-02-01 12:13:27
点击:12467
好评:-2
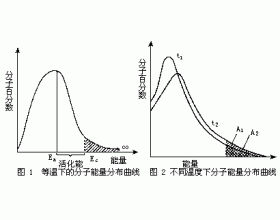
实验证明,只有发生碰撞的分子的能量等于或超过某一定的能量Ec(可称为临界能)时,才可能发生有效碰撞。具有能量大于或等于Ec的分子称为活化分子。 在一定温度下,将具有一定能量的分子百分数对分子能量作图,如图1所示。从图1可以看出,原则上来说,反应物分子的能量可...
 动画演示:活化分子
日期:2012-11-27 18:28:08
点击:466
好评:0
动画演示:活化分子
日期:2012-11-27 18:28:08
点击:466
好评:0
...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。