
|
学习小专题 |

|
学习小专题 |
 [注解与辨疑i] 小议化学平衡中的转化率 作者:李文才 来源:未知 日期:2016-01-08 10:29:06 点击:11785 所属专题:转化率
[注解与辨疑i] 小议化学平衡中的转化率 作者:李文才 来源:未知 日期:2016-01-08 10:29:06 点击:11785 所属专题:转化率
转化率定义式: 转化率 一 . 压强对转化率的影响 例 1. 一定温度下,在一密闭容器中充入 和 ,一定条件下发生如下反应 ,达到平衡后,此时 的转化率为a%。缩小容器的容积,再次达到平衡时 的转化率将( ) A. 增大 B. 减小 C. 不变 D. 无法确定 分析: 反应达到平衡后,...
 [注解与辨疑i] 浅析“自发反应” 作者:张世敏 来源:未知 日期:2016-02-04 12:50:28 点击:15808 所属专题:自发反应
[注解与辨疑i] 浅析“自发反应” 作者:张世敏 来源:未知 日期:2016-02-04 12:50:28 点击:15808 所属专题:自发反应
和同行们讨论自发反应,讲到教材中对自发反应概念的描述,一定条件下,不需要外界的帮助就能自动发生的化学反应,称为自发的化学反应(苏教版《化学反应原理》)。经常要讨论:一定条件含义是什么?怎么理解外界的帮助? 查了一些资料,比较通俗、浅显的说,这两个问题...
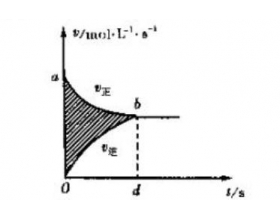 [注解与辨疑i] 化学平衡图像里阴影部分含义 作者:林飞 来源:未知 日期:2023-11-14 17:03:46 点击:12273 所属专题:化学平衡图像
[注解与辨疑i] 化学平衡图像里阴影部分含义 作者:林飞 来源:未知 日期:2023-11-14 17:03:46 点击:12273 所属专题:化学平衡图像
题型:在容积固定的4L容器中,进行可逆反应:X(g) + 2Y(g) == 2Z(g),并达到平衡。在此过程中,以Y浓度的改变表示反应速率V正、V逆与时间t的关系如下图,则阴影部分面积表示: A.X浓度的减少 B.Y的物质的量的减少 C.Z浓度的增加...
 [注解与辨疑i] 把握实质 判断压强对化学平衡的影响 作者:赵宝 来源:未知 日期:2016-05-16 12:51:20 点击:18398 所属专题:压强 平衡移动
[注解与辨疑i] 把握实质 判断压强对化学平衡的影响 作者:赵宝 来源:未知 日期:2016-05-16 12:51:20 点击:18398 所属专题:压强 平衡移动
对于有气体参加的可逆反应,其他条件不变时,增大压强,会使化学平衡向气体体积缩小的方向移动;减小压强会使化学平衡向气体体积增大的方向移动;若反应前后气体体积无变化,改变压强,化学平衡不移动。这是压强对化学平衡影响的规律。然而学生在运规律判断压强对化学平衡...
 [注解与辨疑i] 化学反应速率与化学平衡的是非判断 作者:古盛兰 来源:未知 日期:2020-12-18 15:52:32 点击:11013 所属专题:速率与平衡 是非判断
[注解与辨疑i] 化学反应速率与化学平衡的是非判断 作者:古盛兰 来源:未知 日期:2020-12-18 15:52:32 点击:11013 所属专题:速率与平衡 是非判断
1.一定条件下,增加反应物的量,必定加快反应速率。 2.升高温度会使放热反应速率减慢,吸热反应速率加快。 3.增大压强,对有气体参加的反应都会加快反应速率。 4.使用催化剂一定会加快反应速率。 5.可逆反应的特征是正反应速率总是和逆反应速率相等。 6....
 [注解与辨疑i] 平衡移动与反应物的转化率间的关系 作者:张安荣 来源: 日期:2016-01-08 11:04:16 点击:25046 所属专题:转化率
[注解与辨疑i] 平衡移动与反应物的转化率间的关系 作者:张安荣 来源: 日期:2016-01-08 11:04:16 点击:25046 所属专题:转化率
化学平衡是暂时的,一旦外界条件改变,原有的固定的各种数量关系皆会因平衡的移动而发生改变,平衡移动时反应物的转化率如何变化,这要根据具体反应及引起平衡移动等具体原因而定,不可一概而论。下面对造成平衡移动时反应物的转化率的变化规律分析归纳如下。 一、 由...
 [注解与辨疑i] 用碰撞理论解释影响化学反应速率的因素 作者:马文礼 来源: 日期:2007-12-31 03:26:11 点击:15484 所属专题:有效碰撞 影响反应速率因素
[注解与辨疑i] 用碰撞理论解释影响化学反应速率的因素 作者:马文礼 来源: 日期:2007-12-31 03:26:11 点击:15484 所属专题:有效碰撞 影响反应速率因素
化学反应速率内容理论性强,学生不易理解。特别是在学习影响化学反应速率的因素时,课本是用碰撞理论来解释的,学生初学时更是难懂,下面我结合自己的教学实际,谈几点体会,以帮助学生理解。 一、碰撞理论的要点 (1)反应得以进行的先决条件是反应物分子间必须发生碰...
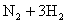 [注解与辨疑i] 选择反应适宜的条件 作者:张瀚 来源: 日期:2016-02-01 13:02:53 点击:8664 所属专题:合成氨
[注解与辨疑i] 选择反应适宜的条件 作者:张瀚 来源: 日期:2016-02-01 13:02:53 点击:8664 所属专题:合成氨
工业生产中既要考虑尽量增大反应物转化率,充分利用原料又要选择较快的反应速率,提高单位时间产率。以上两点就是选择反应条件的出发点,当二者发生矛盾时,要结合具体情况辩证分析,找出最佳反应条件。 以合成氨反应为例: ( 1)增压:合成氨的反应是有气体参加的反...
 [注解与辨疑i] 同温同体积时反应物的量的改变对常见物理量的影响 作者:耿艳 来源: 日期:2016-02-01 13:04:37 点击:13668 所属专题:浓度 转化率 体积分数 百分含量
[注解与辨疑i] 同温同体积时反应物的量的改变对常见物理量的影响 作者:耿艳 来源: 日期:2016-02-01 13:04:37 点击:13668 所属专题:浓度 转化率 体积分数 百分含量
重要提示:在解决反应物的量的改变对常见物理量的影响的问题时,应时刻注意以下2个方面:反应的条件是同温同体积还是同温同压;反应的方程式是气体之间的反应还是有固体参加或生成的反应。 一、反应物只有一种的情况(气体之间的反应) 例如:aA(g) bB(g) + cC(g) ,若...
 [注解与辨疑i] 等效平衡问题的投料方法归纳 作者:耿艳 来源: 日期:2015-12-11 23:11:47 点击:17619 所属专题:等效平衡
[注解与辨疑i] 等效平衡问题的投料方法归纳 作者:耿艳 来源: 日期:2015-12-11 23:11:47 点击:17619 所属专题:等效平衡
重要提示:在解决等效平衡问题时,应时刻注意以下2个方面:反应的条件是同温同体积还是同温同压;反应的方程式是气体之间的反应还是有固体参加或生成的反应。 一、等效平衡问题的投料方法: 1、没有固体参加的化学反应: ①题意要求:同温同体积下达到平衡时,对应物质...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。核心思想: 多、快、好、省, 四大关键条件的分析与调控 1. 温度 (Temperature) ・ 热...
在化学反应动力学与热力学研究中,多平衡系统是一类普遍存在的复杂反应体系。明确其定...
催化反应在现代工业中无处不在,从化工合成到环境治理,都离不开催化剂的参与。而催化...
一、范特霍夫方程:化学反应的“平衡指挥家” 在可逆反应里,化学平衡常数(K)能衡量...
什么是能垒、活化能?二者有什么区别? 1、能垒 活化分子含有的能参加化学反应的最低...
1.无论是用某一反应物表示还是用某一生成物表示,由于Δ C 是取浓度变化的绝对值,因...
在一个恒温恒容的密闭容器里,充入2mol SO 2 和1mol O 2 ,发生如下反应并建立化学平...
...