
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
早在1879年,SmithsonTennant已经发现,金刚石燃烧的产物是碳的氧化物,故金刚石是碳的单质。1913年,Bragg父子用X-衍射实验测定了金刚石的晶体结构。证实通常的天然金刚石属于立方晶系,其晶胞为面心立方,一个晶胞里有8个碳原子(一个点阵点为两个碳原子)。每个碳原子周围有四十呈四面体排列的碳原子,健长为154pm。然而应当指出,在殒石里发现的金刚石却是六方晶系的。两种晶体的差别不在于碳原子的杂化类型(sp3),而在于排列方式不同引起晶体的对称性不同。
金刚石被人类当作宝石而珍藏,据说已有3000年的历史。经过琢磨的金刚石称为钻石,它密度大(3.51g·cm-3),是已知物质中最坚硬的(莫氏硬度10);它对光的透明度好,折射率高,琢磨适当的钻石能反射出更多的光而显得格外耀眼;高色散性还使钻石有‘光彩’,这是白光被钻石色散成单色光所致。金刚石的色散值是天然宝石里最高的。利用色散值的差别可以把金刚石跟很像它的锆石(ZrSiO4)区分开来。天然金刚石有的无色,有的则呈美而的蓝、黄、棕、绿等色,还有的呈黑色。理论研究证实,纯净的金刚石应当是无色的。它可以透过各种不同波长的光(包括红外和紫外)。这是因为把金刚石晶体里的电子从基态激发到最低能量的激发态需要5.4电子伏特的能量,远大于可见光的能量(1.7—3.10电子伏特)。当金刚石里掺杂氮,能量从原来的5.4降到2.2左右,随氮原子的含量的增高,由于热运动引起的氮能级的宽度的差别,吸收不同波长的可见光,呈现黄(C/N=105:1)、绿(C/N=103:1)色,氮原子继续增多,所有可见光都会被吸收掉,便得到黑色的金刚石。在好长一个时期里,人们认为蓝色的金刚石是由于其中掺杂铝引起的。后来经美国通用电气公司的实验室证实,金刚石的蓝色是由其中不到百万分之一的硼引起的。他们发现,蓝色的金刚石是有导电性的。这可以解释为:硼原子的存在可以使碳的价带电子进入硼(受主)能级而在价帝里留下空穴,引起空穴导电。而铝的掺杂不可能有这种性质。金刚石的颜色还可因掺杂原子引起所谓的“色心”(又称F心)而引起。这类金刚石的颜色会因加热、辐照而改交,有的还有荧光。习惯上钻石的质量按克拉(1克拉等于200毫克)计算。一颗钻石,超过10克拉,就已很稀罕很珍贵了。至今最大的一颗金刚石是1906年开采出来的‘非洲之星’,3025克拉。世界上最大的一颗钻石则是称为‘蒙兀儿大帝’的,加工前重780克拉。
人们梦想合成金刚石已经有很长的历史了。这种梦想的推动力一开始就是为了人工造出珍贵的钻石。因为天然的金刚石太少了。地球化学研究证实,自然界里的碳只有当熔化的岩石在3万个大气压的高压下,才能以金刚石的方式结晶出来,有时生成金刚石的压力竟高到60000个大气压。这样大的压力只有在地面下60—100公里的深处才存在,从这样深的地方翻到地秃表层来的岩石太少了。开采金刚石需要很大的投资。那种从地表找到一颗金刚石的机会是极其稀少的。而开采出来的天然金刚12石,只有很少就其质量而言可以加工成钻石,多数是灰色或黑色的。并不透明,有的内部夹杂有石墨,无法琢磨出钻石。最早尝试人工合成金刚石的报导在1880年。而第一个宣称合成金刚石的是著名的法国实验化学家莫瓦桑(H·Moissan)。他以当时已有的化学知识预计,尚未制得的单质氟的化学性质极其活泼,若用它来及其迅猛地夺取碳氢化台物里的氢,就有可能把余留下的碳转变成金刚石。结果,他费了数年的光阴,克服了重重困难,真的制出了活泼的氟,取得了同的代人不可多得的巨大成就(他因此以及由此开拓的氟化学而得到诺贝尔奖金)。然而,当他实施氟和烃类的反应时,既使是在超低温下,也以猛烈的爆炸告终,一无所得。惨重的失败并未动摇过莫瓦桑人工制造金刚石的信念。后来,他从地球化学家那里得知了自然界石墨转化成金刚石的高温高压的条件,便设计了一种模拟天然过程的用石墨造金刚石的实验。他把石墨溶进熔融的铁,然后令铁急速地冷却。企图通过液态的铁转化成固态的铁时产生的巨大内压,把石墨转化成金刚石。这种想法,粗想起来是蛮有道理的。因而莫瓦桑叫他的学生们,一次又一次地把这种实验得到的产品用无机酸把铁溶解掉,从黑乎乎的固态残渣里寻找金刚石。后来,‘真的’从中发现了透明的“金刚石”。其中一颗被命名为法国卢浮宫里的著名钻石——摄政王同名的金刚石至今仍然在莫瓦桑的实验室里展览。莫瓦桑曾经两度在报上发表他已成功地制得金刚石。鉴于莫瓦桑的崇高威信,一时间引起了全球的轰动,穷人为之欢呼雀跃,富人为之垂头丧气。后来虽有著名氟化学家O·Ruff在1915年以及Parsons在1920年宣称重复了莫瓦桑的实验制得了金刚石,却始终不能拿出足以令人信服的证据。到本世纪50年代,有人从理论上论证了金刚石在高温高压下生成的临界条件,根本地否定了莫瓦桑设计的实验取得成功的可能性。据说,莫瓦桑的人造金刚石是他的学生被逼得无奈,投进酸洗后的黑色残渣里的天然金刚石。也有人报导,莫瓦桑得到的只是碳化硅或尖晶石(MgAl2O4)。
首先在理论上计算合成金刚石的热力学条件的是R·Berman。简单地说,他的计算就是建立石墨转化为金刚石相图。计算的结果是:如果以温度为横坐标,压力为纵坐标,可以在图上划出一条由左下方向右上方延伸的近似的直线,在直线的下方是石墨的稳定区(对金刚石则是热力学的介稳区),在直线的上方则是金刚石的稳定区(对石墨则力介稳区)。若温度和压力正好处于直线上则是金刚石和石墨的平衡转化点。这张图表明,例如在1200—1500K的温度范围内,要使石墨转化为金刚石的压力需要达到4.3×109-5.2×109Pa(4—5万大气压)。
值得指出的是,在教学讨论中,我们常常发现有人误解高温对合成金刚石的作用。应当注意,根据上述的石墨转化为金刚石的相图,如前所述,相平衡线的斜率是正值。这就是说,反应温度越高,需要的压力也就越高。若单考虑温度,结论应当是:(就热力学而言)温度越高,石墨越不容易转化为金刚石。这也可以从只考虑温度不考虑压力的Gibbs—Helmholtz方程(△G=△H-T△S)看出。标态下石黑转化为金刚石是吸热反应(△H>0),熵变△S<0(∴-T△S>0),因此温度越高,石墨转化为金刚石的自由能越大,即自发趋势越小。加压有利于转化是不难理解的。这是由于石墨的密度比金刚石的小,转化是体积减小的过程。因此,转化反应所需的高温只是为了提高速度。事实上,在高温高压下合成金刚石也是需要催化剂的。无催化剂时,石墨直接转化为金刚石的实验条件是2700℃,13GPa;利用Ni—Co—Fe合金加入少量的硫、钛、铝等,可使转化温度降到950℃,压力降到4GPa。
金属为什么能够催化石墨转化为金刚石的反应?这是一个引人入胜的问题。在已经提出的理论中有两种十分形象。一种是金属的表面作用的理论:金属镍属于面心立方晶体。镍原子的二维密置层的法线方向是立方晶胞的对角13线方向,在晶体学上称为(111)方向,而每个镍原子周围有6个镍原子的二维密置层则称为(111)面。面上的镍原子形成的正三角形的边长为249pm,跟石墨的二维面上的碳原子形成的三角形的边长(246pm)十分接近。当金属镍的表面正好是(111)面而又正好对着石墨的二维平面肘,镍原子便和碳原子之间一对一地形成化学键(石墨的碳原子的与二维平面垂直的2pz轨道里的单电子进入镍原子的只有单电子的3d轨道),结果把石墨的二维平面上的半数碳原子拉向镍的表面,在高压下,石墨的层间距从335pm被压缩,从而使碳原子的杂化类型由sp2转化为sp3(见图1)。铁、钴、镍及其合金的晶体结构相似,因此都是石墨转化为金刚石的催化剂。另一种理论认为石墨中的碳原子可以单个地进入金属原子之间的四面体空隙,并在金属原子的作用下使其原子轨道杂化成sp3,碳原子通过扩散遇到另一碳原子形成金刚石。
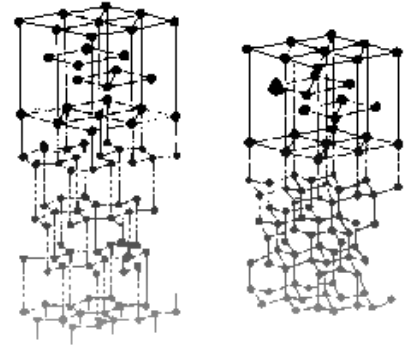
图1石墨在金属表面原子的作用下转化为金刚石
50年代初,在美国和瑞典成立了两个人造金刚石的研究小组,分别在1954和1953年合成了金刚石。我国从1961年开始也友展了合成金刚石的技术。起先合成的金刚石太小,不足以用来制作钻石。1969年,日本就宣布了获得宝石级的金刚石单晶。近三十年来,采用了放置晶种和抑制晶核生成速度而加快晶粒长大的技术,用高温高压法制取的金刚石越来越大。到80年代末,第一次制得一颗11克拉重的人造金刚石。据说,在90年代,人们有可能用高温高压法大量地制取连宝石专家也难以跟天然金刚石区分开的高质量的可以用来制作宝石的人造金刚石,将使昂贵的钻石的身价真的大大下跌,使钻石珠宝真的普及。目前,制造宝石级大小和质量的高温高压法合成金刚石的工艺方法在基本模式上仍可以发现莫瓦桑的设计的影子。但是碳(石墨)是在高达50000—65000大气压的高压和1500℃的高温下被压入液态金属的。在这里,液态金属对金刚石的形成有催化作用。用这种技术合成的金刚石制作的钻石已经进入市场。只有用元素分析的技术才可把它们跟天然金刚石区分开,既从人造的金刚石里可以检出极微量的溶解于其中的镍(它是石墨转化为金刚石的催化剂),而天然金刚石里是不含镍的。值得提到的是,如前所述,人们已经获知美丽的黄、绿、蓝色金刚石的颜色的来源。合成金刚石时,如果在技术上有效地控制迸入金刚石的杂质,便可以获得自然界里很少见的珍贵的带色的(特别是蓝色的)金刚石,真正达到巧夺天工的境地。
金刚石的用途并不只是用来琢磨成宝石。早在罗马时代,就有人把金刚石雕刻成印章,这是最早的金刚石的‘工业用途’。事实上,人们从自然界里开采出来的绝大多数金刚石是用于工业的。长期以来,金刚石的工业用途大多是利用它特别硬,不易磨损的特性。金刚石用来切割玻璃的常识可以启发我们理解为什么大量的金刚石用来制作钻头,用于地质钻探和开采石油,打井等,也使我们容易理解金刚石可以用于切割水泥,甚至大理石等高档的建筑材料。至今,只有用金刚石车刀才能加工超硬的陶瓷,尚无其他代用品。金刚石还是优质的磨料。金刚石砂轮用来磨削硬质合金,比碳化硅耐用一万倍。用金刚石磨料代替碳化硅磨料加工光学玻璃,生产效率可以提高数倍至数十倍。在大块的黑色金刚石里钻一个小孔(例如可以采用激光技术做到这一点),可以用来抽拉直径稳定的金属丝,如制造用于制作灯泡的钨丝或者拉人造丝等合成纤维等。这种金刚石拉丝模比用硬质合金的拉丝模的使用寿命长250倍。此外,金刚石还广泛地用于制作硬度计压头、表面光洁度测量仪的测头、高压腔的压头、电唱机的唱针头等。如令,这些工业用途的金刚石已经主要靠高温高压技术合成的人造金刚石。进入世界市场的息价值已经超过10亿美元。应当指出,合成工业用金刚石跟合成宝石级金刚石属于两种不同的技术。它的产品不是单晶而是聚晶或多晶,直径小到几微米的都有用,而且大多并不要求无色透明,更不追求美丽的色彩。除用上述镍合金催化的技术外,还提到的是“爆炸法”。例如,用TNT或黑索金等炸药引爆产生的强冲击波作用于石墨,在几微秒的瞬间内可得到几十万大气压的高压,使石墨转为金刚石。一次爆炸可生产500克拉,一公斤炸药可得60克拉金刚石。但用此法生产的金刚石平均粒度的10微米,最大不过40微米,杂质含量高达20%,适宜于制造研磨膏或做聚晶金刚石的原料。
近年来,金刚石的工业用途的利用其高硬度的唯一形象已经开始改观。材料科学家们发现,金刚石除了硬度最大的特性外,还有许多令人注目的大大优于我们已经熟识的材料的特性。例如,人们发现,金刚石作为半导体,性能远超过目前在此处独居鳌头的硅。这是由于金刚石不仅有优良的半导性,而且,几乎任何气体杂质都难以送入金刚石的结构里去,这使得金刚石的半导性特别稳定。金刚石在室温下的导热性最大,这使得用金刚石制成的大功率半导体元件不像硅半导体那样由于导热问题解决不了而不能加大其荷载的电流。据报导,纯净的单晶金刚石在室温下的导热率为第摄氏度每厘米约21瓦,比铜高5倍。金刚石可以透过从红外到X-射线的所有波长的辐射(光),因而可作为广谱的光学透镜或传递信息的光导材料。所有这些应用据认为最好把金刚石做成薄膜,可简称钻石薄膜。
用高温高压法就能够制作钻石薄膜。但是,这样制得的钻石薄膜并不理想:高压室的容积较小,不可能用来生产大面积的薄膜;得到的钻石薄膜的金刚石的结构里不可避免地存在用来当反应催化剂的金属杂质,这样产生的晶体的缺陷减低了金刚石的导热性,使它仅比铜好一点点,而且限制了薄膜的光洁度;而且不可避免地在薄膜里有向各个方向生长的大量的金刚石微晶,这种取向不同的微晶有利于把金刚石用作工具镀层却不利于做半导体材料。
早在50年代,就有人研究用低压法合成金刚石的方法了。在60年代,苏联的鲍里斯·德亚金和克利夫兰的西保留地的约翰·安格斯分别宣布可用高温下的烃类的蒸气为原料制得金刚石。到70年代,他们又宣布克服了得到的产品含石墨的难题,但未透露任何细节。到80年代初,日本科学技术厅无机材料研究所的研究人员宣称,他们在常压下合成了具有商业价值的纯净的钻石薄膜。他们的方法是,在一个真空系统中充入氢气和甲烷或者其他烃类,例如乙炔的混合气体,用微波或灯丝把混合气体加热到2200℃,氢气和烃类分子分解,碳原子便沉积在加热室内的硅片或其他材料的薄片上,形成钻石薄膜。这是一种称为化学气相沉积法(CVD)的化学合成新方法。最近5年来,日本和美国开发了几种钻石薄膜CVD合成法。所有方法中,氢气是必需的,而且占混合气体组分的99%;氢气的存在可以保证烃分解产生的碳以金刚石的三维网状结构的方式沉积在基质材料上,而不是石墨。但氢气的作用机制至今仍是一个未解开的谜。CVD钻石薄膜的导热性明显优于高压钻石薄膜,其导热率是高压钻石薄膜的2倍,达8—12瓦/度·厘米,适用于做灵敏电子元件的吸热层。
钻石薄膜的应用前景是十分诱人的。例如,日本的建伍公司,称钻石薄膜可使高保真音响的性能大大改善。用CVD法在钛基或碳化硅基上形成2微米厚的钻石薄膜。制作的扩音器可将声音以任何传统扩音器频率的两倍予以重播。高保真专家认为,可听频率的这种优质重播是得益于过高的听不见的频率的精确重现。美国人认为钻石薄膜的高导热性可使它成为在一小块区域内产生大量热的激光二极管的纤维光学系统。它的耐热性对汽车的发动机的传感器和电子武器将很有价值。它的耐辐射性使它成为空间应用的理想材料,例如用于通信卫星。钻石薄膜作为半导体的信号传递速度要比硅快两倍。钻石薄膜还有开发成超导材料的可能。
钻石薄膜的CVD法的前途在很大的程度上将取决于减低成本。目前,高压钻石每生产1克拉已经降到只需1美元,而用CVD法生产的钻石薄膜每克拉需100美元。高压钻石已经发展了35年以上,时间是否可使CVD钻石薄膜的成本下降?安格斯认为,CVD法中,氢必须分解成氢原子才能起作用,分解氢的成本就已述1—100美元之间。前景究竟如何?尚不得而知

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
石膏在水泥中一般起延缓水泥硬化速率的作用,但在特殊情况下...
早在 1879 年, SmithsonTennant 已经发现,金刚石燃烧的产物是碳的...
什么是钢化玻璃? 钢化玻璃其实是一种预应力玻璃,为提高玻璃...
自然界里碳有3种同位素12C、13C和14C。其中14C是放射性的,半衰期...
( 1)普通玻璃(Na 2 SiO 3 、CaSiO 3 、SiO 2 或Na 2 OCaO6SiO 2 ) ( ...
铅单质 一: 物理性质 铅为暗灰色,重而软的金属,熔点600.7K,沸...