
|
学习小专题 |
 117号元素是金属元素还是非金属元素?
日期:2022-08-13 07:47:45
点击:5179
好评:0
117号元素是金属元素还是非金属元素?
日期:2022-08-13 07:47:45
点击:5179
好评:0
关于117号元素是金属元素还是非金属元素的讨论以下几种意见: 1、非金属元素 虽然根据金属与非金属分界线的延伸法则, 117号元素理应为金属元素。但因为117号元素处于卤族(卤族元素更可能为非金属),且根据现有理论等测算得到的结果,2017年公布的最新版元素周期表上117号...
 比较氧元素和氯元素的非金属性
日期:2018-08-14 16:41:52
点击:18694
好评:0
比较氧元素和氯元素的非金属性
日期:2018-08-14 16:41:52
点击:18694
好评:0
氧元素和氯元素是非金属性仅次于氟元素的两元素,它们的非金属性的强弱一直是中学化学教学中难以讲清的问题。高中课本在介绍元素周期律和元素化合物性质时指出:在同一周期中,各元素的原子从左到右失电子能力逐渐减弱,得电子能力逐渐增强。因此金属性逐渐减弱,非金...
 关于“非金属性”和“非金属活动性”的辨析
日期:2017-08-15 11:16:01
点击:1862
好评:0
关于“非金属性”和“非金属活动性”的辨析
日期:2017-08-15 11:16:01
点击:1862
好评:0
1、问题提出 2011年第3期《化学教学》中刊登了张英锋等老师 的一篇文章“对高中化学教学中几个常见问题的分析与 探讨”,文中提到比较非金属性强弱的规律: (1) 例如:2Cu+S == Cu 2 S,Cu+Cl 2 == CuCl 2 ,所以, Cl的非金属性强于S。 (2) 非常完美的结论:Fe+S = ...
 元素金属性和非金属性比较的几个误区
日期:2016-05-12 15:22:53
点击:2906
好评:0
元素金属性和非金属性比较的几个误区
日期:2016-05-12 15:22:53
点击:2906
好评:0
在中学化学教学中,元素的金属性与非金属 性的比较是一个重点,也是一个难点。不少教师 和学生很容易走人误区。笔者根据多年的教学实 践,将一些常见的误区归纳如下。 误区1:非金属单质A可置换出非金属单质B,A非金属性定大于B。 例1可用化学方程式2C+SiO 2 =Si +2CO...
 比较元素金属性和非金属性强弱的依据
日期:2016-01-24 18:32:25
点击:35570
好评:2
比较元素金属性和非金属性强弱的依据
日期:2016-01-24 18:32:25
点击:35570
好评:2
一、比较元素金属性强弱的依据 金属性——金属原子在气态时失去电子能力强弱(需要吸收能量)的性质 金属活动性——金属原子在水溶液中失去电子能力强弱的性质 注:“金属性”与“金属活动性”并非同一概念,两者有时表示为不一致,如Cu和Zn:金属性是:Cu Zn,而金属活...
 气态氢化物水溶液酸性强弱与元素非金属性强弱的关系
日期:2016-01-24 18:27:33
点击:19537
好评:0
气态氢化物水溶液酸性强弱与元素非金属性强弱的关系
日期:2016-01-24 18:27:33
点击:19537
好评:0
元素的最高价氧化物的水化物酸性强弱往往反映元素的非金属性的强弱。例如,P、S、Cl为同周期元素,它们的非金属性由弱至强的顺序是P<S<Cl,它们的最高价氧化物的水化物酸性由弱至强的顺序是H 3 PO 4 <H 2 SO 4 <HClO 4 。N、P、As为同主族元素,非金属性由强至弱的...
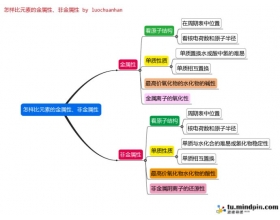 怎样比较金属性、非金属性的强弱之思维导图
日期:2016-01-22 18:53:51
点击:1936
好评:0
怎样比较金属性、非金属性的强弱之思维导图
日期:2016-01-22 18:53:51
点击:1936
好评:0
...
 元素金属性及非金属性的比较方法
日期:2013-11-13 17:18:36
点击:13798
好评:3
元素金属性及非金属性的比较方法
日期:2013-11-13 17:18:36
点击:13798
好评:3
一、元素金属性的比较方法 1 、用失去电子的难易比较:金属原子失去电子越容易,金属元素的金属性就越强;金属原子失去电子越不容易,金属元素的金属性就越弱。 例如:钠比镁更容易失去电子,钠金属性比镁强。 2 、用与水反应产生氢气的能力比较:金属越容易和水反应产生氢...
 非金属性、非金属单质的活动性与氧化性
日期:2012-11-06 16:04:49
点击:7047
好评:0
非金属性、非金属单质的活动性与氧化性
日期:2012-11-06 16:04:49
点击:7047
好评:0
(1)非金属性:指元素的原子得电子能力的大小,它主要与原子结构有关(通过电负性的大小确定)。 (2)非金属单质的活动性:指非金属单质在参加化学反应(一般为得电子过程)时,断裂为单个原子并参与反应的难易程度,它与其分子内化学键的类型及强弱有关.如N 2 分子非常稳定,...
 元素非金属性的强弱规律
日期:2012-09-14 16:11:45
点击:2829
好评:0
元素非金属性的强弱规律
日期:2012-09-14 16:11:45
点击:2829
好评:0
...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。