
|
学习小专题 |
 为什么酸性的硝酸盐具有强氧化性?
日期:2025-02-27 15:19:20
点击:1738
好评:0
为什么酸性的硝酸盐具有强氧化性?
日期:2025-02-27 15:19:20
点击:1738
好评:0
硝酸有氧化性而硝酸根离子却没有,主要是因为硝酸分子(HNO3)中的氮元素处于最高价态(+5价),这使得它具有强烈的氧化性。而硝酸根离子(NO3-)虽然也含有处于高价态的氮元素,但由于其标准电极电势不高,氧化性很弱,几乎可以忽略不计。 具体来说,硝酸的氧化性主要...
 关于硝酸及其盐性质问题讨论
日期:2021-08-22 12:31:23
点击:1451
好评:0
关于硝酸及其盐性质问题讨论
日期:2021-08-22 12:31:23
点击:1451
好评:0
一、硝酸的浓度与其氧化性的关系: 众所周知浓硝酸的氧化性强于稀硝酸,这一点可以用两种角度来分析解释。 1、化学平衡原理定性说明 写成离子方程式时,由于氢离子属于硝酸发生氧化还原反应的反应物,因此反应物浓度越高,反应的平衡常数就越大,当然性质也就越强。用大学知...
 鉴定硝酸根离子的方法之棕色环法
日期:2021-06-24 16:26:03
点击:962
好评:0
鉴定硝酸根离子的方法之棕色环法
日期:2021-06-24 16:26:03
点击:962
好评:0
...
 在新制的硝酸亚铁溶液中,滴入少量的浓盐酸,为什么观察到溶液变黄
日期:2020-11-16 08:59:39
点击:987
好评:0
在新制的硝酸亚铁溶液中,滴入少量的浓盐酸,为什么观察到溶液变黄
日期:2020-11-16 08:59:39
点击:987
好评:0
在硝酸亚铁溶液中加入浓盐酸发生两种变化: ①溶液中存在水解平衡:Fe 2+ +2H 2 O Fe(OH) 2 +2H + ,加入盐酸,使溶液中氢离子浓度增大,平衡左移,使溶液中亚铁离子的浓度增大,表现为浅绿色加深; ②溶液中同时有较多的氢离子和硝酸根离子,硝酸具有较强氧化性,即发...
 硝酸盐受热分解有哪些规律?
日期:2019-11-22 14:48:41
点击:8175
好评:0
硝酸盐受热分解有哪些规律?
日期:2019-11-22 14:48:41
点击:8175
好评:0
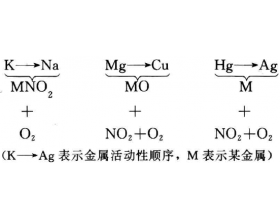
一般来说,活泼金属的硝酸盐,也就是金属活动性顺序表里钾、钙、钠的硝酸盐,受热时放出氧气并生成相应的亚硝酸盐;在 金属活动顺序表中位于镁和铜之间的金属硝酸盐受热时,生成金属氧化物、二氧化氮和氧气;而铜以后的金属硝酸盐受热时,生成金属单质、二氧化氮和氧气...
 硝酸盐的氧化性
日期:2016-01-21 16:16:35
点击:5790
好评:0
硝酸盐的氧化性
日期:2016-01-21 16:16:35
点击:5790
好评:0
硝酸盐多数为无色晶体,易溶于水。硝酸盐在中性或碱性溶液中,NO 3 - 离子通常很稳定,硝酸盐溶液不分解,无氧化性。但在强酸性溶液里,由于NO 3 - 与H + 相当于HNO3,所以表现出强氧化性。如Fe 2+ 、NO 3 - 两种离子在溶液中共存,若增加了H + ,则相互要发生氧化还原...
 硝酸盐的检验方法
日期:2016-01-21 15:10:41
点击:8570
好评:0
硝酸盐的检验方法
日期:2016-01-21 15:10:41
点击:8570
好评:0
一、实验原理 硝酸盐跟浓硫酸共热可产生硝酸,硝酸跟铜反应可放出二氧化氮(红棕色气体)。根据能否产生红棕色气体,即可判断是否有硝酸盐存在。 二、实验方法 取少量被检验的晶体(或溶液加热浓缩后),加入少量浓硫酸和铜片,并在酒精灯火焰上加热。观察红棕色气体的...
 硝酸盐的分解规律
日期:2016-01-21 12:11:42
点击:7604
好评:0
硝酸盐的分解规律
日期:2016-01-21 12:11:42
点击:7604
好评:0
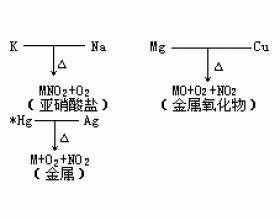
(1)硝酸盐在受热时易分解并放出氧气。 ①含氧酸不稳定,其对应的盐受热也易分解。 ②高温时硝酸盐是强氧化剂:分解时生成氧气。 (2)硝酸盐受热分解规律: ①金属活动顺序表中从K到Mg对应的盐受热分解生成亚硝酸盐和氧气。 Ca(NO 3 ) 2 = Ca(NO 2 ) 2 +O 2 ↑ ②金属活...
 硝酸盐的热分解规律
日期:2015-05-24 17:42:07
点击:10274
好评:0
硝酸盐的热分解规律
日期:2015-05-24 17:42:07
点击:10274
好评:0
金属活动顺序表中( m (表示金属)) 例:2KNO 3 2KNO 2 +O 2 ↑ 2Cu(NO 3 ) 2 2CuO+4NO 2 ↑+O 2 ↑ 2AgNO 3 2Ag+2NO 2 ↑+O 2 ↑ 硝酸盐的热分解之二 由于硝酸盐热稳定性差,加热分解时有氧气放出,所以硝酸盐常在高温时作强氧化剂。硝酸盐的热分解规律为: (1)金属活动...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。